Etude de réticulum endoplasmique et mitochondries Interactions par<em> In Situ</em> Proximité Ligation Assay dans des cellules fixes
Summary
Ici, nous décrivons une procédure pour visualiser et de quantifier avec une grande sensibilité les interactions endogènes entre le réticulum endoplasmique et les mitochondries dans les cellules fixes. Le protocole optimisé comprend un essai de ligature de proximité in situ dans le ciblage de l'inositol 1,4,5-triphosphate récepteur / protéine régulée par le glucose 75 / D complexe canal anionique / cyclophiline dépendant de la tension à l'interface de la membrane associée à la mitochondrie.
Abstract
Structural interactions between the endoplasmic reticular (ER) and mitochondrial membranes, in domains known as mitochondria-associated membranes (MAM), are crucial hubs for cellular signaling and cell fate. Particularly, these inter-organelle contact sites allow the transfer of calcium from the ER to mitochondria through the voltage-dependent anion channel (VDAC)/glucose-regulated protein 75 (GRP75)/inositol 1,4,5-triphosphate receptor (IP3R) calcium channeling complex. While this subcellular compartment is under intense investigation in both physiological and pathological conditions, no simple and sensitive method exists to quantify the endogenous amount of ER-mitochondria contact in cells. Similarly, MAMs are highly dynamic structures, and there is no suitable approach to follow modifications of ER-mitochondria interactions without protein overexpression. Here, we report an optimized protocol based on the use of an in situ proximity ligation assay to visualize and quantify endogenous ER-mitochondria interactions in fixed cells by using the close proximity between proteins of the outer mitochondrial membrane (VDAC1) and of the ER membrane (IP3R1) at the MAM interface. Similar in situ proximity ligation experiments can also be performed with the GRP75/IP3R1 and cyclophilin D/IP3R1 pairs of antibodies. This assay provides several advantages over other imaging procedures, as it is highly specific, sensitive, and suitable to multiple-condition testing. Therefore, the use of this in situ proximity ligation assay should be helpful to better understand the physiological regulations of ER-mitochondria interactions, as well as their role in pathological contexts.
Introduction
Mitochondrie et le réticulum endoplasmique (ER) ne sont pas indépendants dans les organites de la cellule, mais ils interagissent structurellement et fonctionnellement au niveau des sites de contact définis comme membranes du réticulum endoplasmique mitochondries-associés (MAM). En effet, MMA propres correspondent à des régions où les membranes du RE et les mitochondries sont étroitement apposés, ce qui permet des interactions entre les protéines des deux côtés. Néanmoins, les membranes de ces organites ne fusionnent pas dans ces régions, de sorte qu'ils maintiennent leurs entités distinctes. Les jouent un rôle MMA propres crucial dans le calcium (Ca 2+) et transfert des phospholipides d'ER aux mitochondries, un impact sur le métabolisme énergétique et la survie des cellules 1-3.
L'association entre l'ER et des mitochondries a été visualisé dans les années 1970 avec la microscopie électronique. Depuis lors, la microscopie électronique à transmission , 4,5, 6,7 tomographie électronique ou immuno-localisation de ER et spécifiques aux mitochondries fluorophores / protéines fluorescentes 8 ont été classiquement utilisés pour étudier les interactions ER-mitochondries. Un autre outil utile pour l'analyse du MAM est basée sur l'utilisation de fractionnement subcellulaire. Elle permet l'isolement des fractions par ultracentrifugation différentielle MAM couplé à un gradient de Percoll 9. Cependant, le produit final contient des fractions enrichies MAM, plutôt que des fractions pures. Au total, ces stratégies ne sont pas particulièrement sensibles et / ou quantitative, et ils ne sont pas facilement se prêtent à une grande sélection. Alternativement, des approches génétiques utilisant fluorescentes linkers inter-organelles de drogue inductible sont apparus, mais ils ne permettent pas l'analyse des interactions des organites aux niveaux d'expression de protéines endogènes 10.
Sur la base de la découverte de Szabadkai du complexe IP3R / GRP75 / VDAC au MAM 11, nous avons développé une méthode quantitative pour analyser les interactions ER-mitochondries. Nous avons utilisé le in situ la proximité ligatile dosage pour détecter et quantifier les interactions entre les VDAC1 et IP3R1, deux protéines de surface des organites impliqués dans le complexe -channeling Ca2 + à l'interface MAM dans les cellules fixes 12. En bref, nous avons sondé VDAC1 à la membrane externe mitochondriale (souris anticorps primaire anti-VDAC1) et IP3R1 à la membrane du RE (lapin anticorps primaire anti-IP3R1) (figure 1, le panneau a). Ensuite, selon le dosage, on a ajouté à la fois anti-souris et anti-lapin IgG (de sondes de dosage de souris et de lapin proximité de ligature), qui sont conjugués à des extensions d'oligonucléotides complémentaires. Si les deux protéines ciblées sont à une distance inférieure à 40 nm, les oligonucléotides peuvent hybrider avec les oligos de connecteur ajoutés ultérieurement pour permettre la formation d'une matrice d'ADN circulaire (Figure 1, panneau b). Cette molécule d'ADN circulaire est ligaturé et amplifié, en créant un produit d'ADN simple brin lié par covalence à l' un des capteurs de proximité (Figure 1, panneau c) </strong>. Comme la distance entre l'ER et les mitochondries à l'interface MAM varie de 10 nm à 25 nm 6, la proximité ligature et l' amplification peuvent être réalisées, conduisant à une détection ultérieure en raison de l'hybridation de Texas oligonucléotides rouges-sondes marquées (Figure 1, panneau d ). Chaque point fluorescent représente les interactions entre VDAC1 / IP3R1, permettant ainsi la quantification in situ des interactions ER-mitochondries dans des cellules individuelles.
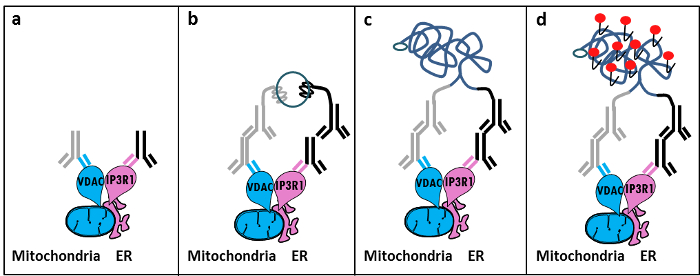
Figure 1: Illustration schématique de la détection des interactions réticulum endoplasmique-mitochondries par In Situ Proximité Ligation Assay. a) un anticorps primaire de souris dirigé contre VDAC1 et un anticorps primaire de lapin dirigé contre IP3R1 peuvent se lier à leurs epitopes à proximité de l'interface MAM, b) l'addition d'une paire de sondes de ligature de proximitédirigé contre la souris et le lapin IgG. Ces sondes sont attachés brins d'ADN qui peuvent former des modèles pour la ligature des oligonucléotides de connecteur. c) Le brin d'ADN circulaire formé après la ligature peut être amplifié , et d) visualisées par microscopie à fluorescence comme un point à l'aide du Texas oligonucléotides marqués au rouge. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Comme dans les expériences d'analyse in situ la proximité de ligature peut être réalisée avec la paire GRP75 / IP3R1 d'anticorps, ainsi que la cyclophiline D (CypD) / anticorps IP3R1, considérant que CypD a été montré pour interagir avec le complexe IP3R / GRP75 / VDAC à l'interface de MAM 12-14.
Protocol
Representative Results
Discussion
Collectively, our studies indicate that the in situ proximity ligation assay is truly a relevant strategy to follow and quantify endogenous ER-mitochondria interactions in fixed cells, without the need for using organelle-specific fluorophores or fluorescent proteins. The specific use of VDAC1/IP3R1 antibodies has been adapted to study ER-mitochondria interactions in HuH7 cells. However, alternative isoforms of VDAC and IP3R may be used, depending on the cell type. In this case, antibodies need to be validated b…
Declarações
The authors have nothing to disclose.
Acknowledgements
Nous remercions toutes les personnes dans notre laboratoire qui ont contribué à optimiser et de valider le protocole. Ce travail a été soutenu par l'INSERM et l'agence nationale de la recherche (ANR-09-JCJC-0116 ET ANR-11-BSV1-033-02). ET a été soutenu au cours de sa thèse par une bourse de recherche du ministère français de l'enseignement supérieur et de la recherche.
Materials
| Formaldehyde | Sigma | F-8775 | |
| Glycine | Sigma | G-8898 | |
| Triton | Sigma | T8532 | |
| 35mm Glass bottom culture dishes | MatTeK corporation | P35G-0-14-C | |
| Blocking solution | Sigma | DUO-92004 or DUO-92002 | provided in the Duolink PLA probes, Sigma |
| VDAC1 antibody | Abcam | ab14734 | |
| IP3R1-H80 antibody | Santa Cruz | sc28614 | |
| CypD antibody | Abcam | ab110324 | |
| Grp75 antibody | Santa Cruz | sc13967 | |
| TBS 10X | euromedex | ET220 | Dilute to obtain 1X |
| Tween 100X | euromedex | 2001-B | dilute in TBS to obtain 0,01% |
| PLA Probes Mouse MINUS | Sigma | DUO-92004 | Duolink, Sigma |
| PLA Probes Rabbit PLUS | Sigma | DUO-92002 | Duolink, Sigma |
| Duolink detection reagents red | Sigma | DUO-92008 | Duolink, Sigma |
| Ligation solution | Sigma | DUO-92008 | Part of the Duolink detection reagents red, Sigma |
| Ligase | Sigma | DUO-92008 | Part of the Duolink detection reagents red, Sigma |
| Amplification solution | Sigma | DUO-92008 | Part of the Duolink detection reagents red, Sigma |
| Polymerase | Sigma | DUO-92008 | Part of the Duolink detection reagents red, Sigma |
| Duolink Mounting Medium | Sigma | DUO80102 | Duolink, Sigma |
| Softwares: | |||
| Blob-finder software | BlobFinder is a freely distributed software that can perform calculations on cells from fluorescence microscopy images. This software can be downloaded for free from The Centre for Image Analysis at Uppsala University who have developed the software and the work was supported by the EU FP6 Project ENLIGHT and Olink Bioscience. http://www.cb.uu.se/~amin/BlobFinder/index_files/Page430.htm | ||
| ImageJ software | Can be downloaded for free from: http://rsb.info.nih.gov/ij/download.html |
Referências
- Bravo-Sagua, R., et al. Organelle communication: signaling crossroads between homeostasis and disease. The international journal of biochemistry & cell biology. 50, 55-59 (2014).
- Giorgi, C., et al. Mitochondria-associated membranes: composition, molecular mechanisms, and physiopathological implications. Antioxidants & redox signaling. 22, 995-1019 (2015).
- Phillips, M. J., Voeltz, G. K. Structure and function of ER membrane contact sites with other organelles. Nature reviews. Molecular cell biology. 17, 69-82 (2016).
- Cosson, P., et al. The RTM resistance to potyviruses in Arabidopsis thaliana: natural variation of the RTM genes and evidence for the implication of additional genes. PLoS One. 7, 39169 (2012).
- Mannella, C. A. Structure and dynamics of the mitochondrial inner membrane cristae. Biochim Biophys Acta. 1763, 542-548 (2006).
- Csordas, G., et al. Structural and functional features and significance of the physical linkage between ER and mitochondria. The Journal of cell biology. 174, 915-921 (2006).
- Mannella, C. A., Buttle, K., Rath, B. K., Marko, M. Electron microscopic tomography of rat-liver mitochondria and their interaction with the endoplasmic reticulum. Biofactors. 8, 225-228 (1998).
- Rizzuto, R., et al. Close contacts with the endoplasmic reticulum as determinants of mitochondrial Ca2+ responses. Science. 280, 1763-1766 (1998).
- Wieckowski, M. R., Giorgi, C., Lebiedzinska, M., Duszynski, J., Pinton, P. Isolation of mitochondria-associated membranes and mitochondria from animal tissues and cells. Nat Protoc. 4, 1582-1590 (2009).
- Csordas, G., et al. Imaging interorganelle contacts and local calcium dynamics at the ER-mitochondrial interface. Mol Cell. 39, 121-132 (2010).
- Szabadkai, G., et al. Chaperone-mediated coupling of endoplasmic reticulum and mitochondrial Ca2+ channels. J Cell Biol. 175, 901-911 (2006).
- Tubbs, E., et al. Mitochondria-associated endoplasmic reticulum membrane (MAM) integrity is required for insulin signaling and is implicated in hepatic insulin resistance. Diabetes. 63, 3279-3294 (2014).
- Paillard, M., et al. Depressing Mitochondria-Reticulum Interactions Protects Cardiomyocytes From Lethal Hypoxia-Reoxygenation Injury. Circulation. 128, 1555-1565 (2013).
- Rieusset, J., et al. Disruption of calcium transfer from ER to mitochondria links alterations of mitochondria-associated ER membrane integrity to hepatic insulin resistance. Diabetologia. 59, 614-623 (2016).
- Allalou, A., Wahlby, C. BlobFinder, a tool for fluorescence microscopy image cytometry. Computer methods and programs in biomedicine. 94, 58-65 (2009).
- Theurey, P., et al. Mitochondria-associated endoplasmic reticulum membranes allow adaptation of mitochondrial metabolism to glucose availability in the liver. Journal of molecular cell biology. , (2016).
- de Brito, O. M., Scorrano, L. Mitofusin 2 tethers endoplasmic reticulum to mitochondria. Nature. 456, 605-610 (2008).
- Soderberg, O., et al. Direct observation of individual endogenous protein complexes in situ by proximity ligation. Nature methods. 3, 995-1000 (2006).
- De Pinto, V., Messina, A., Lane, D. J., Lawen, A. Voltage-dependent anion-selective channel (VDAC) in the plasma membrane. FEBS letters. 584, 1793-1799 (2010).
- Kaul, S. C., Taira, K., Pereira-Smith, O. M., Wadhwa, R. Mortalin: present and prospective. Experimental gerontology. 37, 1157-1164 (2002).

