Biyopololitik katkı maddelerinin varlığında kalsiyum karbonat oluşumu
Summary
Biz biopolymers varlığı şeklinde kalsiyum karbonat kristalleri yağış ve karakterizasyonu için bir protokol açıklanmaktadır.
Abstract
Biomineralizasyon, sıklıkla yaşayan organizmalarda fonksiyonel ve/veya yapısal roller ile ilgili organik moleküllerin varlığında minerallerin oluşumudur. Kompleks bir süreçtir ve bu nedenle basit, in vitro, izole moleküllerin biomineralizasyon sürecinde etkisini anlamak için sistem gereklidir. Birçok durumda, biomineralizasyon, ekstrasellüler matrisinde biyopolimerler tarafından yönlendirilir. İzole biopolymlerin Morfoloji ve kalsit in vitro yapısı üzerinde etkisini değerlendirmek için, kalsiyum karbonat yağlaması için buharı difüzyon yöntemi kullandık, Tarama elektron mikroskobu ve mikro Raman karakterizasyonu için, ve ultraviyole-görünür (UV/vis) kristallerin bir biyopolimer miktarını ölçmek için emici. Bu yöntem, biz izole biopolymers açığa, bir kalsiyum klorür çözeltisi içinde çözünmüş, gazlı amonyak ve karbon dioksit, katı amonyum karbonat debileşimi kaynaklanan. Kalsiyum karbonatın çözünürlük ürününün ulaşabileceği koşullarda, kalsiyum karbonat çökme ve kristaller oluşur. Kalsiyum karbonat, termodinamik istikrarında farklılık gösteren farklı polimorf vardır: amorf kalsiyum karbonat, vaterit, aragonit, ve kalsit. Biopolymers yokluğunda, temiz koşullar altında, kalsiyum karbonat çoğunlukla kalsiyum karbonat en termodinamik istikrarlı polimorf olan kalsit formunda mevcut. Bu yöntem, biyofolymeric katkı maddelerinin kalsiyum karbonat kristallerinin Morfoloji ve yapısına etkisini inceler. Burada, iletişim kuralını, kalsiyum karbonat kristalleri oluşumunda, ekstrüler bir bakteriyel protein, TapA, çalışma yoluyla gösteriyoruz. Özellikle, deneysel olarak ayarlanmış ve optik ve Elektron Mikroskopisi ve Raman spektroskopisi gibi karakterizasyon yöntemlerini odaklanıyoruz.
Introduction
Biomineralizasyon, sıklıkla yaşayan organizmalarda fonksiyonel ve/veya yapısal roller ile ilgili organik moleküllerin varlığında minerallerin oluşumudur. Biomineralizasyon hücre içi olabilir, manyetit içindeki manyetit oluşumunda olduğu gibi1, veya ekstrüküler, deniz atası sivri kalsiyum karbonat oluşumunda olduğu gibi2, içinde kollajen ile ilgili hidroksiapatit kemikler3 ve diş amolgenin ile ilişkili emaye4. Biomineralization, yaşayan organizmadaki birçok parametreye bağlı karmaşık bir süreçtir. Bu nedenle, çalışma altında sistemi basitleştirmek için, işlem üzerinde ayrı bileşenlerin etkisini değerlendirmek gereklidir. Birçok durumda, biomineralizasyon ekstrasellüler biopolymers varlığı ile indüklenir. Burada sunulan yöntemin amacı aşağıdaki gibidir: (1) izole biyopolimerler in vitro varlığını kalsiyum karbonat kristalleri oluşturmak için, bir buhar difüzyon yöntemi kullanarak. (2) biyopolimerler kalsiyum karbonat Morfoloji ve yapısı üzerinde etkisini incelemek için.
Organik katkı maddelerinin varlığına kalsiyum karbonat in vitro çöktmek için üç temel yöntem5,6kullanılır. Çözüm yöntemi olarak atıfta olduğumuz ilk yöntem, çözünür tuz kalsiyum (örn., CaCl2) ile çözünür bir karbonat tuzu (örn., sodyum karbonat) ile karıştırılmaya dayanmaktadır. Karıştırma işlemi çeşitli şekillerde gerçekleştirilebilir: gözenekli membranlarla ayrılan üç hücreli bir reaktör içinde7. Burada, dış hücrelerin her biri çözünür bir tuz içerir ve merkezi hücre, test edilecek katkı maddesi ile bir çözüm içerir. Kalsiyum ve karbonat dış orta hücreye diffuz, daha az çözünür kalsiyum karbonat yağış sonuçlanan zaman kalsiyum ve karbonat konsantrasyonları kendi çözünürlük ürün aşan, KSP = [CA2 +] [Co3 2-]. Ek bir karıştırma yöntemi çift jet prosedürü8‘ dir. Bu yöntemle, her çözünür tuz, kalsiyum karbonat çöktülür katkı içeren bir karıştırıcı çözüm için ayrı bir şırınga enjekte edilir. Burada, enjeksiyon ve bu nedenle karıştırma oranı iyi kontrollü, karışım difüzyon tarafından kontrol edildiği önceki yöntem aksine.
CaCO3 kristalize için kullanılan Ikinci yöntem Kitano Yöntem9‘ dir. Bu yöntem karbonat/hidrojen karbonat dengesine dayanmaktadır (2hco3– (aq) + CA2 +(aq) 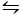 caco3 (s) + Co2 (g) + H2O (l)). Burada, CO2 , katı bir formda caco3 içeren bir çözelti içine bubbled, sol ve bu nedenle kalsiyum karbonat çözünmesi denge kayması. Çözünmemiş kalsiyum karbonat filtrelenir ve istenilen katkı maddeleri bikarbonat zengin çözüme eklenir. CO2 daha sonra buharlığa izin, böylece katkı varlığı içinde kalsiyum karbonat oluşturan, sağa reaksiyon kayması.
caco3 (s) + Co2 (g) + H2O (l)). Burada, CO2 , katı bir formda caco3 içeren bir çözelti içine bubbled, sol ve bu nedenle kalsiyum karbonat çözünmesi denge kayması. Çözünmemiş kalsiyum karbonat filtrelenir ve istenilen katkı maddeleri bikarbonat zengin çözüme eklenir. CO2 daha sonra buharlığa izin, böylece katkı varlığı içinde kalsiyum karbonat oluşturan, sağa reaksiyon kayması.
Burada açıklayacağız kalsiyum karbonat kristalizasyonu, üçüncü yöntem, buharı difüzyon yöntemi10. Bu ayarda, kalsiyum klorür çözeltisi içinde çözünen organik katkı maddesi, bir toz formunda Amonyum karbonat yakınında kapalı bir odaya yerleştirilir. Amonyum karbonat tozu karbondioksit ve amonyak haline geldiğinde, kalsiyum iyonlarının (örn. CaCl2) içeren çözeltisi içine yayılır ve kalsiyum karbonat çöktürülmüştür (bkz. Şekil 1 ). Kalsiyum karbonat kristalleri yavaş yağış veya hızlı yağış ile büyüyebilir. Yavaş yağış için, CaCl2 çözeltisi içinde katkı içeren bir çözüm Amonyum karbonat tozu yanında bir kurutucu yerleştirilir. Protokolde uzunluk olarak açıklanan hızlı yağış, hem katkı çözeltisi hem de Amonyum karbonat çok iyi bir plaka içinde birlikte daha yakın yerleştirilir. Yavaş yağış yöntemi daha az çekirdekleme merkezleri ve daha büyük kristaller üretecek ve hızlı yağış daha çekirdekleme merkezleri ve küçük kristaller neden olur.
Yukarıda açıklanan yöntemler, teknik karmaşıklığı, kontrol düzeyinde ve yağış süreci oranı farklıdır. Karıştırma yöntemi, hem çift Jet hem de üç hücreli sistem için özel bir set-up6 gerektirir. Karıştırma yönteminde, diğer çözünür sayaç iyonlarının varlığı (örn., na+, CL–)6 kaçınılmaz, Kitano yöntemi ise, kalsiyum ve (bi) karbonat çözeltinin tek iyonlarının ve ek varlığı içermez (örn., na+, CL–). Ayrıca, karıştırma yöntemi nispeten büyük hacimli gerektirir ve bu nedenle pahalı biopolymers ile çalışmak için uygun değildir. Çift jetin avantajı, çözüm enjeksiyonu oranını kontrol etmek ve diğer yöntemlere kıyasla hızlı bir süreçtir.
Kitano yöntemi ve buhar difüzyon yönteminin avantajı, kalsiyum karbonat oluşumunun, CO2 ‘ nin bir CAcl2 çözeltisi içine/dışına yayılması ile kontrol edilmesi, böylece daha yavaş çekirdeklenme ve yağış süreçleri için izin verilmesi 11 ‘ i , 12. Ayrıca, Co2 difüzyon ile kalsiyum karbonat oluşumu vivo13,14,15içinde kalsifikasyon süreçleri benzer olabilir. Bu yöntemle, iyi tanımlanmış ve ayrılmış kristaller16oluşturulur. Son olarak, tek veya birden fazla biyopolimerler kalsiyum karbonat oluşumu üzerinde etkisi test edilebilir. Bu da, bir dizi katkı konsantrasyonunun kalsiyum karbonat oluşumuna etkisinin yanı sıra biyopolimerler karışımlarının bir çalışma-tüm kontrollü bir şekilde gerçekleştirilen bir sistematik çalışma sağlar. Bu yöntem, geniş bir yelpazede konsantrasyonları ve hacimleri katkı maddeleri ile kullanılmak için uygundur. Kullanılan en az birim yaklaşık 50 μL ‘dir ve bu nedenle sınırlı miktarda kullanılabilir biopolymers olduğunda bu yöntem avantajlıdır. Maksimal hacim, daha büyük bir iyi plakanın erişilebilirliğine veya CaCl2 içeren plaka veya pancarı yerleştirecek olan kurutucu bağlıdır. Aşağıda açıklanan yöntem bir 96-iyi plaka ile çalışma için optimize edilmiştir protein TapA17olarak seçilmiş bir biyopolimer ile.
Protocol
Representative Results
Discussion
Burada açıklanan yöntem, organik katkı maddelerinin varlığında kalsiyum karbonat kristalleri oluşturma ve organik biyopolymerlerin Morfoloji ve kalsiyum karbonat kristallerinin yapı üzerindeki etkisini değerlendirmek amaçlanmaktadır. Bu yöntem, kontrol deneyinde oluşan kalsit kristalleri için organik katkı maddelerinin varlığını oluşturduğu kristallerin karşılaştırılması üzerine kurulmuştur. Kalsiyum karbonat kristalleri oluşturmak için difüzyon yönteminin nasıl kullanılacağını, op…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Yazarlar, Prof. Lia Addadi, Prof. Jonathan erez ve Dr. Yael Politi ‘ye verimli tartışmalar için teşekkür etmek ister. Bu araştırma Israil Bilim Vakfı (ıSF), Grant 1150/14 tarafından desteklenmektedir.
Materials
| Acetic acid | Gadot | 64-19-7 | |
| Ammonium carbonate | Sigma-Aldrich | 506-87-6 | |
| Calcium chloride dihydrate | Merck KGaA | 10035-04-8 | |
| Ethanol Absolute | Gadot | 64-17-5 | |
| Micro-Raman | Renishaw | inVia Reflex spectrometer coupled with an upright Leica optical microscope | |
| Microscope | Nikon | Eclipse 90i model | |
| Nis elements Br software | Nikon | For microscope imaging | |
| Scanning Electron Microscope | ThermoFisher Scientific | FEI Sirion microscope | |
| Spectrophotometer | JASCO | V-670 model | |
| Sputter coater | Polaron | SC7640 model |
References
- Blakemore, R. Magnetotactic bacteria. Science. 190 (4212), 377-379 (1975).
- Politi, Y., Arad, T., Klein, E., Weiner, S., Addadi, L. Sea Urchin Spine Calcite Forms via a Transient Amorphous Calcium Carbonate Phase. Science. 306 (5699), 1161-1164 (2004).
- Nudelman, F., Lausch, A. J., Sommerdijk, N. A. J. M., Sone, E. D. In vitro models of collagen biomineralization. Journal of Structural Biology. 183 (2), 258-269 (2013).
- Sigel, A., Sigel, H., Sigel, R. K. . Biomineralization: from nature to application. 12, (2008).
- Nielsen, M. H., Lee, J. R. I., De Yoreo, J. J. . Methods in Enzymology. 532, 209-224 (2013).
- Page, M. G., Cölfen, H. Improved Control of CaCO3 Precipitation by Direct Carbon Dioxide Diffusion: Application in Mesocrystal Assembly. Crystal Growth & Design. 6 (8), 1915-1920 (2006).
- Wang, H., Huang, W., Han, Y. Diffusion-reaction compromise the polymorphs of precipitated calcium carbonate. Particuology. 11 (3), 301-308 (2013).
- Sedlák, M., Antonietti, M., Cölfen, H. Synthesis of a new class of double-hydrophilic block copolymers with calcium binding capacity as builders and for biomimetic structure control of minerals. Macromolecular Chemistry and Physics. 199 (2), 247-254 (1998).
- Kitano, Y., Park, K., Hood, D. W. Pure aragonite synthesis. Journal of Geophysical Research. 67 (12), 4873-4874 (1962).
- Politi, Y., Mahamid, J., Goldberg, H., Weiner, S., Addadi, L. Asprich mollusk shell protein: in vitro experiments aimed at elucidating function in CaCO3 crystallization. CrystEngComm. 9 (12), 1171-1177 (2007).
- Gehrke, N., Cölfen, H., Pinna, N., Antonietti, M., Nassif, N. Superstructures of Calcium Carbonate Crystals by Oriented Attachment. Crystal Growth & Design. 5 (4), 1317-1319 (2005).
- Rudloff, J., et al. Double-Hydrophilic Block Copolymers with Monophosphate Ester Moieties as Crystal Growth Modifiers of CaCO3. Macromolecular Chemistry and Physics. 203 (4), 627-635 (2002).
- Boquet, E., Boronat, A., Ramos-Cormenzana, A. Production of Calcite (Calcium Carbonate) Crystals by Soil Bacteria is a General Phenomenon. Nature. 246, 527 (1973).
- Cohen, A. L., McConnaughey, T. A. Geochemical Perspectives on Coral Mineralization. Reviews in Mineralogy and Geochemistry. 54 (1), 151-187 (2003).
- Erez, J. Vital effect on stable-isotope composition seen in foraminifera and coral skeletons. Nature. 273, 199 (1978).
- Azulay, D. N., et al. Biopolymers from a Bacterial Extracellular Matrix Affect the Morphology and Structure of Calcium Carbonate Crystals. Crystal Growth & Design. 18 (9), 5582-5591 (2018).
- Abbasi, R., et al. The Bacterial Extracellular Matrix Protein TapA Is a Two-Domain Partially Disordered Protein. ChemBioChem. , (2018).
- Gauldie, R. W., Sharma, S. K., Volk, E. Micro-raman spectral study of vaterite and aragonite otoliths of the coho salmon, Oncorhynchus kisutch. Comparative Biochemistry and Physiology Part A: Physiology. 118 (3), 753-757 (1997).
- Gasteiger, E., et al. . The Proteomics Protocols Handbook. , 571-607 (2005).
- Gunasekaran, S., Anbalagan, G., Pandi, S. Raman and infrared spectra of carbonates of calcite structure. Journal of Raman Spectroscopy. 37 (9), 892-899 (2006).
- Trushina, D. B., Bukreeva, T. V., Kovalchuk, M. V., Antipina, M. N. CaCO3 vaterite microparticles for biomedical and personal care applications. Materials Science and Engineering: C. 45, 644-658 (2014).
- Weiss, I. M., Tuross, N., Addadi, L., Weiner, S. Mollusc larval shell formation: amorphous calcium carbonate is a precursor phase for aragonite. Journal of Experimental Zoology. 293 (5), 478-491 (2002).
- Yamamoto, Y., Nishimura, T., Saito, T., Kato, T. CaCO3/chitin-whisker hybrids: formation of CaCO3 crystals in chitin-based liquid-crystalline suspension. Polymer Journal. 42, 583 (2010).
- Magnabosco, G., et al. Insights on the interaction of calcein with calcium carbonate and its implications in biomineralization studies. CrystEngComm. 20 (30), 4221-4224 (2018).

