Bereiding van geëxpandeerde chitineschuimen en hun gebruik bij het verwijderen van waterig koper
Summary
Deze studie beschrijft een methode om chitine uit te breiden tot een schuim door chemische technieken die geen gespecialiseerde apparatuur vereisen.
Abstract
Chitine is een onderbenut, van nature overvloedig, mechanisch robuust en chemisch resistent biopolymeer. Deze kwaliteiten zijn wenselijk in een adsorbens, maar chitine mist het noodzakelijke specifieke oppervlak en de wijziging ervan omvat gespecialiseerde technieken en apparatuur. Hierin wordt een nieuwe chemische procedure beschreven voor het uitzetten van chitinevlokken, afgeleid van garnalenschelpafval, in schuimen met een hoger oppervlak. Het proces is gebaseerd op de evolutie van H2-gas uit de reactie van water met NaH gevangen in een chitinegel. De bereidingswijze vereist geen gespecialiseerde apparatuur. Poeder X-ray diffractie en N2-physisorptie geven aan dat de kristallietgrootte afneemt van 6,6 nm tot 4,4 nm en het specifieke oppervlak toeneemt van 12,6 ± 2,1 m2/g tot 73,9 ± 0,2 m2/g. Infraroodspectroscopie en thermogravimetrische analyse geven echter aan dat het proces de chemische identiteit van het chitine niet verandert. De specifieke Cu-adsorptiecapaciteit van het geëxpandeerde chitine neemt toe in verhouding tot het specifieke oppervlak van 13,8 ± 2,9 mg/g tot 73,1 ± 2,0 mg/g. De Cu-adsorptiecapaciteit als oppervlaktedichtheid blijft echter relatief constant bij een gemiddelde van 10,1 ± 0,8 atoom / nm2, wat opnieuw suggereert dat er geen verandering is in de chemische identiteit van het chitine. Deze methode biedt de middelen om chitine om te zetten in een materiaal met een hoger oppervlak zonder de gewenste eigenschappen op te offeren. Hoewel het chitineschuim hier wordt beschreven als een adsorbens, kan het worden voorgesteld als een katalysatorondersteuning, thermische isolator en structureel materiaal.
Introduction
Chitine is een mechanisch robuust en chemisch inert biopolymeer, de tweede alleen voor cellulose in natuurlijke abundantie1. Het is de belangrijkste component in het exoskelet van geleedpotigen en in de celwanden van schimmels en gist2. Chitine is vergelijkbaar met cellulose, maar met één hydroxylgroep van elk monomeer vervangen door een acetylaminegroep (Figuur 1A, B). Dit verschil verhoogt de sterkte van waterstofbinding tussen aangrenzende polymeerketens en geeft chitine zijn karakteristieke structurele veerkracht en chemische inertheid2,3. Vanwege zijn eigenschappen en overvloed heeft chitine aanzienlijke industriële en academische belangstelling aangetrokken. Het is bestudeerd als een steiger voor weefselgroei4,5,6,als een component in composietmaterialen7,8,9,10,11en als ondersteuning voor adsorbentia en katalysatoren11,12,13,14. Met name de chemische stabiliteit maakt chitine aantrekkelijk voor adsorptietoepassingen waarbij aandoeningen betrokken zijn die onherbergzaam zijn voor gewone adsorbentia14. Bovendien maakt de overvloed aan aminegroepen chitine een effectief adsorbens voor metaalionen15. De protonering van de aminegroepen onder zure omstandigheden vermindert echter de metaal adsorptiecapaciteit van chitine16. Een succesvolle strategie is om adsorptieplaatsen te introduceren die beter bestand zijn tegen protonatie17,18. In plaats daarvan wordt hierin een eenvoudige methode beschreven om het specifieke oppervlak en daarom het aantal adsorptieplaatsen in chitine te vergroten.
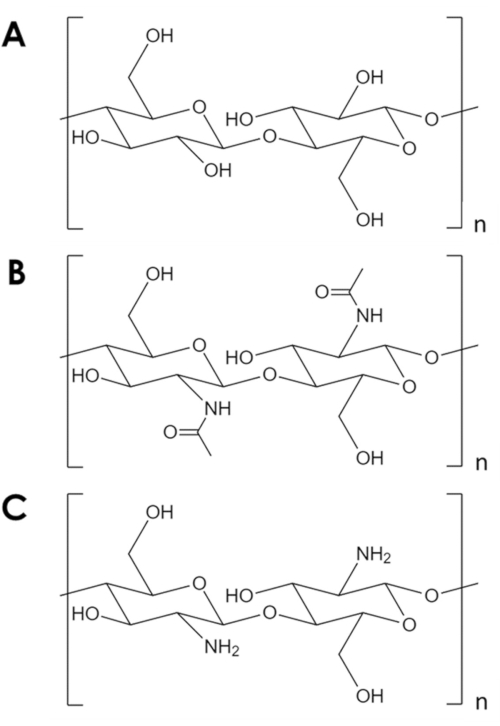
Figuur 1. Chemische structuur. (A) cellulose, (B) chitine, (C) chitosan. Klik hier om een grotere versie van deze figuur te bekijken.
Ondanks de vele potentiële toepassingen, chitine wordt onderbenut. Chitineverwerking is een uitdaging vanwege de lage oplosbaarheid in de meeste oplosmiddelen. Een belangrijke beperking voor het gebruik ervan bij katalyse en adsorptie is het lage specifieke oppervlak. Terwijl typische koolstof- en metaaloxidesteunen specifieke oppervlakken hebben in de orde van 102-103 m2/ g, hebben commerciële chitinevlokken oppervlakten in de orde van grootte van 10 m2/ g19,20,21. Er bestaan methoden om chitine uit te breiden tot schuimen, maar ze zijn steevast afhankelijk van hoge temperatuur en druk, sterke zuren en basen, of gespecialiseerde apparatuur die een belangrijke toegangsdrempel5,21,22,23,24,25vertegenwoordigt. Bovendien hebben deze methoden de neiging om chitine te deacetyleren om chitosan te vormen (Figuur 1C) – een meer oplosbaar en reactief biopolymeer5,25,26.
Hierin wordt een methode beschreven om chitine uit te breiden tot vaste schuimen, het specifieke oppervlak en de adsorptiecapaciteit te vergroten en de chemische integriteit te behouden. De methode is gebaseerd op de snelle evolutie van gas vanuit een chitinegel en vereist geen gespecialiseerde apparatuur. De verhoogde adsorptiecapaciteit van het geëxpandeerde chitine wordt aangetoond met waterige Cu2+-een veel voorkomende verontreiniging in het lokale grondwater26.
| Eenheid | Nette Flake | Gebakken schuim | Gelyofiliseerd schuim | |
| Kristalliniteit | % | 88 | 74 | 58 |
| Kristal grootte | Nm | 6.5 | 4.4 | 4.4 |
| Oppervlakte | m2/g | 12,6 ± 2,1 | 43,1 ± 0,2 | 73,9 ± 0,2 |
| Cu Opname | mg/g | 13,8 ± 2,9 | 48,6 ± 1,9 | 73,1 ± 2,0 |
| Cu Opname | atoom/nm2 | 10,5 ± 2,8 | 10,7 ± 0,4 | 9,4 ± 0,3 |
Tabel 1. Samenvatting van de materiaaleigenschappen. Chitineschuimen hebben een lagere kristalliniteit en kristalgrootte in vergelijking met nette chitinevlokken. Het specifieke oppervlak en de Cu-opname van de chitineschuimen zijn echter verhoudingsgewijs hoger dan die van de nette chitinevlokken.
Protocol
Representative Results
Discussion
De voorgestelde methode voor de fabricage van chitineschuim maakt de productie van dergelijke schuimen mogelijk zonder de noodzaak van gespecialiseerde apparatuur of technieken. De productie van het chitineschuim is afhankelijk van de suspensie van natriumhydride in een chitine sol-gel. Contact met water uit de atmosfeer induceert geleer van de chitinematrix en evolutie van waterstofgas door ontbinding van het natriumhydride. Daarom zijn de kritische stappen van het preparaat (1) vorming van de sol-gel, (2) introductie v…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Het onderzoek werd gesponsord door het Combat Capabilities Development Command Army Research Laboratory (Samenwerkingsovereenkomst Nummer W911NF-15-2-0020). Alle meningen, bevindingen en conclusies of aanbevelingen die in dit materiaal worden uitgedrukt, zijn die van de auteurs en weerspiegelen niet noodzakelijkerwijs de opvattingen van het Army Research Lab.
We bedanken het Center for Advanced Materials Processing (CAMP) aan de Montana Technological University voor het gebruik van enkele van de gespecialiseerde apparatuur die nodig is in deze studie. We bedanken ook Gary Wyss, Nancy Oyer, Rick LaDouceur, John Kirtley en Katherine Zodrow voor de technische assistentie en nuttige discussies.
Materials
| Ammonium bicarbonate | Sigma-Aldrich | 9830 | NH4HCO3, ≥99.5 % |
| Chitin | Sigma-Aldrich | C7170 | Pandalus borealis, practical grade |
| Colorimeter | Hanna Instruments | HI83399-01 | Photometer for wastewater analysis |
| Copper High Range Checker | Hanna Instruments | HI702 | Bicinchoninate colorimetric titration |
| Copper nitrate hydrate | Sigma-Aldrich | 223395 | Cu(NO3)2 · 2.5 H2O, 98 % |
| Dimethylacetamide (DMAc) | Sigma-Aldrich | 271012 | Anhydrous, 99.8 % |
| IR Spectrophotometer | Thermo Nicolet | Nexus 670 | Fitted with an ATR cell |
| Lithium chloride | Sigma-Aldrich | 310468 | LiCl, ≥99 % |
| N2 Physisorption Apparatus | Micromeritics | Tristar II | |
| Nitric acid | BDH | BDH7208-1 | HNO3, 0.1 N |
| Scanning electron microscope | Zeiss LEO | 1430 VP | 15 kV, secondary electron detector, 29-31 mm working distance |
| Sodium hydride | Sigma-Aldrich | 223441 | NaH, packed in mineral oil, 90 % |
| Thermogravimetric analyzer | TA Instruments | Q500 | 100 ml/min N2, 10 °C/min to 800 °C |
| Water Purification System | Millipore | Milli-Q | Type A water (18 MΩ) |
| X-Ray Diffractometer | Rigaku | Ultima IV | Cu K-α radiation, 8.04 keV |
References
- Rinaudo, M. Chitin and chitosan: Properties and applications. Progress in Polymer Science. 31 (7), 603-632 (2006).
- Percot, A., Viton, C., Domard, A. Optimization of chitin extraction from shrimp shells. Biomacromolecules. 4 (1), 12-18 (2003).
- Austin, P. R. Chitin solvents and solubility parameters. Chitin, Chitosan, and Related Enzymes. , 227-237 (1984).
- Deepthi, S., Venkatesan, J., Kim, S. K., Bumgardner, J. D., Jayakumar, R. An overview of chitin or chitosan/nano ceramic composite scaffolds for bone tissue engineering. International Journal of Biological Macromolecules. 93, 1338-1353 (2016).
- Tao, F., et al. Applications of chitin and chitosan nanofibers in bone regenerative engineering. Carbohydrate Polymers. 230, 115658 (2020).
- Zhao, L., et al. Regulation of the morphological and physical properties of a soft tissue scaffold by manipulating DD and DS of O-carboxymethyl chitin. ACS Applied Bio Materials. 3 (9), 6187-6195 (2020).
- Duan, Y., Freyburger, A., Kunz, W., Zollfrank, C. Cellulose and chitin composite materials from an ionic liquid and a green co-solvent. Carbohydrate Polymers. 192, 159-165 (2018).
- Kadokawa, J., Takegawa, A., Mine, S., Prasad, K. Preparation of chitin nanowhiskers using an ionic liquid and their composite materials with poly(vinyl alcohol). Carbohydrate Polymers. 84 (4), 1408-1412 (2011).
- Chen, Z., Wang, J., Qi, H. J., Wang, T., Naguib, H. E. Green and sustainable layered chitin-vitrimer composite with enhanced modulus, reprocessability, and smart actuator function. ACS Sustainable Chemistry and Engineering. 8 (40), 15168-15178 (2020).
- Zhang, Z., Lucia, L. A. Chitin-clay composite gels with enhanced thermal stability prepared in a green and facile approach. Journal of Materials Science. 56 (4), 3600-3611 (2021).
- Ahmed, M. J., Hameed, B. H., Hummadi, E. H. Review on recent progress in chitosan/chitin-carbonaceous material composites for the adsorption of water pollutants. Carbohydrate Polymers. 247, 116690 (2020).
- Matsuoka, A., et al. Hydration of nitriles to amides by a chitin-supported ruthenium catalyst. RSC Advances. 5 (16), 12152-12160 (2015).
- Wang, Y., Li, Y., Liu, S., Li, B. Fabrication of chitin microspheres and their multipurpose application as catalyst support and adsorbent. Carbohydrate Polymers. 120, 53-59 (2015).
- Anastopoulos, I., Bhatnagar, A., Bikiaris, D., Kyzas, G. Chitin Adsorbents for Toxic Metals: A Review. International Journal of Molecular Sciences. 18 (1), 114 (2017).
- Habiba, U., Afifi, A. M., Salleh, A., Ang, B. C. Chitosan/(polyvinyl alcohol)/zeolite electrospun composite nanofibrous membrane for adsorption of Cr6+, Fe3+ and Ni2+. Journal of Hazardous Materials. 322, 182-194 (2017).
- Kim, U. J., et al. Protein adsorption of dialdehyde cellulose-crosslinked chitosan with high amino group contents. Carbohydrate Polymers. 163, 34-42 (2017).
- He, Y., et al. Fabrication of PVA nanofibers grafted with octaamino-POSS and their application in heavy metal adsorption. Journal of Polymers and the Environment. , (2020).
- Tian, H., et al. Electrospinning of polyvinyl alcohol into crosslinked nanofibers: An approach to fabricate functional adsorbent for heavy metals. Journal of Hazardous Materials. 378, (2019).
- Meille, V. Review on methods to deposit catalysts on structured surfaces. Applied Catalysis A: General. 315, 1-17 (2006).
- Dotto, G. L., Cunha, J. M., Calgaro, C. O., Tanabe, E. H., Bertuol, D. A. Surface modification of chitin using ultrasound-assisted and supercritical CO2 technologies for cobalt adsorption. Journal of Hazardous Materials. 295, 29-36 (2015).
- Phongying, S., Aiba, S., Chirachanchai, S. Direct chitosan nanoscaffold formation via chitin whiskers. Polymer. 48 (1), 393-400 (2007).
- Tan, T. S., Chin, H. Y., Tsai, M. L., Liu, C. L. Structural alterations, pore generation, and deacetylation of α- and β-chitin submitted to steam explosion. Carbohydrate Polymers. 122, 321-328 (2015).
- Chang, F. S., Chin, H. Y., Tsai, M. L. Preparation of chitin with puffing pretreatment. Research on Chemical Intermediates. 44 (8), 4939-4955 (2018).
- Goodrich, J. D., Winter, W. T. α-Chitin Nanocrystals prepared from shrimp shells and their specific surface area measurement. Biomacromolecules. 8 (1), 252-257 (2007).
- Rolandi, M., Felts, J. . Naturally sourced chitin foam. , (2020).
- McDermott, S., Hailer, M. K., Lead, J. R. Meconium identifies high levels of metals in newborns from a mining community in the U.S. Science of the Total Environment. 707, 135528 (2020).
- Hach Handbook of Water Analysis. Copper, Bicinchoninate Method, Method 8506. Hach Handbook of Water Analysis. , (1979).
- Crittenden, J. C., Trusell, R. R., Hand, D. R., Howe, K. J., Tchbanoglous, G. Adsorption. MWH’s Water Treatment. , 1117 (2012).
- Focher, B., Beltrame, P. L., Naggi, A., Torri, G. Alkaline N-deacetylation of chitin enhanced by flash treatments. Reaction kinetics and structure modifications. Carbohydrate Polymers. 12 (4), 405-418 (1990).
- Scherrer, P. Determination of the size and the internal structure of colloidal particles by means of X-rays. News from the Society of Sciences in Göttingen, Mathematical- Physical Class. 2, 98-100 (1918).
- Brunauer, S., Emmett, P. H., Teller, E. Adsorption of gases in multimolecular layers. Journal of the American Chemical Society. 60 (2), 309-319 (1938).
- Sing, K. S. W. Adsorption methods for the characterization of porous materials. Advances in Colloid and Interface Science. 76-77, 3-11 (1998).
- Rouquerol, J., Llewellyn, P., Rouquerol, F. Is the bet equation applicable to microporous adsorbents. Studies in Surface Science and Catalysis. 160, 49-56 (2007).
- Vorokh, A. S. Scherrer formula: estimation of error in determining small nanoparticle size. Nanosystems: Physics, Chemistry, Mathematics. , 364-369 (2018).
- Labidi, A., Salaberria, A. M., Fernandes, S. C. M., Labidi, J., Abderrabba, M. Adsorption of copper on chitin-based materials: Kinetic and thermodynamic studies. Journal of the Taiwan Institute of Chemical Engineers. 65, 140-148 (2016).
- Tian, M., Zhao, T. Q., Chin, P. L., Liu, B. S., Cheung, A. S. -. C. Methane and propane co-conversion study over zinc, molybdenum and gallium modified HZSM-5 catalysts using time-of-flight mass-spectrometry. Chemical Physics Letters. 592, 36-40 (2014).

