Un dépistage comportemental des crises induites par la chaleur dans des modèles murins d’épilepsie
Summary
Le but de la méthode est de dépister l’hyperthermie ou les crises induites par la chaleur dans des modèles murins. Le protocole décrit l’utilisation d’une chambre construite sur mesure avec une surveillance continue de la température corporelle pour déterminer si une température corporelle élevée entraîne des convulsions.
Abstract
Les modèles murins transgéniques se sont révélés être des outils puissants dans l’étude de divers aspects des troubles neurologiques humains, y compris l’épilepsie. Les épilepsies génétiques associées au SCN1A comprennent un large éventail de troubles épileptiques avec une pénétrance incomplète et une variabilité clinique. Les mutations SCN1A peuvent entraîner une grande variété de phénotypes épileptiques allant de simples convulsions fébriles associées à la fièvre (FS) auto-limitées, à l’épilepsie génétique de niveau modéré avec convulsions fébriles plus (GEFS +) au syndrome de Dravet (DS) plus sévère. Bien que les FS soient couramment observés chez les enfants de moins de 6 à 7 ans qui ne souffrent pas d’épilepsie génétique, les FS chez les patients GEFS+ continuent de se produire à l’âge adulte. Traditionnellement, les FS expérimentales ont été induites chez la souris en exposant l’animal à un flux d’air sec ou à des lampes chauffantes, et le taux de changement de la température corporelle n’est souvent pas bien contrôlé. Ici, nous décrivons une chambre de chauffage sur mesure, avec une façade en plexiglas, équipée d’un régulateur de température numérique et d’un ventilateur électrique équipé d’un chauffage, qui peut envoyer de l’air forcé chauffé dans l’arène de test de manière contrôlée par la température. La température corporelle d’une souris placée dans la chambre, surveillée par une sonde rectale, peut être augmentée à 40-42 °C de manière reproductible en augmentant la température à l’intérieur de la chambre. La surveillance visuelle continue des animaux pendant la période de chauffage démontre l’induction de crises induites par la chaleur chez les souris porteuses d’une mutation FS à une température corporelle qui ne provoque pas de crises comportementales chez les compagnons de portée de type sauvage. Les animaux peuvent être facilement retirés de la chambre et placés sur un coussin de refroidissement pour ramener rapidement la température corporelle à la normale. Cette méthode fournit un protocole de dépistage simple, rapide et reproductible pour l’apparition de crises induites par la chaleur dans des modèles murins d’épilepsie.
Introduction
L’épilepsie, la quatrième famille la plus courante de troubles neurologiques aux États-Unis1, se caractérise par un déséquilibre de la pulsion excitatrice et inhibitrice dans le SNC qui conduit à des crises récurrentes. Des convulsions fébriles (FS) ou des convulsions associées à la fièvre peuvent survenir dans la population générale, le plus souvent chez les enfants dès l’âge de 3 mois à 6-7 ans. Cependant, chez certaines personnes présentant des mutations génétiques, le plus souvent dans un gène du canal sodique, la FS peut persister au-delà de l’âge de 7 ans à l’âge adulte. Cette condition est appelée convulsions fébriles plus ou FS +. Les progrès rapides dans le séquençage du génome ont permis d’identifier plus de 1 300 mutations dans le gène du canal ionique sodium humain SCN1A, ce qui en fait un point chaud pour les mutations de l’épilepsie. Les mutations SCN1A ont été liées à un large éventail de troubles épileptiques, y compris les convulsions fébriles (FS), l’épilepsie génétique avec convulsions fébriles plus (GEFS +) et le syndrome de Dravet (DS)2,3,4,5,6. Environ 20% des mutations faux-sens SCN1A conduisent à GEFS + 5,7,8. Les antécédents pédiatriques de SS complexes ou prolongés dans l’enfance peuvent par la suite se transformer en formes plus débilitantes d’épilepsie telles que l’épilepsie du lobe temporal (TLE)9,10,11. Le syndrome de Dravet survient en raison de mutations de troncature ou de perte de mutations fonctionnelles dans SCN1A et est une forme grave d’épilepsie intraitable, avec l’apparition chez l’enfant de convulsions fébriles qui se transforment en crises réfractaires, et est souvent associé à des déficiences cognitives, développementales et motrices2,5,12 . Étant donné que de nombreuses personnes atteintes de GEFS+ et/ou de DS présentent des convulsions fébriles, il devient impératif de développer de nouvelles thérapies pour mieux lutter contre ces troubles épileptiques.
Les modèles animaux d’épilepsie associée au SCN1A se sont révélés inestimables pour caractériser différents types de crises (fébriles vs généralisées) et disséquer le mécanisme neuronal de génération de crises13,14,15,16,17,18. Bien que l’étude des crises spontanées via des enregistrements EEG / EMG dans le cerveau des rongeurs soit bien établie et constitue un outil très utile, seules quelques études ont tenté d’imiter les crises fébriles dans des modèles murins14,16,19,20,21,22,23 . Des études antérieures ont utilisé un jet d’air sec chauffé, ou un cylindre de méthacrylate équipé d’un système thermique, ou des lampes chauffantes avec un régulateur de température dans des arènes d’essai fermées9,16,21,22,23,24 pour induire des crises par hyperthermie. Afin d’augmenter la température corporelle dans un environnement plus contrôlé, le protocole décrit ici utilise une chambre construite sur mesure avec un système de chauffage à température contrôlée qui a permis des taux reproductibles d’augmentation de la température corporelle d’une souris à l’intérieur de la chambre. La chambre de chauffage a été construite en bois (longueur 40 cm x largeur 34 cm x hauteur 31 cm) et a été équipée d’un régulateur de température numérique avec un thermocouple K. Un petit ventilateur axial équipé d’un réchauffeur sur le panneau arrière de la chambre dirige l’air chauffé dans la chambre régulée par un régulateur de température numérique. Ce système de chauffage à air pulsé permet de contrôler la vitesse à laquelle la température de la chambre augmente. (Figure 1A,B). Le thermocouple K situé à l’intérieur de la chambre de chauffage en bois envoie un retour d’information au régulateur de température numérique, afin de maintenir des températures constantes à l’intérieur de la boîte pendant le test. Le réglage de la température sur le régulateur de température numérique permet au ventilateur électrique d’envoyer de l’air forcé chauffé à travers les bouches d’aération pour chauffer uniformément la chambre (Figure 1A). Le panneau avant de la chambre de chaleur est une feuille de plexiglas transparent pour permettre un enregistrement vidéo facile des essais.
Des souris adultes (P30-P40), hétérozygotes pour une mutation faux-sens dans SCN1A qui provoque GEFS+ et un nombre égal de compagnons de portée de type sauvage servant de groupe témoin, ont été sélectionnées pour chaque expérience. Les animaux, mâles et femelles, utilisés dans ces études pesaient au moins 15 g, car les souris de type sauvage pesant moins étaient plus sensibles aux crises induites par la chaleur que les animaux plus lourds du même âge. Dans l’étude pilote, on a observé des souris mutantes et de type sauvage à la recherche des coins les plus froids de la chambre à l’arrière et y sont restées pendant de longues périodes. Pour contourner ce problème, la taille effective du plancher à l’intérieur de l’arène d’essai de la chambre thermique a été réduite à 16,5 cm x largeur 21,5 cm x hauteur 27,5 cm en plaçant un bloc de bois B (dimensions 20 cm x 8 cm x 7,2 cm) sur le côté droit de la chambre (Figure 1A). La chambre thermique a été construite en contreplaqué de 1,9 cm d’épaisseur (longueur 40 cm x largeur 34 cm x hauteur 31 cm) recouvert de stratifié blanc et équipé d’un régulateur de température numérique avec un thermocouple K. La surface stratifiée des parois de la chambre est imperméable et peut être facilement désinfectée entre les essais en essuyant avec 70% d’éthanol. La température de la chambre thermique a d’abord été réglée à 50 °C et préchauffée pendant au moins 1 h avant le début de l’expérience, afin d’assurer un chauffage uniforme à l’intérieur de la chambre. Chaque souris a été équipée d’un thermomètre rectal pour une surveillance continue de la température corporelle tout au long de l’expérience. Une seule souris a été placée dans la chambre à la fois et la température a été maintenue à 50 ° C entre la 1ère et la 10ème minute. La température a ensuite été portée à 55 °C pendant la 11e à la 20e minute, puis à 60 °C pendant la 21e à la 30e minute. Il en a résulté un taux reproductible d’augmentation de la température corporelle de la souris (Figure 2A). Chaque essai a été filmé et l’analyse comportementale a été menée hors ligne.
Le protocole de chauffage peut être facilement modifié pour changer la température initiale de la chambre thermique et la vitesse à laquelle la chambre est chauffée, ce qui modifie à son tour la vitesse à laquelle la température corporelle de la souris est élevée pendant le test. Ainsi, cette méthode offre plus de flexibilité par rapport aux méthodes traditionnelles dans la mise en place des écrans comportementaux impliquant des crises induites par la chaleur. Le protocole de crise induite par la chaleur peut également être utilisé pour dépister les médicaments antiépileptiques qui rendent les souris mutantes plus résistantes aux crises induites par la chaleur ou augmentent la température seuil à laquelle les crises sont observées. De même, les effets bénéfiques des régimes restrictifs tels que le régime céto sur les crises induites par la chaleur peuvent être examinés chez les souris normales nourries au chow par rapport aux souris nourries au céto.
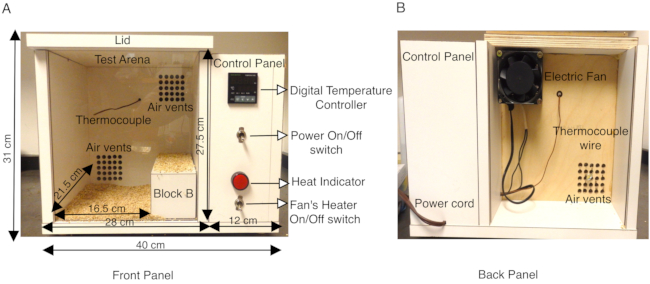
Figure 1 : Description de la chambre chauffante de la souris construite sur mesure. (A) Le panneau avant de la chambre chauffante en bois de la souris montre le panneau de commande latéral contenant l’interrupteur Power ON/OFF qui allume le régulateur de température numérique, le thermocouple K, l’interrupteur ON/OFF du radiateur soufflant et l’indicateur de chaleur. Les dimensions extérieures de la boîte et de l’arène de test intérieure sont indiquées en cm. Un bloc de bois B utilisé pour réduire efficacement la surface de l’arène d’essai est également montré. Le fond de l’arène de test est recouvert de litière en torchis pour empêcher les souris d’entrer directement en contact avec des surfaces en bois chauffées. (B) Le panneau arrière de la chambre de chaleur montre le ventilateur monté sur l’aération supérieure et le cordon d’alimentation pour fournir de l’électricité à la chambre. Cette figure est modifiée à partir de la figure 3 dans Das et al., 2021, eNeuro14. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Protocol
Representative Results
Discussion
Nous décrivons un protocole simple et efficace pour dépister l’apparition de crises induites par la chaleur chez la souris, l’équivalent comportemental des crises fébriles chez les patients humains. Le test évalue plusieurs paramètres – y compris le pourcentage de souris présentant des convulsions, le seuil de crise, la gravité des crises sur une échelle de Racine, afin de comparer la sensibilité des groupes de souris témoins et de test à l’augmentation de la température corporelle.
Une étape critique de ce protocole consiste à augmenter la chaleur dans la chambre tout en surveillant en permanence la température corporelle de la souris. Il est impératif que la température corporelle maximale que les souris connaîtront dans ces essais soit de 44 ° C, car les animaux de type sauvage peuvent subir des crises induites par la chaleur à des températures corporelles >44 ° C. Le prétraitement sous anesthésie générale ou analgésiques pourrait réduire la température corporelle centrale des animaux ou interférer avec la thermorégulation, ce qui à son tour confondrait la collecte de données sur la température du seuil de saisie. Ainsi, les souris sous ce protocole de dépistage n’ont pas pu recevoir ces agents pendant la fenêtre d’essai de 30 minutes. Toutes les procédures doivent être approuvées par le comité de l’IACUC de l’institution. Pour assurer une surveillance continue de la température corporelle centrale de la souris pendant le test, collez solidement la sonde de température rectale à la queue des souris. Si, pendant le test, la température corporelle de la souris reste inchangée pendant de longues périodes, même après avoir augmenté la température de la chambre de la souris, assurez-vous que la sonde de température rectale n’est pas sortie de la souris ou n’est pas attachée lâchement à la queue.
Le contexte génétique des modèles murins peut affecter la sensibilité à la mutation SCN1A et aux crises pharmacologiquement induites18,25,26,27. Comme discuté dans les résultats ci-dessus, le fond génétique des souris peut influencer leur susceptibilité aux crises induites par la chaleur. Scn1a Des souris mutantes K1270T GEFS+ ont été testées dans deux contextes génétiques – 129X1 et B6NJ, et un faible pourcentage de souris de type sauvage (33%) dans le fond B6NJ sensible aux crises, ont également été observées pour subir des crises induites par la chaleur. Cependant, par rapport aux souris mutantes hétérozygotes Scn1aKT/+, les souris de type sauvage B6NJ ont connu des crises induites par la chaleur à un seuil de température significativement plus élevé. Cela confirme que la mutation génétique (Scn1a K1270T) introduite par CRISPR knock-in rend les souris mutantes plus sensibles aux crises induites par l’hyperthermie.
L’adoption de ce protocole présente plusieurs avantages, qui sont résumés ci-dessous. Tout d’abord, contrairement à l’utilisation d’un courant d’air sec ou de lampes chauffées, un air forcé à température contrôlée installé dans un espace clos offre à l’expérimentateur plus de contrôle sur le chauffage de l’arène d’essai à la vitesse souhaitée. Les étapes du protocole de chauffage peuvent être facilement modifiées pour augmenter / diminuer la température de départ, la durée de chaque étape, etc. pour dépister les souris plus âgées qui sont des rongeurs plus lourds ou plus gros tels que les rats. Deuxièmement, la surveillance continue de la température corporelle de la souris via la sonde rectale attachée fournit des informations précieuses sur le taux de changement de température corporelle chez chaque souris, tout au long du test. Cela permet à l’expérimentateur d’observer de près que le taux de changement de température chez la souris ne dépasse pas 0,25-0,5 ° C / min (ce qui pourrait être stressant pour les animaux), lors de l’adaptation de ce protocole à d’autres arènes de test. Il est important de noter que le taux de changement de la température corporelle au fil du temps dans différents groupes de souris peut faire la lumière sur leur capacité à thermoréguler et pourrait être utile pour comprendre si les convulsions fébriles causant des mutations modifient également la thermorégulation chez la souris. Troisièmement, la surveillance continue de la température corporelle garantit que les mesures de température du seuil de saisie à l’aide de ce protocole sont exactes, car elles sont enregistrées en même temps que le premier épisode de crise subi par la souris. Si la température corporelle de l’animal n’est pas surveillée en permanence ou si la température du seuil de saisie est mesurée après avoir sorti l’animal de l’arène d’essai, les valeurs seuils de saisie peuvent varier en raison du temps nécessaire pour manipuler les souris après les crises. Enfin, cette méthode contourne la nécessité d’utiliser des méthodes invasives pour induire de la fièvre (en injectant des agents pathogènes) chez la souris afin d’imiter les convulsions fébriles chez les patients humains.
L’une des limites de ce protocole est qu’il est difficile de dépister les souris juvéniles (moins de P30 en âge) pour les crises induites par la chaleur. Le protocole a été développé pour dépister la sensibilité des souris adultes (P30-P40 et plus) aux crises induites par la chaleur ou l’hyperthermie. D’après notre expérience, les jeunes souris de type sauvage, en particulier celles pesant moins de 15 g, sont plus susceptibles de subir des crises induites par la chaleur, ce qui pourrait être dû à des mécanismes de thermorégulation sous-développés, à un stress thermique physiologique ou à une combinaison des deux. Par conséquent, il n’est pas idéal d’effectuer le dépistage des crises induites par la chaleur sur des souris juvéniles en utilisant ce protocole.
Des études futures qui combinent la surveillance EEG tout en soumettant la souris à des crises induites par la chaleur peuvent faire la lumière sur les modèles de crises EEG des crises induites par la chaleur, similaires à une étude précédente19. L’activité neuronale dans des zones spécifiques du cerveau de la souris peut être tracée en combinant des approches optogénétiques et des études basées sur l’immunohistochimie après la récolte du tissu cérébral. En outre, les effets des régimes restrictifs tels que le régime céto sur la réduction des convulsions fébriles peuvent être évalués en soumettant les souris nourries au céto et les souris normales nourries au chow au protocole de crise induite par la chaleur. De même, des paradigmes de dépistage des médicaments contre l’épilepsie peuvent être développés pour tester et identifier les médicaments antiépileptiques candidats qui améliorent ou suppriment les crises induites par la chaleur chez les souris nourries ou traitées par rapport aux souris nourries au véhicule ou témoins.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Nous tenons à remercier Connor J. Smith pour son aide dans la construction de la chambre chauffante personnalisée de la souris. Nous reconnaissons l’aide des membres du laboratoire O’Dowd, Lisha Zeng et Andrew Salgado, pour normaliser le protocole de chauffage au cours des premières étapes du développement du test. Nous remercions également Danny Benavides et Kumar Perinbam pour l’enregistrement vidéo de certaines parties de la procédure expérimentale du manuscrit. Ce travail a été soutenu par la subvention nih (NS083009) accordée à D.O.D.
Materials
| Axial fan | Farnam | AF20-200-120-xx10-3.1 | Farnam custom products -Axial Fan Heater with Fan |
| Digital temperature controller | Inkbird | ITC-100RH | Inkbird digital PID temperature controller ITC-100RH with K thermocouple |
| Mouse rectal temperature probe | ThermoWorks, Braintree Scientific, Inc | RET-3 | Mouse rectal temperature probe with thermometer |
References
- Hirtz, D., et al. How common are the ‘common’ neurologic disorders. Neurology. 68, 326-337 (2007).
- Catterall, W. A. Sodium Channel Mutations and Epilepsy. Jasper’s Basic Mechanisms of the Epilepsies. , (2012).
- Mantegazza, M., Broccoli, V. SCN 1A /Na V 1.1 channelopathies: Mechanisms in expression systems, animal models, and human iPSC models. Epilepsia. 60, (2019).
- Stafstrom, C. E. Persistent Sodium Current and Its Role in Epilepsy. Epilepsy Currents. 7, 15-22 (2007).
- Schutte, S. S., Schutte, R. J., Barragan, E. V., O’Dowd, D. K. Model systems for studying cellular mechanisms of SCN1A-related epilepsy. Journal of Neurophysiology. 115, 1755-1766 (2016).
- Wei, F., et al. Ion Channel Genes and Epilepsy: Functional Alteration, Pathogenic Potential, and Mechanism of Epilepsy. Neuroscience Bulletin. 33, 455-477 (2017).
- Abou-Khalil, B., et al. Partial and generalized epilepsy with febrile seizures plus and a novel SCN1A mutation. Neurology. 57, 2265-2272 (2001).
- Zhang, Y. -. H., et al. Genetic epilepsy with febrile seizures plus: Refining the spectrum. Neurology. 89, 1210-1219 (2017).
- Patterson, K. P., et al. Enduring memory impairments provoked by developmental febrile seizures are mediated by functional and structural effects of neuronal restrictive silencing factor. Journal of Neuroscience. 37, 3799-3812 (2017).
- Rossi, M. A. SCN1A and febrile seizures in mesial temporal epilepsy: An early signal to guide prognosis and treatment. Epilepsy Currents. 14, 189-190 (2014).
- Zhang, Y., et al. Altered gut microbiome composition in children with refractory epilepsy after ketogenic diet. Epilepsy Research. 145, 163-168 (2018).
- Meng, H., et al. The SCN1A mutation database: Updating information and analysis of the relationships among genotype, functional alteration, and phenotype. Human Mutation. 36, 573-580 (2015).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Das, A., et al. Interneuron dysfunction in a new mouse model of SCN1A GEFS. eNeuro. , (2021).
- Kalume, F., et al. Sudden unexpected death in a mouse model of Dravet syndrome. Journal of Clinical Investigations. 123, 1798-1808 (2013).
- Martin, M. S., et al. Altered function of the SCN1A voltage-gated sodium channel leads to gamma-aminobutyric acid-ergic (GABAergic) interneuron abnormalities. Journal of Biological Chemistry. 285, 9823-9834 (2010).
- Rubinstein, M., et al. Dissecting the phenotypes of Dravet syndrome by gene deletion. Brain. 138, 2219-2233 (2015).
- Yu, F. H., et al. Reduced sodium current in GABAergic interneurons in a mouse model of severe myoclonic epilepsy in infancy. Nature Neuroscience. 9, 1142-1149 (2006).
- Dutton, S. B. B., et al. Early-life febrile seizures worsen adult phenotypes in Scn1a mutants. Experimental Neurology. 293, 159-171 (2017).
- Cheah, C. S., et al. Specific deletion of NaV1.1 sodium channels in inhibitory interneurons causes seizures and premature death in a mouse model of Dravet syndrome. Proceedings of the National Academy of Science U.S.A. 109, 14646-14651 (2012).
- Oakley, J. C., Cho, A. R., Cheah, C. S., Scheuer, T., Catterall, W. A. Synergistic GABA-enhancing therapy against seizures in a mouse model of Dravet Syndrome. Journal of Pharmacology and Experimental Therapeutics. 345, 215-224 (2013).
- Ricobaraza, A., et al. Epilepsy and neuropsychiatric comorbidities in mice carrying a recurrent Dravet syndrome SCN1A missense mutation. Scientific Reports. 9, (2019).
- Warner, T. A., Liu, Z., Macdonald, R. L., Kang, J. -. Q. Heat induced temperature dysregulation and seizures in Dravet Syndrome/GEFS+ Gabrg2+/Q390X mice. Epilepsy Research. 134, 1-8 (2017).
- Eun, B. -. L., Abraham, J., Mlsna, L., Kim, M. J., Koh, S. Lipopolysaccharide potentiates hyperthermia-induced seizures. Brain and Behavior. 5, 00348 (2015).
- Miller, A. R., Hawkins, N. A., McCollom, C. E., Kearney, J. A. Mapping genetic modifiers of survival in a mouse model of Dravet syndrome. Genes Brain and Behavior. 13, 163-172 (2013).
- Mistry, A. M., et al. Strain- and age-dependent hippocampal neuron sodium currents correlate with epilepsy severity in Dravet syndrome mice. Neurobiology of Disease. 65, 1-11 (2014).
- Ogiwara, I., et al. Nav1.1 localizes to axons of parvalbumin-positive inhibitory interneurons: a circuit basis for epileptic seizures in mice carrying an Scn1a gene mutation. Journal of Neuroscience. 27, 5903-5914 (2007).

