Modellazione di voltammetria ciclica veloce dei dati da dati neurotrasmettivali elettromagnetici a dopamina utilizzando QNsim1.0
Summary
La voltammetria ciclica veloce può monitorare la neurotrasmissione dopamina in vivo nel contesto di farmaci, malattie e altre manipolazioni sperimentali. Questo lavoro descrive l'implementazione di QNsim1.0, un software per modellare le risposte dopaminiche stimolate elettricamente secondo il modello quantitativo neurobiologico per quantificare le stime della dinamica di rilascio e di reuptake della dopamina.
Abstract
I percorsi dopaminergici centrali (DAergic) hanno un ruolo importante in una vasta gamma di funzioni, come l'attenzione, la motivazione e il movimento. La dopamina (DA) è implicata in malattie e disturbi tra cui disordine di iperattività, deficit di attenzione, malattia di Parkinson e lesioni cerebrali traumatiche. Quindi, la neurotrasmissione DA ei metodi per lo studio sono di interesse scientifico intenso. La voltammetria ciclica veloce di scansione in vivo (FSCV) è un metodo che consente di monitorare selettivamente i cambiamenti di concentrazione di DA con una risoluzione fine temporale e spaziale. Questa tecnica è comunemente usata in combinazione con stimoli elettrici di ascendenti vie DAergiche per controllare il flusso impulsivo della neurotrasmissione della dopamina. Sebbene il paradigma di neurotrasmissione DA stimolato possa produrre robuste risposte DA con morfologie chiare, rendendole suscettibili di analisi cinetiche, c'è ancora molto dibattito su come interpretare le risposte in termini di rilascio di DA e chiareCe componenti. Per affrontare questa preoccupazione, è stato recentemente sviluppato un quadro quantitativo neurobiologico (QN) di stimolato neurotrasmissione DA per modellare realisticamente le dinamiche di rilascio e reuptake di DA nel corso di una risposta stimolata DA. Le basi di questo modello sono basate su dati sperimentali provenienti da stimolati neurotrasmissione DA e su principi di neurotrasmissione adottati da varie linee di ricerca. Il modello QN implementa 12 parametri relativi alla stimolazione della dinamica di rilascio e di ricupero DA per modellare le risposte DA. Questo lavoro descrive come simulare le risposte DA utilizzando QNsim1.0 e anche dettagli i principi che sono stati implementati per discernere sistematicamente le alterazioni nella stimolazione della dopamina di rilascio e di reuptake.
Introduction
La neurotrasmissione della dopamina (DA) svolge un ruolo essenziale nelle varie funzioni cognitive e comportamentali, e la sua disfunzione è implicata in varie malattie e disturbi comuni. In quanto tale, è fondamentale sviluppare metodi accurati per studiare quantitativamente la neurotrasmissione DA in vivo per valutare come la neurotrasmissione DA sia alterata nei contesti dei modelli di malattia e della farmacologia farmacologica. La voltammetria ciclica veloce (FSCV) consente di monitorare la neurotrasmissione in vivo DA con una risoluzione fine spaziale e temporale. Mentre è possibile monitorare la neurotrasmissione fisiologica DA in animali svegli e liberamente comportati, la stimolazione elettrica dei percorsi dopaminergici ascendenti in animali anestetizzati può produrre risposte robuste DA che sono suscettibili di una migliore analisi cinetica della neurotrasmissione DA.
Le risposte DA stimolate elettricamente riflettono un gioco dinamico di rilascio e reuptake DA e interpretazioniDi queste risposte hanno utilizzato prevalentemente un modello semplice di stimolazione della neurotrasmissione DA chiamata il modello Michaelis-Menten (MM) 12 . Il modello MM è costituito da 3 variabili per descrivere le risposte DA in termini di velocità di rilascio DA costante e di efficienza di reuptake costante ( cioè, la relazione tra il tasso di reuptake DA e le concentrazioni di extracellulari DA), come descritto nell'equazione 1 : 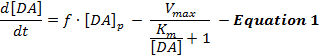
(Rilascio DA) (ricupero DA)
Nell'equazione 1, f è la frequenza di stimolazione; [DA] p è l'aumento stimato della concentrazione DA per impulso di stimolazione; V max rappresenta il tasso massimo di ricupero stimato; E K m è la costante MM stimata, che è teoricamente equivalente alla concentrazione di DA extracellulare che satura il 50% di DAT, portando ad una velocità di ricuprimento half-maximal. Questo è diversoL'equazione può essere integrata per simulare le risposte DA sperimentali stimando i parametri [DA] p , V max e K m .
Anche se il modello MM ha facilitato notevoli progressi nella comprensione della cinetica di neurotrasmissione DA in vari contesti sperimentali, il modello MM rende ipotesi fondamentali semplici che limitano la sua applicabilità quando si modellano le risposte DA ottenute da stimoli suprafisiologici 2 , 13 . Ad esempio, il modello MM può approssimare solo le forme di risposta DA se ascendono in modo convesso, ma non possono rappresentare le risposte graduali (concave) che si trovano nelle regioni striatali dorsali 12 . Quindi, le ipotesi di modello MM non acquisiscono con precisione i processi di rilascio dinamico e di reuptake della stimolata neurotrasmissione DA.
Modellare le risposte DA stimolate in base a un quant realisticoIl quadro quantitativo neurobiologico (QN) è stato sviluppato sulla base di principi di cinetica stimolata di neurotrasmissione derivata dalla ricerca complementare e dalla sperimentazione 2 . Diverse linee di ricerca di neurotrasmissione dimostrano che (1) la liberazione del neurotrasmettitore stimolato è un processo dinamico che diminuisce nel tasso nel corso della stimolazione 14 , (2) rilascio continua nella fase poststimulazione con cinetica di decadimento bifasica 15 e (3) DA L'efficienza di ricupero viene inibito progressivamente durante la durata della stessa stimolazione 2 , 16 . Questi tre concetti fungono da fondamento del framework QN e le tre equazioni costituite da 12 parametri che descrivono le dinamiche di rilascio e reuptake DA ( tabella 1 ). Il quadro QN può simulare da vicino i tipi di risposta sperimentale eterogenei, nonché il pEffetti ridotti delle manipolazioni sperimentali di parametri di stimolazione e somministrazione di farmaci 2 , 6 . Sebbene sia necessaria un'ulteriore ricerca per perfezionare l'approccio di modellazione dei dati, i prossimi esperimenti possono trarre profitto da questo approccio di modellazione neurobiologicamente fondato, che aggiunge notevolmente le inferenze tratte dal paradigma stimolato DA di neurotrasmissione.

Tabella 1: Equazioni e parametri di modellazione . Clicca qui per visualizzare una versione più grande di questa figura.
Questo tutorial descrive come modellare i dati di risposta stimolati DA per stimare la rilascio di DA e ricompare la cinetica utilizzando QNsim 1.0. L'effettiva raccolta di dati sperimentali e prL'elaborazione non è descritta qui e richiede solo dati temporali di concentrazione DA. Il supporto teorico e le fondamenta del framework QN sono stati descritti in precedenza 2 , ma una prospettiva pratica sull'applicazione del framework QN per la modellazione dei dati di risposta DA è descritta di seguito.
Il framework QNM modella l'interazione dinamica tra: 1) rilascio dinamico DA, 2) reuptake DA, 3) effetti di stimoli suprafisiologici su questi processi per estrarre informazioni cinetiche significative dai dati di risposta DA. Il framework QN è più adatto per la modellazione di dati FSCV acquisiti utilizzando stimoli altamente suprafisiologici di lunga durata ( ad es., 60 Hz, 10 s stimolazioni), che producono robuste risposte DA che sono suscettibili di analisi cinetica. Seguendo la corretta modellizzazione dei processi di rilascio e di reuptake sottostante, i parametri del modello possono essere utilizzati per simulare una risposta DA che dovrebbe approssimare la forma dell'exRisposta perorale DA.
Le equazioni del quadro QN descrivono i tassi di rilascio e reuptake di DA nel corso delle risposte DA stimolate. Il quadro QN descrive la velocità di rilascio DA stimolata in funzione del tempo dall'inizio della stimolazione (t stim ), quando la velocità di rilascio DA diminuisce esponenzialmente nel corso dello stimolo. Ciò è coerente con l'esaurimento di una piscina prontamente rilasciata, con un tasso di rilascio aggiuntivo di DA (DARss) a rendere conto della ricostituzione della vescicola, simile ad altri rapporti (Equazione 2 ) 14 , 17 .
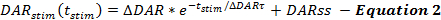
Le manipolazioni che aumentano il tasso di rilascio del DA, ad esempio aumentando ΔDAR, ΔDAR τ o DARss, portano ad aumentate ampiezze di risposta nei diagrammi DA rispetto a tempo. Ogni parameTer contribuisce in modo differenziato alle forme di risposta DA. Aumentando DARss e ΔDAR τ entrambi rendono la fase crescente di risposte più lineari (meno convessa). La diminuzione di ΔDAR τ promuove la convessità, controllata dalla grandezza di ΔDAR. Sulla base dell'esperienza di modellazione, DARss è generalmente inferiore a 1/5 di ΔDAR; Quindi, ΔDAR è il parametro di rilascio che determina principalmente l'ampiezza complessiva di risposta di una risposta DA.
La velocità di rilascio post-stimolazione DA è modellata dall'equazione 3 come una continuazione della velocità di rilascio DA stimolata dalla fine della stimolazione (DAR ES ) in funzione del tempo dopo la stimolazione (t post ). La velocità di rilascio DA dopo la stimolazione segue un modello di decadimento bifasico, come descritto in precedenza 15 , con una rapida fase di decadimento esponenziale e una prolungata fase di decadimento lineare per modellare due caProcessi di rilascio del neurotrasmettitore dipendente dal calcio.
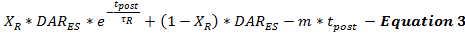
(Decadimento rapido esponenziale) (Decadimento lineare prolungato)
Attualmente non è possibile determinare la percentuale di rilascio post-stimolazione DA. Questa limitazione può essere affrontata riducendo sistematicamente le stime di rilascio DA poststimulazione e convalidando i parametri del modello attraverso un insieme di risposte DA sperimentali raccolte dallo stesso sito di registrazione utilizzando varie durate di stimolazione. Questa minimizzazione consente agli utenti di effettuare stime conservative di rilascio e riutilizzo. Poiché le stimolazioni elettriche conducono all'accumulo di calcio che promuove il rilascio del neurotrasmettitore post-stimolazione, la durata della stimolazione influenza i neurotrasci poststimulativiI parametri di rilascio del mittente 18 , 19 . Sulla base dell'esperienza di modellazione, si è scoperto che mentre aumenta la durata della stimolazione, τ aumenta e X R diminuisce, coerente con gli effetti previsti di un maggiore accumulo di calcio 20 .
L' equazione 4 descrive la frequenza di ricupero DA come estensione del quadro MM e incorpora un termine dinamico Km che aumenta durante la stimolazione per modellare un'efficienza di reuptake progressivamente diminuita causata dalle stimoli suprafisiologiche 2 , 16 . La stimolazione K m viene mantenuta costante al valore K m alla fine della stimolazione (K mES ).
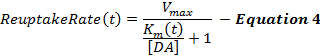
dove,
<img alt = "Equazione 6" src = "/ files / ftp_upload / 55595 / 55595eq6.jpg" />
(Durante la stimolazione) (dopo stimolazione)
Le risposte stimolate DA, in particolare dalle regioni striatali ventrali, spesso sono insensibili a variazioni del valore iniziale Km (K mi ), che rende problematica la definizione di un valore K mi . Così, come il quadro MM originale, K mi è approssimato a 0,1-0,4 μM per le risposte DA raccolte da animali di controllo non trattati 12 . Il termine Δ K m determina l'entità del cambiamento di efficienza di riutilizzo durante la stimolazione, che dalla nostra esperienza è di circa 2081; M nel corso di una stimolazione da 60 Hz, 10-s. I valori k e K minf determinano come Km cambia nel tempo e aumentando uno di questi termini promuove la concavità della fase crescente. V max è la frequenza massima di ricupero che in parte si riferisce alla densità locale del trasportatore DA, che presenta un gradiente ventromediale a dorsolaterale 21 . Di conseguenza, i valori V max nel striato dorsale (D-Str) sono generalmente superiori a 30 μM / s, ma generalmente inferiori a 30 μM / s nelle regioni ventrali, come il nucleo accumbens (NAc) 6 .
Le linee guida di cui sopra possono aiutare a modellare i dati sperimentali di risposta DA, ma generando una simulazione che si avvicina alla risposta sperimentale DA richiede una revisione iterativa dei parametri del modello. L'accuratezza dei parametri del modello può essere migliorata ottenendo risposta DA a stimoli suprafisiologici che fornisconoE un substrato robusto per la simulazione, nonché ottenendo e modellando molteplici risposte DA a stimoli di varia durate nello stesso luogo di registrazione ( ad esempio, stimoli da 60, 5 e 10) per convalidare l'accuratezza dei parametri ( Vedere i dati del campione). Per dimostrare, un set di dati è incluso con il pacchetto software contenente risposte DA regiospecificamente stimolate raccolte nel nucleus accumbens e nello striato dorsale, prima e dopo una sfida farmacologica già modellata utilizzando il framework QN. Per estensione, gli utenti troveranno che questa metodologia può essere applicata allo stesso modo per caratterizzare la cinetica della neurotrasmissione DA in vari contesti di malattia e manipolazioni farmacologiche.
Protocol
Representative Results
Discussion
L'uso di FSCV per studiare la neurotrasmissione DA stimolata in vivo in origine negli anni '80 e che continua ad essere una ricca fonte di dati in vivo di neurotrasmissione con risoluzione senza precedenti spaziali e temporali. Le risposte stimolate DA riflettono un equilibrio complesso di rilascio e reuptake DA che sono modulati dalle stesse stimolazioni elettriche. Il modello QN incorpora i principi della ricerca di neurotrasmissione contemporanea per modellare in vivo i dati di neur…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Riconosciamo l'Istituto di Riabilitazione UPMC per sostenere questo lavoro.
Materials
| MATLAB R2016a for Mac | Mathworks | ||
| QNsim1.0 | In house software package | Software to model FSCV data using the QN framework |
References
- Taylor, I. M., et al. Kinetic diversity of dopamine transmission in the dorsal striatum. J Neurochem. 133 (4), 522-531 (2015).
- Harun, R., Grassi, C. M., Munoz, M. J., Torres, G. E., Wagner, A. K. Neurobiological model of stimulated dopamine neurotransmission to interpret fast-scan cyclic voltammetry data. Brain Res. 1599, 67-84 (2015).
- Taylor, I. M., Jaquins-Gerstl, A., Sesack, S. R., Michael, A. C. Domain-dependent effects of DAT inhibition in the rat dorsal striatum. Journal of neurochemistry. 122 (2), 283-294 (2012).
- Garris, P. A., Ciolkowski, E. L., Wightman, R. M. Heterogeneity of evoked dopamine overflow within the striatal and striatoamygdaloid regions. 神经科学. 59 (2), 417-427 (1994).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain Res. 487 (2), 311-320 (1989).
- Harun, R., et al. Fast-scan cyclic voltammetry demonstrates that L-DOPA produces dose-dependent regionally selective, bimodal effects on striatal dopamine kinetics in vivo. J Neurochem. , (2015).
- Jones, S. R., Garris, P. A., Wightman, R. M. Different effects of cocaine and nomifensine on dopamine uptake in the caudate-putamen and nucleus accumbens. The Journal of pharmacology and experimental therapeutics. 274 (1), 396-403 (1995).
- Budygin, E. A., John, C. E., Mateo, Y., Jones, S. R. Lack of cocaine effect on dopamine clearance in the core and shell of the nucleus accumbens of dopamine transporter knock-out mice. J Neurosci. 22 (10), RC222 (2002).
- Jones, S. R., et al. Loss of autoreceptor functions in mice lacking the dopamine transporter. Nat Neurosci. 2 (7), 649-655 (1999).
- Wagner, A. K., et al. Chronic methylphenidate treatment enhances striatal dopamine neurotransmission after experimental traumatic brain injury. J Neurochem. 108 (4), 986-997 (2009).
- Wagner, A. K., et al. Controlled cortical impact injury influences methylphenidate-induced changes in striatal dopamine neurotransmission. J Neurochem. 110 (3), 801-810 (2009).
- Wightman, R. M., et al. Real-time characterization of dopamine overflow and uptake in the rat striatum. 神经科学. 25 (2), 513-523 (1988).
- Moquin, K. F., Michael, A. C. Tonic autoinhibition contributes to the heterogeneity of evoked dopamine release in the rat striatum. J Neurochem. 110 (5), 1491-1501 (2009).
- Pyott, S. J., Rosenmund, C. The effects of temperature on vesicular supply and release in autaptic cultures of rat and mouse hippocampal neurons. J Physiol. 539 (Pt 2), 523-535 (2002).
- Atluri, P. P., Regehr, W. G. Delayed release of neurotransmitter from cerebellar granule cells. J Neurosci. 18 (20), 8214-8227 (1998).
- Wang, S. R., et al. Role of vesicle pools in action potential pattern-dependent dopamine overflow in rat striatum in vivo. J Neurochem. 119 (2), 342-353 (2011).
- Taschenberger, H., von Gersdorff, H. Fine-tuning an auditory synapse for speed and fidelity: developmental changes in presynaptic waveform, EPSC kinetics, and synaptic plasticity. J Neurosci. 20 (24), 9162-9173 (2000).
- Goda, Y., Stevens, C. F. Two components of transmitter release at a central synapse. Proc Nat Acad of Sci U S A. 91 (26), 12942-12946 (1994).
- Yao, J., Gaffaney, J. D., Kwon, S. E., Chapman, E. R. Doc2 is a Ca2+ sensor required for asynchronous neurotransmitter release. Cell. 147 (3), 666-677 (2011).
- Hagler, D. J., Goda, Y. Properties of synchronous and asynchronous release during pulse train depression in cultured hippocampal neurons. J Neurophysiol. 85 (6), 2324-2334 (2001).
- Ciliax, B. J., et al. The dopamine transporter: immunochemical characterization and localization in brain. J Neurosci. 15 (3 Pt 1), 1714-1723 (1995).
- Volz, T. J., Farnsworth, S. J., Rowley, S. D., Hanson, G. R., Fleckenstein, A. E. Methylphenidate-induced increases in vesicular dopamine sequestration and dopamine release in the striatum: the role of muscarinic and dopamine D2 receptors. J Pharm Exp Ther. 327 (1), 161-167 (2008).
- Dresel, S. H., Kung, M. P., Plossl, K., Meegalla, S. K., Kung, H. F. Pharmacological effects of dopaminergic drugs on in vivo binding of [99mTc]TRODAT-1 to the central dopamine transporters in rats. Eur J Nucl Med. 25 (1), 31-39 (1998).
- Near, J. A., Bigelow, J. C., Wightman, R. M. Comparison of uptake of dopamine in rat striatal chopped tissue and synaptosomes. J Pharm Exp Ther. 245 (3), 921-927 (1988).
- Michael, A. C., Ikeda, M., Justice, J. B. Dynamics of the recovery of releasable dopamine following electrical stimulation of the medial forebrain bundle. Neurosci Lett. 76 (1), 81-86 (1987).
- Fierro, L., DiPolo, R., Llano, I. Intracellular calcium clearance in Purkinje cell somata from rat cerebellar slices. The Journal of physiology. 510 (Pt 2), 499-512 (1998).
- Sandoval, V., Riddle, E. L., Hanson, G. R., Fleckenstein, A. E. Methylphenidate redistributes vesicular monoamine transporter-2: role of dopamine receptors. J Neurosci. 22 (19), 8705-8710 (2002).
- Daws, L. C., et al. Cocaine increases dopamine uptake and cell surface expression of dopamine transporters. Biochem Biophys Res Commun. 290 (5), 1545-1550 (2002).
- Little, K. Y., Kirkman, J. A., Carroll, F. I., Clark, T. B., Duncan, G. E. Cocaine use increases [3H]WIN 35428 binding sites in human striatum. Brain Res. 628 (1-2), 17-25 (1993).
- Ewing, A. G., Bigelow, J. C., Wightman, R. M. Direct in vivo monitoring of dopamine released from two striatal compartments in the rat. Science. 221 (4606), 169-171 (1983).
- Janezic, S., et al. Deficits in dopaminergic transmission precede neuron loss and dysfunction in a new Parkinson model. Proc Natl Acad Sci U S A. 110 (42), E4016-E4025 (2013).
- Macdonald, P. A., Monchi, O. Differential effects of dopaminergic therapies on dorsal and ventral striatum in Parkinson’s disease: implications for cognitive function. Parkinsons Dis. 2011, 572743 (2011).
- Kile, B. M., et al. Optimizing the Temporal Resolution of Fast-Scan Cyclic Voltammetry. ACS Chem Neurosci. 3 (4), 285-292 (2012).
- Venton, B. J., Troyer, K. P., Wightman, R. M. Response times of carbon fiber microelectrodes to dynamic changes in catecholamine concentration. Anal Chem. 74 (3), 539-546 (2002).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain research. 487 (2), 311-320 (1989).
- Wu, Q., Reith, M. E., Wightman, R. M., Kawagoe, K. T., Garris, P. A. Determination of release and uptake parameters from electrically evoked dopamine dynamics measured by real-time voltammetry. J Neurosci Methods. 112 (2), 119-133 (2001).

