De Fluorescence Imaging rapide à moléculaire loi Diffusion sur les membranes cellulaires en direct dans un microscope commercial
Summary
Spatial distribution and temporal dynamics of plasma membrane proteins and lipids is a hot topic in biology. Here this issue is addressed by a spatio-temporal image fluctuation analysis that provides conceptually the same physical quantities of single particle tracking, but it uses small molecular labels and standard microscopy setups.
Abstract
Il est devenu de plus en plus évident que la distribution spatiale et le mouvement des composants de la membrane comme les lipides et les protéines sont des facteurs clés dans la régulation de nombreuses fonctions cellulaires. Toutefois, en raison de la dynamique rapide et les petites structures impliquées, une résolution spatio-temporelle très élevée est nécessaire pour rattraper le comportement réel de molécules. Ici, nous présentons le protocole expérimental pour l'étude de la dynamique des protéines et des lipides du plasma membrane marquées par fluorescence dans des cellules vivantes avec une résolution spatio-temporelle élevée. En particulier, cette approche n'a pas besoin de suivre chaque molécule, mais il calcule le comportement de la population en utilisant les molécules d'une région donnée de la membrane. Le point de départ est une imagerie rapide d'une région donnée sur la membrane. Ensuite, une fonction spatio-temporelle complète autocorrélation est calculée en corrélation des images acquises à l'augmentation des retards de temps, par exemple tous les 2, 3, n répétitions. Il est possible de démontrer que la largeurdu pic de la fonction d'autocorrélation spatiale augmente en augmentant le temps de retard en fonction du mouvement des particules par diffusion. Par conséquent, le montage de la série de fonctions d'auto-corrélation permet d'extraire la protéine réelle signifie déplacement quadratique de l'imagerie (DSGI), présenté ici sous la forme de la diffusivité apparente vs déplacement moyen. Cela donne une vision quantitative de la dynamique moyenne des molécules simples avec une précision nanométrique. En utilisant une variante de la GFP étiqueté du récepteur de la transferrine (TfR) et un ATTO488 1-palmitoyl-2-hydroxy-sn -glycéro-3-phosphoéthanolamine (PPE), il est possible d'observer la régulation spatio-temporelle des protéines et des lipides diffusion sur régions membranaires um de taille dans la gamme micro-à-milli-seconde fois.
Introduction
À partir du modèle original "de la mosaïque fluide» par Singer et Nicolson, l'image de la membrane plasmique cellulaire a été continuellement mis à jour au cours des dernières décennies afin d'inclure le nouveau rôle de cytosquelette et de lipides domaines 1,2.
Les premières observations ont été obtenues par récupération de fluorescence après photoblanchiment (FRAP) dévoilement qu'une fraction significative des protéines de la membrane est immobile 5.3. Ces études pionnières, bien que très instructif, ont souffert de la résolution relativement faible dans l'espace (microns) et de temps (en secondes) de configurations du PAF. En outre, étant une mesure de la moyenne d'ensemble, FRAP manque en donnant des informations sur le comportement de la molécule unique.
Dans ce contexte, la possibilité d'étiqueter spécifiquement une molécule unique avec des balises très claires (permettant l'étude du processus de diffusion d'une molécule à la fois) a été très réussie. En particulier, en poussant l'résolution temporelle de l'approche unique de suivi de particules (SPT) à l'échelle de temps de microsecondes, Kusumi, et al. pu accéder aux fonctions inconnues de lipides et de protéines dynamique qui a grandement contribué à la reconnaissance du rôle de base de l'actine-membrane squelette dans la membrane physiologie 6 , 7. Ces résultats ont généré le soi-disant le «piquetage et de clôture» modèle, dans lequel lipides et des protéines diffusion est régie par squelette d'actine. Toutefois, afin d'avoir accès à l'énorme quantité d'informations fournies par SPT nombreuses questions expérimentales doivent être pris en compte. En particulier, la procédure de marquage est typiquement constituée par de nombreuses étapes telles que la production, la purification et l'introduction de l'espèce marquée dans le système. En outre, de grandes étiquettes, comme des boîtes quantiques ou des nanoparticules métalliques, sont souvent nécessaires pour parvenir à l'échelle de temps inférieure à la milliseconde et de la réticulation des molécules cibles par l'étiquette ne peut être évitée dans la plupart des cas. Enfin, de nombreuses trajectoiresdoivent être enregistrés pour s'adapter à des critères statistiques et de façon concomitante une faible densité de l'étiquette est nécessaire pour permettre le suivi.
Par rapport à SPT, la spectroscopie de corrélation de fluorescence (FCS), surmonter un grand nombre de ces inconvénients, représente une approche très prometteuse pour étudier la dynamique moléculaire. En fait, FCS fonctionne bien également avec des étiquettes sombres et denses, ce qui permet d'étudier la dynamique des molécules de protéines étiquetées fluorescentes dans les cellules transfectées de façon transitoire. En outre, il permet d'atteindre des statistiques élevées dans un laps de temps limité. Enfin, malgré la densité «élevé» d'étiquettes FCS fournit des informations sur les molécules simples. Merci à toutes ces propriétés, FCS représente une approche très simple et a été largement appliquées à l'étude de lipides et de protéines dynamique à la fois dans des membranes modèles et dans les cellules vivantes 8-10. De nombreuses approches différentes ont été proposées pour augmenter la capacité de FCS pour révéler les détails de la diffusion moléculaire. Par exemple, il est shpropre que par l'exécution FCS sur les zones d'observation de taille différente, on peut définir un "droit de diffusion FCS" caractéristiques éclairantes cachés de mouvement moléculaire 11,12. En plus d'être varié en taille, le domaine d'intervention a également été dupliqué 13, déplacé dans l'espace le long des lignes 14-20 ou conjugués avec des caméras rapides 21,22. L'utilisation de ces corrélation «spatio-temporelle» les approches, les paramètres biologiques pertinents de plusieurs composants membranaires ont été décrits quantitativement sur les deux membranes modèles et les systèmes biologiques réels, ainsi aperçu rendement dans la membrane organisation spatiale.
Cependant, dans tous les FRAP et applications FCS décrit jusqu'à présent la taille de la zone de convergence représente une limite de la résolution spatiale qui ne peut être surmontée. Plusieurs méthodes d'imagerie de super-résolution ont été développés récemment pour contourner cette limite. Certains sont basés sur la précision de localisation, telles que la microscopie optique de reconstruction stochastique (STORM) <sup> 23,24, microscopie photo-activation de la localisation (PALM) 25, fluorescence PALM (FPALM) 26, et une particule suivi PALM (sptPALM) 27: la quantité relativement importante de photons nécessaires à chaque cliché, cependant, limite la résolution temporelle de ces méthodes à au moins quelques millisecondes, ce qui entrave leur applicabilité in vivo.
En revanche, une alternative prometteuse pour l'imagerie de super résolution ont été ouverts en modulant spatialement l'émission de fluorescence avec des procédés d'épuisement émission stimulés (STED ou transitions réversibles saturables optique de fluorescence (RESOLFT) 28,29). Ces approches se combinent la mise en forme du volume d'observation et au-dessous de la limite de diffraction, avec la possibilité d'utiliser des microscopes à balayage rapide et des systèmes de détection. En combinaison avec l'analyse de fluctuation de fluorescence, la microscopie STED a permis de sonder directement les dynamiques spatio-temporelles à l'échelle nanométrique de lipides et de proteins dans les membranes des cellules vivantes 30,31.
Les mêmes quantités physiques de base de la microscopie STED peuvent être obtenus par une spectroscopie de corrélation de l'image spatio-temporel modifié (TIQUES 32,33) procédé qui est approprié pour l'étude de la dynamique des protéines marquées par fluorescence de membrane et / ou des lipides dans les cellules vivantes et par un microscope commercial. Le protocole expérimental présenté ici se compose de quelques étapes. La première nécessite une imagerie rapide de la région d'intérêt sur la membrane. Ensuite, la pile résultante d'images est utilisée pour calculer les fonctions de corrélation spatio-temporelle moyenne. En adaptant la série de fonctions de corrélation, la «loi de diffusion» moléculaire peut être obtenu directement à partir de l'imagerie sous la forme d'une diffusivité apparente (D app) – vs tracé du déplacement -Moyenne. Cette parcelle est fortement tributaire de l'environnement exploré par les molécules et permet de reconnaître directement les modes de diffusion réelsdu lipide / protéine d'intérêt.
Dans plus de détails, comme indiqué précédemment 34, la fonction d'auto-corrélation spatio-temporelle de la série d'images acquises dépend essentiellement de la dynamique des molécules en mouvement dans la série d'images recueillies (s'il vous plaît noter que le même raisonnement peut être appliqué à l'acquisition d'une ligne où seulement une dimension dans l'espace est pris en compte). En particulier, nous définissons la fonction de corrélation:
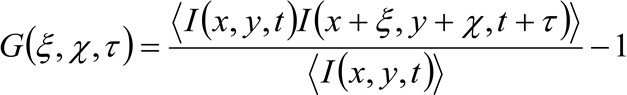 (1)
(1)
où 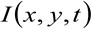 représente l'intensité de fluorescence mesurée à la position x, y et à l'instant t,
représente l'intensité de fluorescence mesurée à la position x, y et à l'instant t, ![]() et
et ![]() représente la distance dans le plan x etdirections y respectivement,
représente la distance dans le plan x etdirections y respectivement, ![]() représente le décalage dans le temps, et
représente le décalage dans le temps, et ![]() représente la moyenne. Cette fonction peut être exprimée comme suit:
représente la moyenne. Cette fonction peut être exprimée comme suit:
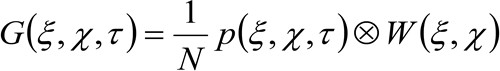 (2)
(2)
où «N» représente le nombre moyen de molécules dans la zone d'observation, ![]() représente l'opération de convolution dans l'espace, et
représente l'opération de convolution dans l'espace, et 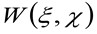 représente l'auto-corrélation de la taille instrumentale. Ce dernier peut être interprété comme une mesure de la façon dont les photons d'un seul émetteur sont répartis dans l'espace en raison de la configuration optique / enregistrement (ce qu'on appelle le Point Spread Function, PSF, gèneRALLYE bien approchée par une fonction gaussienne). Enfin,
représente l'auto-corrélation de la taille instrumentale. Ce dernier peut être interprété comme une mesure de la façon dont les photons d'un seul émetteur sont répartis dans l'espace en raison de la configuration optique / enregistrement (ce qu'on appelle le Point Spread Function, PSF, gèneRALLYE bien approchée par une fonction gaussienne). Enfin, 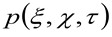 représente la probabilité de trouver une particule à une distance
représente la probabilité de trouver une particule à une distance ![]() et
et ![]() après un temps de retard
après un temps de retard ![]() . Si l'on considère une dynamique de diffusion, dans laquelle les particules se déplacent au hasard dans toutes les directions et les flux nets ne sont pas présents, cette fonction est également bien approchée par une fonction gaussienne où la variance peut être identifié comme le déplacement quadratique moyen (MSD) de la particule en mouvement . Ainsi, la taille de la fonction de corrélation (également désigné en tant que
. Si l'on considère une dynamique de diffusion, dans laquelle les particules se déplacent au hasard dans toutes les directions et les flux nets ne sont pas présents, cette fonction est également bien approchée par une fonction gaussienne où la variance peut être identifié comme le déplacement quadratique moyen (MSD) de la particule en mouvement . Ainsi, la taille de la fonction de corrélation (également désigné en tant que ![]() ), Peut être définie comme la somme des TMS de particules et la taille instrumental et peut être mesurée par un ajustement gaussiention de la fonction de corrélation pour chaque temps de retard. Le TMS i mesurée peut être utilisée pour calculer une diffusivité apparente des molécules qui se déplacent
), Peut être définie comme la somme des TMS de particules et la taille instrumental et peut être mesurée par un ajustement gaussiention de la fonction de corrélation pour chaque temps de retard. Le TMS i mesurée peut être utilisée pour calculer une diffusivité apparente des molécules qui se déplacent ![]() et un moyen de déplacement
et un moyen de déplacement ![]() en tant que:
en tant que:
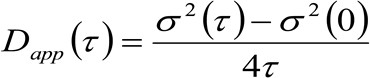 (3)
(3)
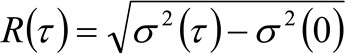 (4)
(4)
Quelques considérations sur le dispositif expérimental utilisé peut guider le lecteur à travers les sections suivantes. Pour exciter sélectivement les fluorophores sur la membrane basale des cellules, nous allons utiliser un éclairage réflexion totale interne (TIR) vivant, en utilisant une fluorescence TIR commerciale (FRBR) microscope (détails peuvent être trouvés dans la section matériel). En outre, afin de recueillir èmee fluorescence, nous allons utiliser un objectif de grossissement (100X NA 1,47, ouverture numérique élevée est nécessaire pour la FRBR éclairage) et une caméra EMCCD (taille physique du pixel sur la puce um 16). Pour atteindre une taille de pixel de 100 nm, nous appliquons une lentille de grossissement supplémentaire de 1.6X. Comme nous le verrons, une résolution temporelle inférieure à 1 ms serait nécessaire pour décrire correctement la dynamique des lipides membranaires rapides en dessous de 100 nm. Afin d'atteindre cette résolution temporelle nous devons sélectionner une région d'intérêt (ROI) plus petit que l'ensemble puce de l'appareil photo (512 x 512). De cette façon, la caméra va lire un nombre réduit de lignes de plus en plus la résolution temporelle. Toutefois, dans ce régime de lecture du temps de trame serait limitée par le temps nécessaire pour transférer les charges de l'exposition à la puce de lecture sur l'appareil et est généralement de l'ordre de 512 millisecondes pour x 512 pixels EMCCD. Pour battre cette limite, une technologie émergente permet le déplacement des ROI lignes seulement au lieu de toute la trame, wvec une réduction effective pratique de la taille de la puce exposée (appelé mode du capteur recadrée dans notre EMCCD). Pour cette configuration, pour être efficace, la puce à l'extérieur de la région d'intérêt doit être couverte par un couple de fentes montées dans le chemin optique. Merci pour cette configuration une résolution de temps d'arrêt à 10 -4 secondes peut être obtenue. S'il vous plaît noter, cependant, que cette approche peut être couplé avec différents montages expérimentaux, comme expliqué dans la section «discussion».
Démonstration de la méthode sera fourni dans les cellules vivantes, en utilisant à la fois un ATTO488 1-palmitoyl-2-hydroxy-sn–glycéro 3-phosphoéthanolamine (ATTO488-EPI) et un variant de la GFP-marqué de récepteur de la transferrine (GFP TfR). Dans le cas de ATTO488 EPI cette approche peut réussir à récupérer une application presque constante de D en fonction de déplacement moyenne indiquant une diffusion pour la plupart gratuites, comme indiqué précédemment 30,35. En revanche, l'ISF-GFP montre une diminution D <sub> application en fonction du déplacement moyen, suggérant diffusion partiellement confinée 6. En outre, dans ce dernier cas, il est possible de quantifier la constante de diffusion locale et la région de confinement moyenne sur plusieurs microns sur le plan de la membrane.
Protocol
Representative Results
Discussion
Suivi de particules unique (SPT) représente l'une des stratégies les plus courantes pour étudier la dynamique moléculaire et il a le grand avantage de mesurer les trajectoires des particules. Cela permet à son tour le comportement de palpage de même quelques particules marquées dans un système complexe. Toutefois, pour atteindre cet avantage SPT a généralement besoin d'une faible densité de la sonde et des étiquettes très brillantes. En particulier, pour obtenir haute résolution temporelle (plage d…
Divulgations
The authors have nothing to disclose.
Acknowledgements
This work is supported in part by NIH-P41 P41-RRO3155 and NIH P50-GM076516 (grant to EG), and Fondazione Monte dei Paschi di Siena (grant to FB).
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| iXon Ultra 897 | Andor | DU-897U-CS0 | |
| Solis | Andor | ||
| CHO-K1 | ATCC | CCL-61 | |
| ATTO 488 labeled PPE | ATTO-TEC GmbH | AD 488-151 | |
| DOPE | Avanti Polar Lipids, Inc. | 850725 | |
| DOTAP | Avanti Polar Lipids, Inc. | 890890 | |
| 100X Penicillin-Streptomycin-Glutamine | Gibco | 10378-016 | |
| DMEM/F-12 | Gibco | 21331 | |
| FBS | Gibco | 10082147 | |
| HEPES | Gibco | 15630-106 | |
| PBS | Gibco | 10010-023 | |
| SimFCS 3.0 | Globals Software | the software can be downloaded here: http://www.lfd.uci.edu/globals/ | |
| DMI6000 with TIRF modulus | Leica | ||
| LAS AF | Leica | ||
| Lipofectamine 2000 | Lipofectamine | 11668019 | |
| Matlab | MathWork | ||
| Imagej | NIH | ||
| C-terminal GFP tagged Tranferrin Receptor | OriGene | RG200980 | |
| Agar | Sigma Aldrich | A5306 | |
| Chloroform | Sigma Aldrich | 528730 | |
| Latex beads, fluorescent yellow-green, 30 nm | Sigma Aldrich | L5155 | |
| SONICA Ultrasonic Cleaners | SOLTEC | ETH S3 | |
| Petri Dishes | Willco | GWSt-3522 | |
| Bio-Format importer for Matlab | http://www.openmicroscopy.org/site/support/bio-formats5/users/matlab/ | ||
| ICS-MatLab Tools | https://www.cellmigration.org/resource/imaging/software/ICSMATLAB_28-02-06.zip | ||
| Simulation by Matlab Tutorial | https://www.cellmigration.org/resource/imaging/icsmatlab/ICSTutorial.html | ||
| Simulation by SimFCS Tutorial | https://www.cellmigration.org/resource/imaging/ppt-pdf/RICS%20Simulations.ppt |
References
- Engelman, D. M. Membranes are more mosaic than fluid. Nature. 438 (7068), 578-580 (2005).
- Vereb, G., et al. yet structured: The cell membrane three decades after the Singer-Nicolson model. Proc. Natl. Acad. Sci. U. S. A. 100 (14), 8053-8058 (1073).
- Ishihara, A., Hou, Y., Jacobson, K. The Thy-1 antigen exhibits rapid lateral diffusion in the plasma membrane of rodent lymphoid cells and fibroblasts. 84 (5), 1290-1293 (1987).
- Axelrod, D., et al. Lateral motion of fluorescently labeled acetylcholine receptors in membranes of developing muscle fibers. Proc. Natl. Acad. Sci. U. S. A. 73 (12), 4594-4598 (1976).
- Jacobson, K., Derzko, Z., Wu, E. S., Hou, Y., Poste, G. Measurement of the lateral mobility of cell surface components in single, living cells by fluorescence recovery after photobleaching. J. Supramol. Struct. 5 (4), 10-1002 (1976).
- Kusumi, A., et al. Paradigm shift of the plasma membrane concept from the two-dimensional continuum fluid to the partitioned fluid: high-speed single-molecule tracking of membrane molecules. Annu. Rev. Biophys. Biomol. Struct. 34, 351-378 (2005).
- Kusumi, A., Ike, H., Nakada, C., Murase, K., Fujiwara, T. Single-molecule tracking of membrane molecules: plasma membrane compartmentalization and dynamic assembly of raft-philic signaling molecules. Semin. Immunol. 17 (1), 3-21 (2005).
- Schwille, P., Korlach, J., Webb, W. W. Fluorescence correlation spectroscopy with single-molecule sensitivity on cell and model membranes. Cytometry. 36, 176-182 (1999).
- Gielen, E., et al. Diffusion of sphingomyelin and myelin oligodendrocyte glycoprotein in the membrane of OLN-93 oligodendroglial cells studied by fluorescence correlation spectroscopy. C. R. Biol. 328 (12), 1057-1064 (2005).
- Weiss, M., Hashimoto, H., Nilsson, T. Anomalous protein diffusion in living cells as seen by fluorescence correlation spectroscopy. Biophys. J. 84, 4043-4052 (2003).
- Wawrezinieck, L., Rigneault, H., Marguet, D., Lenne, P. F. Fluorescence correlation spectroscopy diffusion laws to probe the submicron cell membrane organization. Biophys. J. 89 (6), 4029-4042 (2005).
- Lenne, P. F., et al. Dynamic molecular confinement in the plasma membrane by microdomains and the cytoskeleton meshwork. EMBO J. 25 (14), 3245-3256 (2006).
- Ries, J., Schwille, P. Studying slow membrane dynamics with continuous wave scanning fluorescence correlation spectroscopy. Biophys. J. 91 (5), 1915-1924 (2006).
- Ruan, Q., Cheng, M. A., Levi, M., Gratton, E., Mantulin, W. W. Spatial-temporal studies of membrane dynamics: scanning fluorescence correlation spectroscopy (SFCS). Biophys. J. 87 (2), 1260-1267 (2004).
- Berland, K. M., So, P. T., Chen, Y., Mantulin, W. W., Gratton, E. Scanning two-photon fluctuation correlation spectroscopy: particle counting measurements for detection of molecular aggregation. Biophys. J. 71, 410-420 (1996).
- Heinemann, F., Betaneli, V., Thomas, F. A., Schwille, P. Quantifying lipid diffusion by fluorescence correlation spectroscopy: a critical treatise. Langmuir. 28 (37), 13395-13404 (2012).
- Cardarelli, F., Lanzano, L., Gratton, E. Capturing directed molecular motion in the nuclear pore complex of live cells. Proc. Natl. Acad. Sci. U. S. A. 109 (25), 9863-9868 (2012).
- Sanchez, S. A., Tricerri, M. A., Gratton, E. Laurdan generalized polarization fluctuations measures membrane packing micro-heterogeneity in vivo. Proc. Natl. Acad. Sci. U. S. A. 109 (19), 7314-7319 (2012).
- Cardarelli, F., Lanzano, L., Gratton, E. Fluorescence correlation spectroscopy of intact nuclear pore complexes. Biophys. J. 101 (4), 27-29 (2012).
- Di Rienzo, C., et al. Unveiling LOX-1 receptor interplay with nanotopography: mechanotransduction and atherosclerosis onset. Sci. Rep. 3, 10-1038 (2013).
- Unruh, J. R., Gratton, E. Analysis of molecular concentration and brightness from fluorescence fluctuation data with an electron multiplied CCD camera. Biophys. J. 95 (11), 5385-5398 (2008).
- Kannan, B., et al. Electron multiplying charge-coupled device camera based fluorescence correlation spectroscopy. Anal. Chem. 78 (10), 3444-3451 (2006).
- Jones, S. A., Shim, S. H., He, J., Fast Zhuang, X. three-dimensional super-resolution imaging of live cells. Nat. Methods. 8 (6), 499-508 (2011).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy. 3 (10), 793-795 (2006).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313 (5793), 1642-1645 (2006).
- Hess, S. T., Girirajan, T. P., Mason, M. D. Ultra-high resolution imaging by fluorescence photoactivation localization microscopy. Biophys. J. 91 (11), 4258-4272 (2006).
- Manley, S., et al. High-density mapping of single-molecule trajectories with photoactivated localization microscopy. Nat. Methods. 5 (2), 155-157 (2008).
- Hell, S. W. Far-field optical nanoscopy. Science. 316 (5828), 1153-1158 (2007).
- Klar, T. A., Hell, S. W. Subdiffraction resolution in far-field fluorescence microscopy. Opt. Lett. 24 (14), 954-956 (1999).
- Eggeling, C., et al. Direct observation of the nanoscale dynamics of membrane lipids in a living cell. Nature. 457 (7233), 1159-1162 (2009).
- Hedde, P. N., et al. Stimulated emission depletion-based raster image correlation spectroscopy reveals biomolecular dynamics in live cells. Nat. Commun. 4, .
- Hebert, B., Costantino, S., Wiseman, P. W. Spatiotemporal image correlation spectroscopy (STICS) theory, verification, and application to protein velocity mapping in living CHO cells. Biophys. J. 88 (5), 3601-3614 (2005).
- Brown, C. M., et al. Probing the integrin-actin linkage using high-resolution protein velocity mapping. J. Cell Sci. 119, 5204-5214 (2006).
- Di Rienzo, C., Gratton, E., Beltram, F., Cardarelli, F. Fast spatiotemporal correlation spectroscopy to determine protein lateral diffusion laws in live cell membranes. Proc. Natl. Acad. Sci. U. S. A. 110 (30), 12307-12312 (2013).
- Mueller, V., et al. STED nanoscopy reveals molecular details of cholesterol- and cytoskeleton-modulated lipid interactions in living cells. Biophys. J. 101 (7), 1651-1660 (2011).
- Kleusch, C., Hersch, N., Hoffmann, B., Merkel, R., Csiszar, A. Fluorescent lipids: functional parts of fusogenic liposomes and tools for cell membrane labeling and visualization. Molecules. 17 (1), 1055-1073 (2012).
- Ries, J., Chiantia, S., Schwille, P. Accurate determination of membrane dynamics with line-scan FCS. Biophys. J. 96 (5), 1999-2008 (2009).
- Kolin, D. L., Wiseman, P. W. Advances in image correlation spectroscopy: measuring number densities, aggregation states, and dynamics of fluorescently labeled macromolecules in cells. Cell Biochem. Biophys. 49 (3), 141-164 (2007).
- Digman, M. A., et al. Measuring fast dynamics in solutions and cells with a laser scanning microscope. Biophys. J. 89 (2), 1317-1327 (2005).
- Ritchie, K., et al. Detection of non-Brownian diffusion in the cell membrane in single molecule tracking. Biophys. J. 88 (3), 2266-2277 (2005).
- Voie, A. H., Burns, D. H., Spelman, F. A. Orthogonal-plane fluorescence optical sectioning: three-dimensional imaging of macroscopic biological specimens. J. Microsc. 170, 229-236 (1993).
- Huisken, J., Swoger, J., Del Bene, ., Wittbrodt, F., J, E. H., Stelzer, Optical sectioning deep inside live embryos by selective plane illumination microscopy. Science. 305 (5686), 1007-1009 (2004).
- Wohland, T., Shi, X., Sankaran, J., Stelzer, E. H. Single plane illumination fluorescence correlation spectroscopy (SPIM-FCS) probes inhomogeneous three-dimensional environments. Opt. Express. 18 (10), 10627-10641 (2010).

