Nişaste Granül Boyutu Dağılımlarının Analizi ve Spesifikasyonu
Summary
Burada nişasta granül boyutu dağılımlarının tekrarlanabilir ve istatistiksel olarak geçerli tayinleri ve iki parametreli multiplicative form kullanılarak belirlenen granül lognormal boyut dağılımlarının belirtilmesi için bir prosedür sunulmaktadır. Bitki ve gıda bilimi araştırmaları için gram ölçekli nişasta örneklerinin tüm granül boyutlandırma analizleri için geçerlidir.
Abstract
Tüm bitki kaynaklarından nişasta, farklı oluşum frekanslarına sahip, yani bir boyut ve şekil dağılımı sergileyen çeşitli boyut ve şekillerde granüllerdenoluşur. Çeşitli parçacık boyutlandırma teknikleri kullanılarak belirlenen nişasta granül boyutu verileri, granül şekillerine duyarlılık ve granül örnek boyutlarının sınırları da dahil olmak üzere bazı aşılmaz sistematik hatalardan kaynaklanan zayıf tekrarlanabilirlik veya istatistiksel önemin olmaması nedeniyle genellikle sorunludur. Elektrik algılama bölgesi tekniğini kullanarak nişasta granül boyutu dağılımlarının tekrarlanabilir ve istatistiksel olarak geçerli tayinleri ve gelişmiş doğruluk ve karşılaştırılılabilirlik ile benimsenmiş iki parametreli multiplicative form kullanarak belirlenen granül lognormal boyut dağılımlarını belirtmek için bir prosedür özetledik. Gram ölçekli nişasta örneklerinin tüm granül boyutlandırma analizleri için geçerlidir ve bu nedenle nişasta granül boyutlarının nişasta biyosentez aparatı ve mekanizmaları tarafından nasıl kalıplandırıldığı ile ilgili çalışmaları kolaylaştırabilir; ve gıda ve endüstriyel kullanımlar için nişasdaların özelliklerini ve işlevselliğini nasıl etkilediklerini. Temsili sonuçlar, özetlenen prosedür kullanılarak sweetpotato nişaste örneklerinin granül boyutu dağılımlarının çoğaltılması analizlerinden sunulur. Ayrıca, prosedürün birkaç temel teknik yönünü, özellikle granül lognormal boyut dağılımlarının multiplicative spesifikasyonunu ve granül agregaları ile sık diyafram tıkanıklığı aşmak için bazı teknik araçları tartıştık.
Introduction
Nişasta granülleri, bitki fotosentez ve saklama dokularındaki iki ana rezerv homoglucan polimerinin, doğrusal veya seyrek dallı amilozun ve yüksek dallı amilektin, lipitler ve proteinler de dahil olmak üzere bazı küçük bileşenlerle birlikte düzenli olarak paket edildiği fiziksel yapıdır. Çeşitli bitki türlerinden nişasta granülleri küreler, elipsoidler, polihedronlar, trombositler, küpler, küboidler ve düzensiz tübüller dahil olmak üzere birçok üç boyutlu (3D) şekiller(ref.1,2’deincelenmiştir) sergiler. Aynı dokudan veya aynı bitki türünün farklı dokularından gelenler bile, değişen oluşum frekanslarına sahip bir dizi şekle sahip olabilir. Başka bir deyişle, bir bitki türünden gelen nişasta granülleri, belirli bir şekil yerine karakteristik bir istatistiksel şekil dağılımına sahip olabilir. Homojen olmayan ve küresel olmayan granül şekilleri, nişasta granül boyutlarının düzgün bir şekilde ölçülmesi ve tanımlanmasını zorlaştırır. Ek olarak, bir bitki türünün aynı dokularından gelen nişasta granülleri, farklı oranlarda, yani karakteristik bir boyut dağılımı sergileyen çeşitli boyutlardadır. Bu boyut dağılımı, nişaste granül boyutlarının analizini ve açıklamasını daha da karmaşık hale gelir.
Nişasta granül boyutları, mikroskopi, sedimansasyon/sterik alan akışı fraksiyonasyonu (Sd/StFFF), lazer kırınım ve elektrik algılama bölgesi (ESZ) dahil olmak üzere çeşitli parçacık boyutlandırma teknikleri kategorileri(ref. 3’tegözden geçirilmiştir) kullanılarak analiz edilmiştir. Bununla birlikte, bu teknikler granül şekli ve boyut dağılımı varlığında nişasta granül boyutlarının belirlenmesi için eşit derecede uygun değildir. Işık, konfokal ve taramalı elektron mikroskopisi de dahil olmak üzere mikroskopi, morfoloji4,5,6,7, yapı 8,9 ve nişaste granüllerinin gelişimi10,11 çalışmaları için mükemmeldir, ancak bazı doğal eksiklikler nedeniyle boyut dağılımlarını tanımlamak için pek uygun değildir. Çeşitli türlerden nişastelerin granül boyutlarının belirlenmesinde kullanılan mikroskobik granül görüntülerin doğrudan ölçümleri veya optik mikroskopi verilerinin (IAOM) yazılım destekli görüntü analizi, mısır12, buğday13,14,patates15 ve arpa16dahil olmak üzere, nişasta granül görüntülerinin çok sınırlı sayıda (on ila birkaç bin) sadece 1D (genellikle maksimal uzunluk) veya 2D (yüzey alanı) boyutlarını ölçebilir. Doğal olarak tekniklerle kısıtlanan küçük granül örnekleme boyutları, nişastanın birim ağırlığı başına muazzam granül sayıları göz önüne alındığında nadiren istatistiksel olarak temsil edilebilir (~120 x 10 gram başına6, 10 μm kürenin tümü 1,5 g/cm³ yoğunlukta varsayılır) ve bu nedenle sonuçların zayıf tekrarlanabilirliğine yol açabilir. Sd / StFFF tekniği yüksek hız ve çözünürlüğe ve nişasta granüllerinin dar boyut fraksiyonlarına sahip olabilir17, ancak muhtemelen doğruluğu hasarlardan, farklı şekillerden ve nişasta granüllerinin yoğunluğundan ciddi şekilde etkilenebileceği için nadiren kullanılmıştır. Lazer kırınım tekniği en yaygın kullanılan tekniktir ve tüm büyük mahsul türleri için nişaste granül boyutu analizleri için uygulanmıştır3,14,16. Tekniğin birçok avantajı olmasına rağmen, granül şekil dağılımı varlığında nişasta granül boyutlarının belirlenmesi için aslında uygun değildir. Eşzamanlı lazer kırınım araçlarının çoğu, tekdüze küresel parçacıklar için Mie ışık saçılma teorisi18’e ve diğer bazı homojenlik şekilleri için değiştirilmiş Mie teorisi18’e dayanır. Bu nedenle teknik, doğal olarak parçacık şekillerine karşı çok hassastır ve belirli homojenlik şekilleri için bile tamamen uygun değildir19, farklı oranlarda bir dizi şekle sahip nişasta granülleri için bırakın. ESZ tekniği, elektrik alanı rahatsızlığını bir diyafram açıklığından geçen parçacığın hacmiyle orantılı olarak ölçen bir tekniktir. Granül hacim boyutlarının yanı sıra sayı ve hacim dağıtım bilgilerini vb. ESZ tekniği renk, şekil, kompozisyon veya kırılma indeksi de dahil olmak üzere parçacıkların herhangi bir optik özelliğinden bağımsız olduğundan ve sonuçlar çok tekrarlanabilir olduğundan, özellikle bir dizi şekle sahip nişasta granüllerinin boyut dağılımlarını belirlemek için uygundur.
Nişaste granül boyutları da birçok parametre kullanılarak tanımlanmıştır. Genellikle, bazı durumlarda mikroskobik olarak ölçülen 2D görüntülerin12,20veya eşdeğer küre çaplarının ortalamalarının aritmetik araçları olan ortalama çaplarla basit bir şekilde tanımlanmıştır3. Diğer durumlarda, granül boyutu dağılımları, normal dağılım 14 ,23, 24,25,26 varsayılarak21,22,dağılım ortalama hacmi veya ortalama çapı (küre eşdeğeri, sayı, hacim veya yüzey alanına göre ağırlıklandı) kullanılarak belirtilmiştir. Çeşitli analizlerden nişasta granül boyutlarının bu tanımlayıcıları çok farklı bir yapıya sahiptir ve kesinlikle karşılaştırılamaz. Farklı türlerden nişaste granüllerinin bu “boyutları” ve hatta aynı türün aynı dokuları doğrudan karşılaştırıldığında çok yanıltıcı olabilir. Ayrıca, varsayılan normal dağılımların yayılma (veya şekil) parametresi, yani dağılımın genişliğini (yani boyutların yayılmasını) ölçen standart sapma σ (veya grafik standart sapma σg)çoğu çalışmada göz ardı edilmiştir.
Nişasta granül boyutlandırma analizlerinin karşı karşıya olduğu yukarıda belirtilen kritik sorunları çözmek için, ESZ tekniğini kullanarak nişasta örneklerinin granül boyut dağılımlarının tekrarlanabilir ve istatistiksel olarak geçerli tayin edilmesi ve belirlenen granül lognormal boyut dağılımlarının, benimsenmiş iki parametreli çarpanlı form27 kullanılarak daha iyi doğruluk ve karşılaştırılılabilirlik ile doğru bir şekilde belirtilmesi için bir prosedür özetledik. Doğrulama ve gösterim için, prosedürü kullanarak sweetpotato nişasta örneklerinin granül boyutlandırma analizlerini çoğalttık ve grafik geometrik araçlarını ve multiplicative standart sapmalarını s * kullanarak lognormal diferansiyel hacim yüzdesi hacim eşdeğeri küre çapı 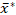 dağılımlarını
dağılımlarını 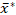 x/ (çarpın ve bölün) s* formunda belirttik.
x/ (çarpın ve bölün) s* formunda belirttik.
Protocol
Representative Results
Discussion
Özetlenen prosedür, nişasta granül boyutu analizleri için mevcut birkaç yöntemde bazı kritik sorunları çözmüştür, 3B granüllerin uygunsuz 1D veya 2D boyutlandırılması, tekdüze olmayan granül şekilleri nedeniyle boyutlandırma ölçümlerinin bozulması, sınırlı granül numune boyutları nedeniyle zayıf tekrarlanabilirlik ve şüpheli istatistiksel geçerlilik, hem granül şekli hem de normal olmayan boyut dağılımları varlığında granül boyutlarının yanlış veya yanlış spesifikasyonu …
Divulgations
The authors have nothing to disclose.
Acknowledgements
Bu çalışma kısmen Kooperatif Tarım Araştırma Merkezi ve Prairie View A&M Üniversitesi Tarım ve İnsan Bilimleri Koleji Entegre Gıda Güvenliği Araştırma Merkezi tarafından desteklenmektedir. Hua Tian’a teknik desteği için teşekkür ederiz.
Materials
| Analytical beaker | Beckman Coulter Life Sciences | A35595 | Smart-Technology (ST) beaker |
| Aperture tube, 100 µm | Beckman Coulter Life Sciences | A36394 | For the MS4E, , 1000 µm |
| Disposable transfer pipettor, | Fisher Scientific (Fishersci.com) | 13-711-9AM | Other disposable transfer pipettors with similar orifice can also be used. |
| Fisherbrand Conical Polypropylene Centrifuge Tubes, 50 ml | Fisher Scientific (Fishersci.com) | 05-539-13 | Any other similar types of tubes can be used. |
| Glass beakers, 150 to 250 ml | Fisher Scientific (Fishersci.com) | 02-540K | These beakers are used to contain methanol for washing the aperture tube and stirer between runs. |
| LiCl | Fisher Chemical | L121-100 | |
| Methanol | Fisher Chemical | A412-500 | Buy in bulk as the analysis uses a large quantity of methanol. |
| Mettler Toledo ML-T Precision Balances | Mettler Toledo | 30243412 | Any other precision balance with a readablity 0.01 g to 1 mg will work. |
| Multisizer 4e Coulter Counter | Beckman Coulter Life Sciences | B23005 | The old model, Multisizer 3 can also be used with slight adjustment of parameters. The 4e model comes with a 100 μm aperture tube. Other aperture tubes of different diameter can be purchased separately from the company. |
| Ultrasonic processor UP50H | Hielscher Ultrasound Technology | UP50H | Other laborator sonicator having a low-power (<50 Watt) output can be also used. Both MS1 and MS2 sonotrodes for the particular sonicator can be used to disperse starch granules in 5 ml methanol. Always use the lowest setting first, 20% amplitude and 0.1 or 0.2 cycle, and raise the setting if aggregates persist in suspension. |
References
- Shannon, J. C., Garwood, D. L., Boyer, C. D., BeMiller, J., Whistler, R. . Starch:Chemistry and Technology Food Science and Technology. , 23-82 (2009).
- Singh, N., Singh, J., Kaur, L., Singh Sodhi, N., Singh Gill, B. Morphological, thermal and rheological properties of starches from different botanical sources. Food Chemistry. 81 (2), 219-231 (2003).
- Lindeboom, N., Chang, P. R., Tyler, R. T. Analytical, biochemical and physicochemical aspects of starch granule size, with emphasis on small granule starches: a review. Starch – Stärke. 56 (34), 89-99 (2004).
- Baldwin, P. M., Davies, M. C., Melia, C. D. Starch granule surface imaging using low-voltage scanning electron microscopy and atomic force microscopy. International Journal of Biological Macromolecules. 21 (1-2), 103-107 (1997).
- Jane, J. L., Kasemsuwan, T., Leas, S., Zobel, H., Robyt, J. F. Anthology of starch granule morphology by scanning electron microscopy. Starch-Stärke. 46 (4), 121-129 (1994).
- Matsushima, R., Nakamura, Y. . Starch: Metabolism and Structure. , 425-441 (2015).
- Wang, S. -. q., Wanf, L. -. l., Fan, W. -. h., Cao, H., Cao, B. -. s. Morphological analysis of common edible starch granules by scanning electron microscopy. Food Science. 32 (15), 74-79 (2011).
- Baldwin, P. M., Adler, J., Davies, M. C., Melia, C. D. Holes in starch granules: confocal, SEM and light microscopy studies of starch granule structure. Starch-Stärke. 46 (9), 341-346 (1994).
- Chakraborty, I., Pallen, S., Shetty, Y., Roy, N., Mazumder, N. Advanced microscopy techniques for revealing molecular structure of starch granules. Biophysical Reviews. 12 (1), 105-122 (2020).
- Bechtel, D. B., Wilson, J. D. Amyloplast formation and starch granule development in hard red winter wheat. Cereal Chemistry. 80 (2), 175-183 (2003).
- Evers, A. Scanning electron microscopy of wheat starch. III. Granule development in the endosperm. Starch-Stärke. 23 (5), 157-162 (1971).
- Wang, Y. J., White, P., Pollak, L., Jane, J. L. Characterization of starch structures of 17 maize endosperm mutant genotypes with Oh43 inbred line background. Cereal Chemistry. 70, 171-179 (1993).
- Peng, M., Gao, M., Abdel-Aal, E. S. M., Hucl, P., Chibbar, R. N. Separation and characterization of A-and B-type starch granules in wheat endosperm. Cereal Chemistry. 76, 375-379 (1999).
- Wilson, J. D., Bechtel, D. B., Todd, T. C., Seib, P. A. Measurement of wheat starch granule size distribution using image analysis and laser diffraction technology. Cereal Chemistry. 83 (3), 259-268 (2006).
- Liu, Q., Weber, E., Currie, V., Yada, R. Physicochemical properties of starches during potato growth. Carbohydrate Polymers. 51 (2), 213-221 (2003).
- Chmelik, J., et al. Comparison of size characterization of barley starch granules determined by electron and optical microscopy, low angle laser light scattering and gravitational field-flow fractionation. Journal of the Institute of Brewing. 107 (1), 11-17 (2001).
- Moon, M. H., Giddings, J. C. Rapid separation and measurement of particle size distribution of starch granules by sedimentation/steric field-flow fractionation. Journal of Food Science. 58 (5), 1166-1171 (1993).
- Wriedt, T., Wolfram, H., Wriedt, T. . The Mie Theory: Basics and Applications. , 53-71 (2012).
- Schuerman, D. W., Wang, R. T., Gustafson, B. &. #. 1. 9. 7. ;. S., Schaefer, R. W. Systematic studies of light scattering. 1: Particle shape. Applied Optics. 20 (23), 4039-4050 (1981).
- Goering, K. J., Fritts, D. H., Eslick, R. F. A study of starch granule size and distribution in 29 barley varieties. Starch-Stärke. 25 (9), 297-302 (1973).
- Chen, Z., Schols, H. A., Voragen, A. G. J. Starch granule size strongly determines starch noodle processing and noodle quality. Journal of Food Sciences. 68 (5), 1584-1589 (2003).
- Dai, Z. M. Starch granule size distribution in grains at different positions on the spike of wheat (Triticum aestivum L.). Starch-Starke. 61 (10), 582-589 (2009).
- Edwards, M. A., Osborne, B. G., Henry, R. J. Effect of endosperm starch granule size distribution on milling yield in hard wheat. Journal of Cereal Science. 48 (1), 180-192 (2008).
- Karlsson, R., Olered, R., Eliasson, A. C. Changes in starch granule size distribution and starch gelatinization properties during development and maturation of wheat, barley and rye. Starch – Starke. 35 (10), 335-340 (1983).
- Li, W. -. Y., et al. Comparison of starch granule size distribution between hard and soft wheat cultivars in Eastern China. Agricultural Sciences China. 7 (8), 907-914 (2008).
- Park, S. H., Wilson, J. D., Seabourn, B. W. Starch granule size distribution of hard red winter and hard red spring wheat: Its effects on mixing and breadmaking quality. Journal of Cereal Science. 49 (1), 98-105 (2009).
- Limpert, E., Stahel, W. A., Abbt, M. Log-normal distributions across the sciences: keys and clues. Bioscience. 51 (5), 341-352 (2001).
- Gao, M., et al. Self-preserving lognormal volume-size distributions of starch granules in developing sweetpotatoes and modulation of their scale parameters by a starch synthase II (SSII). Acta Physiologiae Plantarum. 38 (11), 259 (2016).
- Wattebled, F., et al. STA11, a Chlamydomonas reinhardtii locus required for normal starch granule biogenesis, encodes disproportionating enzyme. Further evidence for a function of alpha-1,4 glucanotransferases during starch granule biosynthesis in green algae. Plant Physiology. 132 (1), 137-145 (2003).
- Ji, Y., Seetharaman, K., White, P. J. Optimizing a Small-Scale Corn-Starch Extraction Method for Use in the Laboratory. Cereal Chemistry. 81 (1), 55-58 (2004).
- Halloy, S., Whigham, P. The lognormal as universal descriptor of unconstrained complex systems: a unifying theory for complexity. Proceedings of the 7th Asia-Pacific Complex Systems Conference. , 309-320 (2004).
- Furusawa, C., Suzuki, T., Kashiwagi, A., Yomo, T., Kaneko, K. Ubiquity of log-normal distributions in intra-cellular reaction dynamics. Biophysics (Nagoya-shi). 1, 25-31 (2005).

