Ett experiment med funktionell nära-infraröd spektroskopi och robotassisterade flerledspekande rörelser i nedre extremiteten
Summary
Det uppskattas att 1 av 6 individer i världen kommer att få en stroke under sin livstid, vilket orsakar långvarig funktionsnedsättning, vars rehabiliteringsmekanismer fortfarande är dåligt förstådda. Denna studie föreslår ett protokoll för att utvärdera hjärnaktivering genom funktionell nära-infraröd spektroskopi (fNIRS) under en robotterapisession i nedre extremiteter.
Abstract
Stroke drabbar cirka 17 miljoner individer världen över varje år och är en ledande orsak till långvarig funktionsnedsättning. Robotterapi har visat sig lovande när det gäller att hjälpa strokepatienter att återfå förlorade motoriska funktioner. En möjlig väg för att öka förståelsen för hur motorisk återhämtning sker är att studera hjärnans aktivering under de rörelser som terapin riktar in sig på hos friska individer. Funktionell nära-infraröd spektroskopi (fNIRS) har dykt upp som en lovande hjärnavbildningsteknik för att undersöka neurala underlag för motorisk funktion. Denna studie syftade till att undersöka fNIRS neurala korrelat av komplexa rörelser i nedre extremiteterna hos friska försökspersoner. Deltagarna ombads att utföra cykler av vila och rörelse i 6 minuter med hjälp av en robotanordning för motorisk rehabilitering. Uppgiften krävde koordinerade knä- och fotledsrörelser för att peka mot mål som visades på en datorskärm. Två experimentella betingelser med olika nivåer av rörelsehjälp från roboten undersöktes. Resultaten visade att fNIRS-protokollet effektivt detekterade hjärnregioner associerade med motorisk kontroll under uppgiften. Noterbart är att alla försökspersoner uppvisade större aktivering i det kontralaterala premotoriska området under tillståndet utan assistans jämfört med det assisterade tillståndet. Sammanfattningsvis verkar fNIRS vara ett värdefullt tillvägagångssätt för att upptäcka förändringar i oxihemoglobinkoncentrationen i samband med pekrörelser i flera leder i nedre extremiteten. Denna forskning kan bidra till förståelsen av strokemotoriska återhämtningsmekanismer och kan bana väg för förbättrade rehabiliteringsbehandlingar för strokepatienter. Ytterligare forskning behövs dock för att fullt ut belysa potentialen för fNIRS för att studera motorisk funktion och dess tillämpningar i kliniska miljöer.
Introduction
Epidemiologiska data visar att det över hela världen finns ~17 miljoner nya fall av stroke varje år, med en ökning av incidensen i låg- och medelinkomstländer1. Antalet nya fall beräknas öka till 77 miljoner år 20302. Motorisk nedsättning på grund av stroke påverkar ofta patientens rörlighet och delaktighet i dagliga aktiviteter, vilket bidrar till en låg livskvalitet. Traditionell motorisk rehabilitering inkluderar manuell terapi, men under de senaste decennierna har robotsystem för rehabilitering utvecklats. Dessa system kan leverera behandling med hög intensitet, dos, kvantifierbarhet, tillförlitlighet, repeterbarhet och flexibilitet3 och har visat potential som effektiva rehabiliteringsbehandlingar för både akuta och kroniska strokepatienter 4,5,6. Förutom att ge terapi kan robotsystem för rehabilitering användas som utvärderingsverktyg eftersom de kan utrustas med sensorer som kan mäta patientens rörelsekinematiska / kinetiska data 7,8. För motorisk rehabilitering i övre extremiteterna har sådana data inte bara visat sig vara användbara för att bedöma nivån på patientens motoriska återhämtning som framkallas av robotterapi och fungerat som ett kompletterande verktyg till traditionella kliniska bedömningar 9,10, utan de har också bidragit till att öka förståelsen för processen för motorisk återhämtning från stroke11, 12 samt neural kontroll av rörelse och motorisk inlärning hos friska försökspersoner 3,13,14. Som ett resultat av detta har dessa fynd gett en grund för att förbättra rehabiliteringsbehandlingarna15.
Under de senaste två decennierna har många robotenheter för neurorehabilitering av nedre extremiteter föreslagits, allt från exoskelett som stöder patientens kroppsvikt under gång (t.ex. över ett löpband, som Lokomat16) till stationära robotsystem som gör det möjligt för patienten att träna fotleden, knäet eller foten utan att gå (t.ex. Rutgers Ankle17, High-Performance Ankle Rehabilitation Robot18 och Gwangju Institute of Science and Technology (GIST) fotleds-/fotrehabiliteringsrobot19) eller aktiva fotortoser som aktiveras exoskelett som bärs av patienten för att gå över marken eller över ett löpband (t.ex. Powered Gait Orthosis20 och MIT Anklebot21). Se 22,23,4 för en genomgång av robotar för rehabilitering av nedre extremiteter.
Resultaten av kliniska studier av robotutrustning för rehabilitering av nedre extremiteter på strokepatienter har varit uppmuntrande och har visat att dessa system kan förbättra ledernas rörelseomfång (ROM), muskelstyrka eller gång, beroende på den specifika enheten och det kliniska protokollet (se 24,25 för en granskning av effektiviteten hos robotar för nedre extremiteter för rehabilitering). Även om det har antagits att robotassisterad terapi främjar neuroplastiska förändringar, som i slutändan resulterar i förbättrade motoriska förmågor26, är det fortfarande mestadels oklart hur processen för motorisk återhämtning från stroke exakt sker och vilka robotträningsprotokoll som optimerar processen för återhämtning av motoriska förmågor i nedre extremiteterna. Faktum är att det finns en betydande, växande skillnad mellan den ökande utvecklingen av rehabiliteringsrobotar (antingen av akademiska forskare eller kommersiella enheter) och den begränsade förståelsen av de neurofysiologiska mekanismer som ligger till grund för motorisk återhämtning4. Mätningar av rörelsekinematik eller ledmoment tagna med inbyggda sensorer har bidragit till att kvantitativt beskriva motoriska beteendeförändringar som uppstår när patienter återfår motoriska förmågori nedre extremiteterna 27,28,29, vilket delvis fyller denna lucka. De neurala korrelat som ligger till grund för sådana förändringar har dock undersökts mindre. Detta beror på flera anledningar.
Funktionell avbildning av hjärnan är tidskrävande och ibland svår att genomföra i samband med kliniska prövningar, som ofta kräver att patientbördan minimeras för att maximera sannolikheten för att patienten följer studien. Detta gäller särskilt för personer som har drabbats av stroke, med tanke på att trötthet och muskelsvaghet efter stroke ofta observeras30. Avbildningsmodaliteter som är baserade på magnetfält, såsom funktionell magnetisk resonanstomografi (fMRI), kräver också att både patient- och robothårdvara är magnetsäker.
Bland icke-invasiva avbildningsmodaliteter är funktionell nära-infraröd spektroskopi (fNIRS) en avbildningsteknik som är särskilt lämplig för att bedöma områden för hjärnaktivering hos personer som genomgår robotterapi. På samma sätt som fMRI mäter fNIRS blodets syresättning/deoxygenering i hjärnan. Men till skillnad från fMRI är fNIRS helt kompatibel med robothårdvara, och den är ofta bärbar, till och med användbar vid sängen. Dessutom har fNIRS låg kostnad och mindre känslighet för rörelseartefakter 31,32,33.
Trots dess tydliga fördelar och utbredda användning i många kliniska miljöer sedan dess första introduktion i slutet av 70-talet34, har endast ett fåtal studier använt fNIRS för att kvantifiera hjärnaktivering i samband med rörelser i nedre extremiteter och strokemotorisk återhämtning. FNIRS-studier som syftar till att belysa mekanismer för neural kontroll av rörelse och/eller mekanismer eller utvärdering av motorisk återhämtning från stroke har främst undersökt rörelser i en led (t.ex. dorsalflexion, plantarflexion eller knäextensionsrörelser 35,36,37), gång 38,39,40,41,42,43 eller cykling 44. Se45 för en recension. På samma sätt har fNIRS-studier om robotassisterad terapi för de nedre extremiteterna främst fokuserat på robotassisterad gångrehabilitering; Se46 för en recension. Några studier har fokuserat på att använda fNIRS som en del av ett Brain-Computer Interface (BCI) -system för att härleda styrsignaler för robotenheter47,48; även om detta forskningsområde också är beroende av bearbetning av fNIRS-signaler, är dess mål annorlunda och främst inriktat på att avkoda patientens avsikter (t.ex. patienter med svåra motoriska funktionsnedsättningar).
Pilotstudien som presenteras här är en del av ett första försök att undersöka effekterna av ett robotsystem för rehabilitering av nedre extremiteter. Roboten kan leverera målinriktad rehabilitering av nedre extremiteter som involverar träning i vardagliga flerledsrörelser samt ge terapi till enskilda leder (t.ex. knä eller fotled) i nedre extremiteten (dvs. implementera ett rehabiliteringsprogram nedifrån och upp).
Studien syftade till att undersöka genomförbarheten av ett experimentellt protokoll som krävde insamling av fNIRS-data under utförandet av pekrörelser i nedre extremiteter och flera leder. Varaktigheten av datainsamlingsperioden i denna studie, som var begränsad till 6 minuter, är kortare än typiska fNIRS-protokoll. Detta var ett medvetet val som gjordes i syfte att förbättra den praktiska och kliniska tillämpbarheten av denna forskning, särskilt hos patienter med begränsad rörlighet eller styrka. Att identifiera fNIRS-korrelat till sådana komplexa rörelser i flera leder och få insikter i hur hjärnaktivering moduleras av robotassistans var också intressanta punkter. För detta ändamål genomfördes två experimentsessioner med samma deltagare: en utan robotassistans och en med robotassistans. Slutligen är det viktigt att påpeka att denna studie fokuserade på friska försökspersoner för att skapa en grund för framtida forskning när det gäller att registrera protokollgenomförbarhet och utvärdering av hjärnaktivering under rörelser som är inriktade på robotterapi.
Apparat
En bärbar robot som är utformad för att ge rehabilitering av nedre extremiteter (se figur 1) användes för att utföra våra experiment. Roboten har en 3D-nåbar arbetsyta och är kompakt och lätt, väger cirka 35 lb., vilket gör den enkel att transportera och installera.
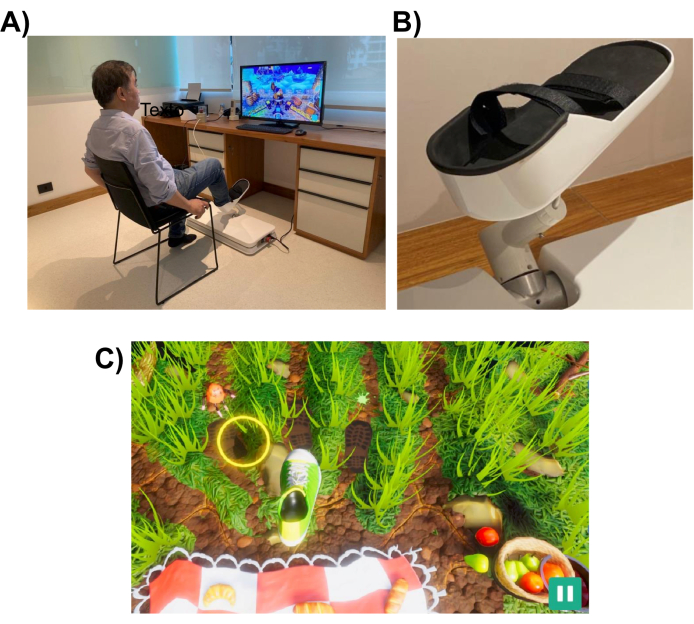
Figur 1: Experimentell uppställning. (A) Robotsystemet (installerat på golvet) som är utformat för den nedre extremiteten. En volontär visas använda gränssnittet med sin högra fot. (B) Stödstruktur för försökspersonens fot som möjliggör fastsättning på robotsystemet. (C) En skärmdump av Picnic-spelet. Målet med spelet är att flytta foten (grön och vit sko) till målet (gul cirkel). Klicka här för att se en större version av denna figur.
Robotsystemet är utformat för att hjälpa en patient att utföra rörelser i nedre extremiteter som liknar de som utförs i vardagliga uppgifter, som att peka eller sparka. Den använder interaktiva virtual reality-spel, som visas på en datorskärm eller en tv-skärm placerad framför robotenheten (se figur 1). Robotgripdonet fästs på patientens nedre extremitet (t.ex. fotleden) och dess position mappas till positionen för en markör på skärmen. Ett typiskt spel visar patientens rörelsemål (t.ex. föremålet att peka på eller var man ska sparka bollen).
För att slutföra rörelseuppgiften kan roboten hjälpa patienten med en assistansnivå som kan variera från full assistans till ingen. Nivån på robotassistansen väljs i början av varje rehabiliteringssession baserat på patientens nivå av motorisk funktionsnedsättning. Rörelserna som utförs av försökspersonen används av spelet för att poängsätta patientens prestation och ge dem feedback om deras prestation (t.ex. ROM, antal rörelser och nivå av robotassistans). Spelen är utformade för att vara interaktiva och underhållande för att upprätthålla patientens intresse och uppmärksamhet. I den här studien spelade deltagarna “Picknick-spelet”, där spelaren var tvungen att stoppa insekterna från att nå handduken och stjäla maten (se figur 1, nedre panelen, för en skärmdump).
Datainsamlingen utfördes med ett portabelt fNIRS-insamlingssystem med två olika kontinuerliga vågopatoder (760 nm och 850 nm), 8 dual-tip LED-källor och 8 dual-tip aktiva detektorer. Signalerna samlades in med en samplingsfrekvens på 10,17 Hz. En bärbar dator användes för kalibreringsoptimering och signalregistrering med hjälp av ett Wi-Fi-nätverk skapat av fNIRS-systemet.
En mössa användes för att hålla optoderna på de förutbestämda platserna. Källorna och detektorerna placerades enligt det internationella EEG-systemet 10-10 i en rutnätsfördelning. Varje fNIRS-kanal definierades av ett källdetektorpar med interoptodavstånd på cirka 30 mm. Optoderna placerades över de kompletterande motor-, förmotor- och motorområdena på de platser som visas i figur 2. Det totala antalet kanaler var 28, varav 8 var kortdistanskanaler som kopplades till varje källa med hjälp av en fiberoptisk adapter till en enda detektor. Med tanke på hårdvarans multiplexeringsinställning är det möjligt att samla in information på korta avstånd från alla källor med endast en detektor.
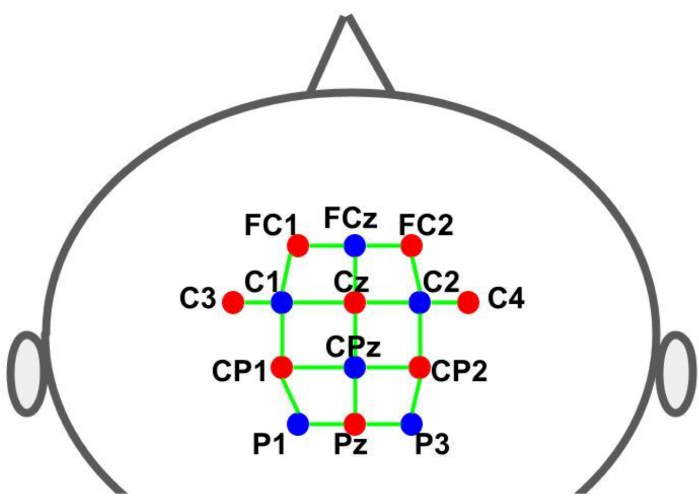
Figur 2: Montagelayout med 10-10 EEG-systemet. Bokstäverna och siffrorna anger källans/detektorns placering. De röda och blå prickarna representerar käll- respektive detektoroptoderna. De gröna linjerna representerar fNIRS-kanalerna som består av käll- och detektorpar. Klicka här för att se en större version av denna figur.
Experimentell design
Experimentet utfördes under två distinkta experimentella förhållanden, som skilde sig åt i nivån av assistans från roboten för försökspersonens rörelser. I det första tillståndet var roboten programmerad att inte ge någon hjälp till försökspersonens rörelser, medan roboten i det andra tillståndet styrde försökspersonens fot- och benrörelser (robotassisterad rörelse).
Varje experiment följde ett paradigm för blockdesign som involverade alternerande cykler av en motorisk uppgift (spela spelet – 30 s) och vila (30 s), vilket illustreras i figur 3. Början och slutet av varje fas (lek/spel eller vila) signalerades visuellt till försökspersonen via datorskärmen. Under vilofasen visades ett meddelande som indikerade en paus. Varje cykel (spel/spel + vila) hade en varaktighet på 60 s och upprepades sex gånger, vilket resulterade i en total körtid på 360 s (6 min).
Deltagarna lekte “Picknickleken”, där målet var att hindra insekter från att nå handduken och stjäla mat. Detta spel involverade en sekvens av rörelser i de nedre extremiteterna, som började från ett utsett hemmål (initial position) och sträckte sig mot ett av tre yttre mål innan de återvände till hemmålet. På skärmen representerades de yttre målen visuellt som animerade rörliga insekter, som deltagarna var tvungna att nå och kliva på. Det fanns tre mål som sträckte sig utåt, var och en slumpmässigt presenterad lika många gånger, tillsammans med ett gemensamt hemmål för varje rörelse. Avståndet som foten behövde för att färdas från hemmålet till de yttre målens position bildade en båge, ungefär 26 cm. Den motoriska uppgiften krävde utförande av flerledsrörelser, vilket krävde koordination mellan knäböjning/sträckning, plantarflexion och dorsalflexionsrörelser.
fNIRS-datainspelningarna synkroniserades med de visuella stimuli som spelet presenterade för försökspersonen genom en transistor-transistor-logisk (TTL) puls som genererades av roboten. Pulser genererades i början av varje fas (lek/spel och vila). Således utfördes all tidskontroll av spelet, som gav visuella signaler (mål) till deltagaren för att starta varje rörelse, skickade TTL-signaler till fNIRS-systemet för att markera hjärnaktivitetsregistreringarna och, om experimentet krävde det, skickade signaler till robotens styrsystem för att initiera rörelsehjälp.
Protocol
Representative Results
Discussion
I denna proof-of-concept-studie undersöktes möjligheten att dra slutsatser om kartläggning av hjärnaktivering med hjälp av fNIRS-data från friska försökspersoner medan de tränade med olika typer av rörelser med hjälp av en robot för rehabilitering av nedre extremiteter. Typiska fNIRS-inspelningssessioner hos vuxna är längre än 6 min54. Men för att göra inspelningar möjliga i samband med en rehabiliteringsmiljö måste experimentets totala varaktighet minimeras för att undvika on…
Divulgations
The authors have nothing to disclose.
Acknowledgements
Åsikterna, hypoteserna, slutsatserna och rekommendationerna i denna studie är författarnas egna och representerar inte nödvändigtvis finansiärens åsikter. JRS är tacksamma mot Sao Paulo Research Foundation (FAPESP, anslagsnummer 2021/05332-8, 2018/04654-9, 2018/21934-5 och 2023/02538-0) och Jackson Cionek för tekniskt stöd. AMM och Vivax Ltda är tacksamma mot FAPESP (São Paulo Research Foundation) och FINEP (Brazilian Innovation Agency). Projektet finansierades med anslag från FAPESP (anslagsnummer 2018/09559-4) och FINEP (anslagsnummer 2019/09933-6).
Materials
| 32 inch Smart TV | Samsung | N/A | TV connected to robot via HDMI cable |
| 8-detector silicon photodiode (SiPD) optodes for optical detection with dual tip | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| 8-source optodes bundle for optical illumination with dual tip | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| Aurora acquisition software | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| Laptop Precision XPS 13 | Dell Technologies (Round Rock, TX, USA) | ||
| nirsLAB fNIRS Analysis software | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | |
| NIRSports2 fNIRS acquisition system | NIRx Medical Technologies (Glen Head, NY, USA) | https://nirx.net/nirsport | It has two different continuous wave optics (760 and 850 nm), 8 dual-ended LED sources and 8 dual-ended active detectors. |
| R | R-project.org (open source software) | https://www.r-project.org/ | |
| Standard cut cap, black color for up to 128 holders. | Easycap GmbH (Wörthsee, Germany) | https://www.easycap.de/ | |
| Vivax Assistive Rehabilitation Machine (ARM) | Vivax Ltda (São Paulo, Brazil) | https://vivaxbr.com/home/ | It is a portable robot designed to deliver lower limb rehabilitation. It has a 3D reachable workspace and is compact and light, weighing about 35 lb., which makes it easy to transport and to install. |
References
- GBD 2016 Stroke Collaborators. Global, regional, and national burden of stroke, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. The Lancet. Neurology. 18 (5), 439-458 (2019).
- GBD 2019 Stroke Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. The Lancet. Neurology. 20 (10), 795-820 (2021).
- Huang, V. S., Krakauer, J. W. Robotic neurorehabilitation: a computational motor learning perspective. Journal of NeuroEngineering and Rehabilitation. 6, 5 (2009).
- Hobbs, B., Artemiadis, P. A Review of Robot-Assisted Lower-Limb Stroke Therapy: Unexplored Paths and Future Directions in Gait Rehabilitation. Frontiers in neurorobotics. 14, 19 (2020).
- Bertani, R., Melegari, C., De Cola, M. C., Bramanti, A., Bramanti, P., Calabrò, R. S. Effects of robot-assisted upper limb rehabilitation in stroke patients: a systematic review with meta-analysis. Neurological Sciences. 38 (9), 1561-1569 (2017).
- Warutkar, V., Dadgal, R., Mangulkar, U. R. Use of robotics in gait rehabilitation following stroke: A review. Cureus. 14 (11), e31075 (2022).
- Dipietro, L., et al. Changing motor synergies in chronic stroke. Journal of Neurophysiology. 98 (2), 757-768 (2007).
- Dipietro, L., et al. Learning, not adaptation, characterizes stroke motor recovery: evidence from kinematic changes induced by robot-assisted therapy in trained and untrained task in the same workspace. IEEE Trans Neural Syst Rehabil Eng. 20 (1), 48-57 (2012).
- Bosecker, C., Dipietro, L., Volpe, B., Krebs, H. I. Kinematic robot-based evaluation scales and clinical counterparts to measure upper limb motor performance in patients with chronic stroke. Neurorehabilitation and Neural Repair. 24 (1), 62-69 (2010).
- Krebs, H. I., et al. Robotic measurement of arm movements after stroke establishes biomarkers of motor recovery. Stroke. 45 (1), 200-204 (2014).
- Volpe, B. T., et al. Robotic devices as therapeutic and diagnostic tools for stroke recovery. Archives of Neurology. 66 (9), 1086-1090 (2009).
- Hogan, N., et al. Motions or muscles? Some behavioral factors underlying robotic assistance of motor recovery. Journal of Rehabilitation Research and Development. 43 (5), 605-618 (2006).
- Shadmehr, R., Wise, S. P. . The Computational Neurobiology of Reaching and Pointing: A Foundation for Motor Learning. , (2005).
- Dipietro, L., Poizner, H., Krebs, H. I. Spatiotemporal dynamics of online motor correction processing revealed by high-density electroencephalography. J Cogn Neurosci. 26 (9), 1966-1980 (2014).
- Krebs, H., et al. Rehabilitation robotics: Performance-based progressive robot-assisted therapy. Autonomous Robots. 15, 7-20 (2003).
- Colombo, G., Joerg, M., Schreier, R., Dietz, V. Treadmill training of paraplegic patients using a robotic orthosis. Journal of Rehabilitation Research and Development. 37 (6), 693-700 (2000).
- Girone, M., et al. A Stewart platform-based system for ankle telerehabilitation. Autonomous Robots. 10, 203-212 (2001).
- Saglia, J. A., Tsagarakis, N. G., Dai, J. S., Caldwell, D. G. A high-performance redundantly actuated parallel mechanism for ankle rehabilitation. The International Journal of Robotics Research. 28 (9), 1216-1227 (2009).
- Yoon, J., Ryu, J. A novel reconfigurable ankle/foot rehabilitation robot. , 2290-2295 (2005).
- Ruthenberg, B. J., Wasylewski, N. A., Beard, J. E. An experimental device for investigating the force and power requirements of a powered gait orthosis. Journal of Rehabilitation Research and Development. 34 (2), 203-213 (1997).
- Forrester, L. W., et al. Clinical application of a modular ankle robot for stroke rehabilitation. NeuroRehabilitation. 33 (1), 85-97 (2013).
- Díaz, I., Gil, J. J., Sánchez, E. Lower-limb robotic rehabilitation: Literature review and challenges. Journal of Robotics. 2011, 759764 (2011).
- Zhang, X., Yue, Z., Wang, J. Robotics in lower-limb rehabilitation after stroke. Behavioural Neurology. 2017, 3731802 (2017).
- Zhang, M., Davies, T. C., Xie, S. Effectiveness of robot-assisted therapy on ankle rehabilitation – a systematic review. Journal of NeuroEngineering and Rehabilitation. 10, 30 (2013).
- Lo, K., Stephenson, M., Lockwood, C. Effectiveness of robotic assisted rehabilitation for mobility and functional ability in adult stroke patients: a systematic review protocol. JBI Database of Systematic Reviews and Implementation Reports. 15 (1), 39-48 (2017).
- Belda-Lois, J. M., et al. Rehabilitation of gait after stroke: a review towards a top-down approach. Journal of NeuroEngineering and Rehabilitation. 8, 66 (2011).
- Bortole, M., et al. The H2 robotic exoskeleton for gait rehabilitation after stroke: early findings from a clinical study. Journal of NeuroEngineering and Rehabilitation. 12, 54 (2015).
- Banala, S. K., Kim, S. H., Agrawal, S. K., Scholz, J. P. Robot assisted gait training with active leg exoskeleton (ALEX). IEEE Transactions on Neural Systems and Rehabilitation Engineering. 17 (1), 2-8 (2009).
- Bartenbach, V., Wyss, D., Seuret, D., Riener, R. A lower limb exoskeleton research platform to investigate human-robot interaction. 2015 IEEE International Conference on Rehabilitation Robotics (ICORR). 2015, 600-605 (2015).
- Hinkle, J. L., et al. Poststroke fatigue: Emerging evidence and approaches to management: A scientific statement for healthcare professionals from the American heart association. Stroke. 48 (7), e159-e170 (2017).
- Balardin, J. B., Zimeo Morais, G. A., Furucho, R. A., Trambaiolli, L. R., Sato, J. R. Impact of communicative head movements on the quality of functional near-infrared spectroscopy signals: negligible effects for affirmative and negative gestures and consistent artifacts related to raising eyebrows. Journal of Biomedical Optics. 22 (4), 4601 (2017).
- Nazeer, H., Naseer, N., Mehboob, A., Khan, M. J., Khan, R. A., Khan, U. S., Ayaz, Y. Enhancing classification performance of fNIRS-BCI by identifying cortically active channels using the z-score method. Sensors. 20 (23), 6995 (2020).
- Ayaz, H., et al. Optical imaging and spectroscopy for the study of the human brain: status report. Neurophotonics. 9, S24001 (2022).
- Chen, W. L., et al. Functional near-infrared spectroscopy and its clinical application in the field of neuroscience: Advances and future directions. Frontiers in Neuroscience. 14, 724 (2020).
- Yamamoto, K., Miyata, T., Onozuka, A., Koyama, H., Ohtsu, H., Nagawa, H. Plantar flexion as an alternative to treadmill exercise for evaluating patients with intermittent claudication. European Journal of Vascular and Endovascular Surgery. 33 (3), 325-329 (2007).
- Formenti, D., et al. Effects of knee extension with different speeds of movement on muscle and cerebral oxygenation. PeerJ. 6, 5704 (2018).
- Miyai, I., et al. Cortical mapping of gait in humans: a near-infrared spectroscopic topography study. NeuroImage. 14 (5), 1186-1192 (2001).
- Miyai, I., et al. Premotor cortex is involved in restoration of gait in stroke. Annals of Neurology. 52 (2), 188-194 (2002).
- Mihara, M., et al. Sustained prefrontal activation during ataxic gait: a compensatory mechanism for ataxic stroke?. NeuroImage. 37 (4), 1338-1345 (2007).
- Rea, M., et al. Lower limb movement preparation in chronic stroke: A pilot study toward an fNIRS-BCI for gait rehabilitation. Neurorehabilitation and Neural Repair. 28 (6), 564-575 (2014).
- Holtzer, R., Verghese, J., Allali, G., Izzetoglu, M., Wang, C., Mahoney, J. R. Neurological gait abnormalities moderate the functional brain signature of the posture first hypothesis. Brain Topography. 29 (2), 334-343 (2016).
- Kim, H. Y., Yang, S. P., Park, G. L., Kim, E. J., You, J. S. Best facilitated cortical activation during different stepping, treadmill, and robot-assisted walking training paradigms and speeds: A functional near-infrared spectroscopy neuroimaging study. NeuroRehabilitation. 38 (2), 171-178 (2016).
- Khan, H., Nazeer, H., Engell, H., Naseer, N., Korostynska, O., Mirtaheri, P. Prefrontal cortex activation measured during different footwear and ground conditions using fNIRS-A case study. 2021 IEEE International Conference on Artificial Intelligence and Mechatronics Systems (AIMS). , 1-6 (2021).
- Lin, P. Y., Chen, J. J., Lin, S. I. The cortical control of cycling exercise in stroke patients: an fNIRS study). Human Brain Mapping. 34 (10), 2381-2390 (2013).
- Yang, M., Yang, Z., Yuan, T., Feng, W., Wang, P. A systemic review of functional near-infrared spectroscopy for stroke: Current application and future directions. Frontiers in Neurology. 10, 58 (2019).
- Berger, A., Horst, F., Müller, S., Steinberg, F., Doppelmayr, M. Current state and future prospects of EEG and fNIRS in robot-assisted gait rehabilitation: A brief review. Frontiers in Human Neuroscience. 13, 172 (2019).
- Khan, R. A., Naseer, N., Qureshi, N. K., et al. fNIRS-based Neurorobotic Interface for gait rehabilitation. J NeuroEngineering Rehabil. 15 (1), 7 (2018).
- Khan, H., Naseer, N., Yazidi, A., Eide, P. K., Hassan, H. W., Mirtaheri, P. Analysis of Human Gait Using Hybrid EEG-fNIRS-Based BCI System: A Review. Front. Hum. Neurosci. 14, (2020).
- Delpy, D. T., Cope, M. Quantification in tissue near-infrared spectroscopy. Philosophical Transactions of the Royal Society B: Biological Sciences. 352 (1354), 649-659 (1997).
- Huppert, T. J. Commentary on the statistical properties of noise and its implication on general linear models in functional near-infrared spectroscopy. Neurophotonics. 3, 010401 (2016).
- Alexandre, F., Heraud, N., Oliver, N., Varray, A. Cortical implication in lower voluntary muscle force production in non-hypoxemic COPD patients. PLoS One. 9 (6), 100961 (2014).
- Yoon, T., Vanden Noven, M. L., Nielson, K. A., Hunter, S. K. Brain areas associated with force steadiness and intensity during isometric ankle dorsiflexion in men and women. Experimental Brain Research. 232 (10), 3133-3145 (2014).
- Ciccarelli, O., et al. Identifying brain regions for integrative sensorimotor processing with ankle movements. Experimental Brain Research. 166 (1), 31-42 (2005).
- Udina, C., et al. Functional near-infrared spectroscopy to study cerebral hemodynamics in older adults during cognitive and motor tasks: A review. Frontiers in Aging Neuroscience. 11, 367 (2020).
- Thickbroom, G. W., Phillips, B. A., Morris, I., Byrnes, M. L., Mastaglia, F. L. Isometric force-related activity in sensorimotor cortex measured with functional MRI. Experimental Brain Research. 121 (1), 59-64 (1998).
- Derosière, G., Alexandre, F., Bourdillon, N., Mandrick, K., Ward, T. E., Perrey, S. Similar scaling of contralateral and ipsilateral cortical responses during graded unimanual force generation. NeuroImage. 85 (1), 471-477 (2014).
- Shi, P., Li, A., Yu, H. Response of the cerebral cortex to resistance and non-resistance exercise under different trajectories: A functional near-infrared spectroscopy study. Frontiers in Neuroscience. 15, 685920 (2021).
- Dettmers, C., et al. Relation between cerebral activity and force in the motor areas of the human brain. Journal of Neurophysiology. 74 (2), 802-815 (1995).
- Keisker, B., Hepp-Reymond, M. C., Blickenstorfer, A., Kollias, S. S. Differential representation of dynamic and static power grip force in the sensorimotor network. The European Journal of Neuroscience. 31 (8), 1483-1491 (2010).
- Harada, T., Miyai, I., Suzuki, M., Kubota, K. Gait capacity affects cortical activation patterns related to speed control in the elderly. Experimental Brain Research. 193 (3), 445-454 (2009).
- Saleh, S., et al. The role of premotor areas in dual tasking in healthy controls and persons with multiple sclerosis: An fNIRS imaging study. Frontiers in Behavioral Neuroscience. 12, 296 (2018).
- Bonnal, J., et al. Relation between cortical activation and effort during robot-mediated walking in healthy people: A functional near-infrared spectroscopy neuroimaging study (fNIRS). Sensors. 22 (15), 5542 (2022).
- Shibuya, K., Sadamoto, T., Sato, K., Moriyama, M., Iwadate, M. Quantification of delayed oxygenation in ipsilateral primary motor cortex compared with contralateral side during a unimanual dominant-hand motor task using near-infrared spectroscopy. Brain Research. 1210, 142-147 (2008).
- Dai, T. H., Liu, J. Z., Sahgal, V., Brown, R. W., Yue, G. W. Relationship between muscle output and functional MRI-measured brain activation. Experimental brain research. 140 (3), 290-300 (2001).
- Cabibel, V., Hordacre, B., Perrey, S. Implication of the ipsilateral motor network in unilateral voluntary muscle contraction: the cross-activation phenomenon. Journal of Neurophysiology. 123 (5), 2090-2098 (2020).
- Akselrod, M., Martuzzi, R., Serino, A., vander Zwaag, W., Gassert, R., Blanke, O. Anatomical and functional properties of the foot and leg representation in areas 3b, 1 and 2 of primary somatosensory cortex in humans: A 7T fMRI study. NeuroImage. 159, 473-487 (2017).
- Brigadoi, S., Cooper, R. J. How short is short? Optimum source-detector distance for short-separation channels in functional near-infrared spectroscopy. Neurophotonics. 2 (2), 025005 (2015).
- Funahashi, S. Prefrontal contribution to decision-making under free-choice conditions. Frontiers in Neuroscience. 11, 431 (2017).
- Simon, S. R., Meunier, M., Piettre, L., Berardi, A. M., Segebarth, C. M., Boussaoud, D. Spatial attention and memory versus motor preparation: premotor cortex involvement as revealed by fMRI. Journal of Neurophysiology. 88 (4), 2047-2057 (2002).
- Desmurget, M., Sirigu, A. A parietal-premotor network for movement intention and motor awareness. Trends in Cognitive Sciences. 13 (10), 411-419 (2009).
- Nachev, P., Kennard, C., Husain, M. Functional role of the supplementary and pre-supplementary motor areas. Nature reviews. Neuroscience. 9 (11), 856-869 (2008).
- Thoenissen, D., Zilles, K., Toni, I. Differential involvement of parietal and precentral regions in movement preparation and motor intention. The Journal of neuroscience: the official journal of the Society for Neuroscience. 22 (20), 9024-9034 (2002).
- Al-Quraishi, M. S., Elamvazuthi, I., Tang, T. B., Al-Qurishi, M., Adil, S. H., Ebrahim, M. Bimodal data fusion of simultaneous measurements of EEG and fNIRS during lower limb movements. Brain Sciences. 11 (6), 713 (2021).
- Bishnoi, A., Holtzer, R., Hernandez, M. E. Brain Activation Changes While Walking in Adults with and without Neurological Disease: Systematic Review and Meta-Analysis of Functional Near-Infrared Spectroscopy Studies. Brain sciences. 11 (3), 291 (2021).
- Oh, S., Song, M., Kim, J. Validating attentive locomotion training using interactive treadmill: an fNIRS study. Journal of NeuroEngineering and Rehabilitation. 15 (1), 122 (2018).

