نقل الحرارة المريء للتحكم في درجة حرارة المريض وإدارة الحرارة المستهدفة
Summary
تقدم هذه الدراسة طريقة جديدة لتوفير التحكم في درجة حرارة المريض كفاءة التبريد أو الاحترار المرضى. على استخدام واحد، ثلاثية التجويف جهاز يوضع داخل المريء، شبيهة بأنبوب أوروجاستريك قياسية، ويربط الحرارة تبادل الوحدات القائمة لأداء الإدارة التلقائية درجة حرارة المريض.
Abstract
التحكم في درجة حرارة المريض مهم لمجموعة متنوعة من الظروف السريرية. التبريد العادي أو تقل درجة حرارة الجسم العادية يتم غالباً نيوروبروتيكشن بعد إهانة الدماغية (مثل السكتة الدماغية النزفية، نزيف تحت العنكبوتية، والسكتة القلبية، أو إصابة أخرى التاكسج). التبريد من الدول الحموية يعامل الحمى، ويقلل من الآثار السلبية هايبرثيرميا على إصابة الخلايا العصبية. هي درجة حرارة المرضى في غرفة العمليات لمنع انخفاض حرارة الجسم المحيطة بالجراحة غير مقصود، الذي يعرف بالتسبب في فقدان الدم زيادة وعدوى الجرح، وإصابة احتشاء عضلة القلب، بينما أيضا إطالة وقت الاسترداد. هناك الكثير من النهج المبلغ عنها لإدارة الحرارة، بما في ذلك أساليب بدائية أن معيار ممتدة الإمدادات (مثل، الجليد، مالحة مبردة، والمشجعين، والبطانيات) إنما متطورة أكثر التكنولوجيات المصممة لإدارة الحرارة عادة أكثر نجاحا في إيصال بروتوكولا أمثل. على مدى العقد الماضي، تطورت تقنيات متقدمة حول اثنين من أساليب نقل الحرارة: سطح الأجهزة (المياه البطانيات وتدفئة الهواء القسري) أو الأجهزة داخل الأوعية (القسطرة العقيمة التي تتطلب وضع الأوعية الدموية). في الآونة الأخيرة، أصبح جهاز رواية المتاحة هو وضعها في المريء، شبيهة بأنبوب أوروجاستريك قياسية، التي توفر نقل الحرارة فعالة عن طريق الأساسية للمريض. اتصال الجهاز الوحدات تبادل الحرارة الحالية للسماح للإدارة درجة حرارة المريض التلقائي عن طريق إليه مضاعفات، باستخدام درجة حرارة المريض من أجهزة استشعار درجة الحرارة القياسية (المستقيم، فولي، أو الأخرى الأساسية مجسات درجة الحرارة) كمتغير الإدخال. هذا النهج يلغي مضاعفات التنسيب والأوعية الدموية (تجلط وريدي عميق، وعدوى مجرى الدم الخط المركزي المرتبطة) ويقلل من عرقلة وصول المريض، ويسبب الارتعاش أقل بالمقارنة مع النهج السطحي. وأظهرت البيانات المنشورة أيضا على درجة عالية من الدقة والحفاظ على درجة الحرارة المستهدفة باستخدام نهج إدارة الحرارة المريء. ولذلك، والغرض من هذا الأسلوب توفير وسيلة بديلة منخفضة المخاطر لدرجة حرارة المريض التحكم في إعدادات الرعاية الحرجة.
Introduction
هناك حاجة كبيرة للإدارة درجة حرارة المريض عند التعامل مع طائفة واسعة من الظروف، بما في ذلك السكتة القلبية والمواد المقاومة للحرارة أو الحمى المتكررة وحمى العصبية وجراحة كبيرة. في الولايات المتحدة، اعتقال القلب نصف مليون سنوياً تأتي في المستشفى (على سبيل المثال، في المرضى الذين يخضعون للرعاية للشروط الطبية أو الجراحية العامة)1 أو الخروج من المستشفى (على سبيل المثال، في المنزل أو في الأماكن العامة، ثم الذين ينقلون إلى قسم الطوارئ)2. في كلا الحالتين، إلى حد كبير تحسين نتائج المرضى عند إدارة الحرارة النشطة التي تدار3 ، وإدارة الحرارة المستهدفة (الإيراد) معياراً للرعاية لسكتة قلبية منذ عام 2005. ويتم قبول المرضى ما يزيد على 5 مليون لوحدات العناية المركزة سنوياً في الولايات المتحدة4 . هذه، يطور الحمى في يصل إلى 45% من المرضى المصابين غير عصبيا5 وما يصل إلى 70% من المرضى المصابين عصبيا6. مكافحة الحمى في وحدة العناية المركزة يرتبط بتحسين النتائج وخفض مخاطر الوفاة، لأن درجات الحرارة المرتفعة يزيد مطالب الأيضية ويتأزم الاسكيمية الدماغي، ويزيد من فقدان الخلايا العصبية7. على الأقل 10 مليون عملية جراحية تجري سنوياً في الولايات المتحدة تتطلب الاحترار المريض نشطة لمنع انخفاض حرارة الجسم المحيطة بالجراحة دون قصد8. في غرفة العمليات، ينبغي الحفاظ على المرضى الذين يخضعون لجراحة درجة حرارة جسم أعلاه 36 درجة مئوية لتجنب عدد كبير من الآثار الضارة. غير المخطط لها من انخفاض في درجة حرارة الجسم قبل أو أثناء أو بعد الجراحة زيادة الدم الخسائر والإصابات ومستشفى طول فترة الإقامة، مما يضيف دولار 7,000 أو أكثر كل مريض إلى المستشفى تكاليف9،10،11 ،12.
رغم الحاجة السريرية كبيرة، درجة الحرارة الأكثر انتشارا التي تدار إدارة البروتوكولات تبين عدم كفاية الأداء أو الأخذ بمخاطر كبيرة للمريض. أجهزة السطحية (مثل البطانيات الماء وفرشات التوصيل، ويغطي الهواء القسري) مرهقة ومحدودة القدرة على نقل الحرارة، ويجب أن تلغي للسماح بالوصول إلى المريض للعناية بالمرضى والإجراءات. الأجهزة داخل الأوعية الغازية، من الصعب مكان، وتعرض المرضى للعدوى، والجلطات الدموية. فشل النهج القائمة لمنع انخفاض حرارة الجسم المحيطة بالجراحة غير مقصود للحفاظ على نورموثيرميا تصل إلى 70 في المائة من الوقت12،13،14،،من1516 وتحليل استعادي القلب بعد إلقاء القبض عليه تبريد وجدت هذا العام، 30 في المائة من المرضى الذين فشلوا في التوصل إلى درجة حرارة الهدف ضمن ح 617.
ويوفر نهج إدارة درجة حرارة المريض المريء مزايا كبيرة ل التكنولوجيات القائمة18. يحتفظ الجهاز إدارة الحرارة المريء وظيفة أنبوب المعدة عادة وضع في العناية المركزة والسكان المريض الجراحي. أنه يسمح لشفط المعدة المستمرة والضغط للغازات والسوائل أثناء إضافة القدرة على التحكم في درجة حرارة المريض بأمان وكفاءة بالاستفادة من بيئة تبادل الحرارة الملائمة المريء (الشكل 1). تعديل درجة حرارة يتحقق عن طريق توصيل الجهاز إدارة الحرارة المريء إلى أي من عدة الخارجية مبادلات الحرارة (تسمى أيضا المبردات) التي تستخدم مياه التبريد. إنتاج عدة بائعين متوافق مع مبادلات الحرارة التي تتوفر في المستشفيات للمحرك المنتجات مراقبة درجة الحرارة الحالية (في أغلب الأحيان من المياه والبطاطين). الممرضات أو الأطباء الممارسين ممرضة عادة بوضع جهاز إدارة حرارة المريء، ولكن يمكن أيضا إدراجها قبل أي مقدم لتدريبهم على وضع أنبوب أوروجاستريك قياسية. جهاز إدارة الحرارة المريء عدم تقييد الوصول إلى المريض ولا يلزم أن تكون عقيمة وتتجنب مخاطر إبرة عصا الإصابات بين مقدمي الخدمات وتتجنب مخاطر المضاعفات الجلد والتهابات مجرى الدم، وتجلط الدم في المريض. ولذلك، والغرض من هذا الأسلوب توفر طريقة بديلة منخفضة المخاطر للتحكم في درجة حرارة المريض في إعدادات غرفة التشغيل والرعاية الحرجة.
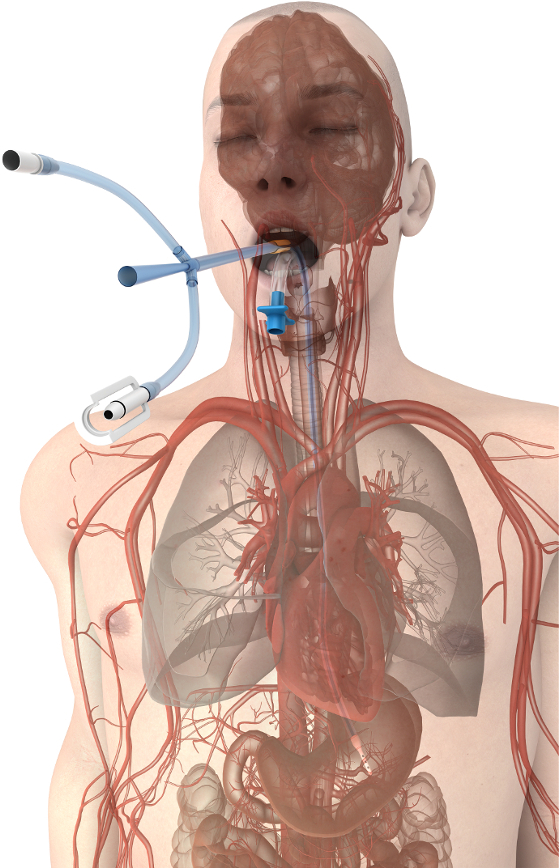
رقم 1. درجة حرارة البلعوم إدارة الجهاز التنسيب. قرب الجهاز من سفن كبيرة وقلب تشجيع نقل الحرارة كفاءة لب المريض. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
Protocol
Representative Results
Discussion
التعديل واستكشاف الأخطاء وإصلاحها لهذا البروتوكول يقتصر عموما على أن المواصفات أعلاه، وينطوي على رصد نموذجي لرعاية المرضى العاملين في الرعاية الحرجة. تحوير درجة الحرارة الأساسية حاسمة بالنسبة لنتائج المرضى في مجموعة متنامية من سيناريوهات السريرية. هذه تشمل تحريض متعمد من انخفاض درجة حرارة الجسم من نورموثيرميا، ريوارمينج من انخفاض حرارة الجسم غير مقصودة أو متعمدة، ونشاط المحافظة على درجة حرارة الجسم العادية (أي، نورموثيرميا) خلال ظروف في البرد غير المقصودة التي هي المشتركة، كما هو الحال في غرفة العمليات. كأمثلة محددة السريرية، المرضى الذين يعانون من الإصابة ضخه الاسكيمية، مثلما يحدث أثناء السكتة القلبية، تستفيد من التبريد (عموما إلى درجة حرارة أقل من درجة حرارة الجسم العادية) متبوعاً بمنع ريوارمينج وحمى لطيف ليصل إلى 3 بعد الإنعاش28،،من2930يوما. حديثي الولادة الذين يعانون من اعتلال الدماغ الاقفاري التاكسج الحصول على نتائج أفضل إذا يبرد تحت درجة حرارة الجسم الطبيعية31. التبريد للمانحين الكلي بعد وفاة العصبية، قبل زرع الأعضاء، قد ثبت للحد من معدل تأخر الاختلاس الدالة32. السيطرة على الحمى في مرضى الصدمة الانتانية قد خفض الاحتياجات فاسوبريسور وتسهم في تخفيض معدلات الوفيات المبكرة33. الحفاظ على نورموثيرميا في المرضى الذين يخضعون للعمليات الجراحية يقلل التهابات الجرح الجراحي ومضاعفات احتشاء عضلة القلب، وفقدان الدم، ومتطلبات نقل الدم، مع تقصير مدة الإقامة والحد من احتمال وفاة10 , 11 , 16.
وتشمل القيود أسلوب التحديات التي واجهتها في إدارة المرضى الرعاية الحرجة. بينما إدارة الحرارة هادفة تعزز نتائج جيدة، تقنيات تعديل درجة الحرارة الأكثر شيوعاً إدخال المخاطر للمرضى والتحديات اللوجستية لمقدمي الخدمات (بما في ذلك صعوبات في التوظيف، والتهابات مجرى الدم، وتجلط الدم، تلف الجلد، والتكلفة). إدارة الحرارة المريء يهدف إلى التغلب على هذه العيوب34،،من3536. عندما تدار بشكل مناسب، جهاز إدارة الحرارة المريء تتلامس مع عدم المفرج (كما تفعل درجة الحرارة داخل الأوعية الأجهزة التحوير) أو الجلد (كما تفعل أجهزة تعديل درجة الحرارة السطحية)، متجنبة بذلك تجلط الدم وعدوى مجرى الدم وتدهور البشرة. يمكن وضع الجهاز بسرعة بمجموعة متنوعة من مقدمي الرعاية الصحية، وعادة في غضون دقائق21،37. تقنية الإدراج يحاكي وضع أنبوب أوروجاستريك القياسية، مما يقلل من تعطل سير العمل التي قد تؤخر بدء العلاج. باستخدام نهج أساسية كما يبدو أن تشكل عبء يرتجف أقل إلى حد كبير من سطح النهج27،38،،من3940 . وهذا له ميزة تقليل المسكنات والأدوية المضادة يرتجف التكاليف، والتي ثم يقصر طول فترة الإقامة عن طريق الصحوة أسرع من درجة أدنى من التخدير مطلوب المرضى. هذه الميزات، نظرت في الحفل مع أداء السريرية المذكورة أعلاه، دعم إدارة الحرارة المريء كبديل ناجع لمقدمي الخدمات في قسم الطوارئ والعناية المركزة، وغرفة العمليات. وبالمثل تؤيد مجموعة متنامية من البيانات المنشورة على الجهاز هذا الجديد نهج21،،من2223،24،27،41.
وتشمل الخطوات الحاسمة في إطار البروتوكول بدء تدفق داخل الجهاز قبل الإدراج، توفير تزييت كاف للجهاز لضمان التنسيب السهل، أداء المص المعدة والضغط للسماح بالاتصال الحد الأقصى بين وقد وضع الجهاز والمريض، والتصدي لأي مريض يرتجف أن. عقب هذا البروتوكول وستوفر النتائج المثلى وتسمح بدرجة عالية من الأداء والسلامة في رعاية هذا السكان المريض مهم.
Disclosures
The authors have nothing to disclose.
Acknowledgements
لا شيء.
Materials
| EnsoETM | Attune Medical | ECD01 | Device compatible with Gaymar/Stryker Medi-Therm III and Stryker Altrix Precision Temperature Management System |
| EnsoETM | Attune Medical | ECD02 | Device compatible with Cincinnati SubZero Blanketrol II and Cincinnati SubZero Blanketrol III |
| Gaymar/Stryker Medi-Therm III | Stryker | n/a | Compatible heater-cooler with the ECD01 |
| Cincinnati SubZero Blanketrol II | Gentherm | n/a | Compatible heater-cooler with the ECD02 |
| Cincinnati SubZero Blanketrol III | Gentherm | n/a | Compatible heater-cooler with the ECD02 |
| Stryker Altrix Precision Temperature Management System | Stryker | n/a | Compatible heater-cooler with the ECD01 |
| Water-soluble lubricant | Various | n/a | Standard water-soluble lubricant used to ease insertion of tubes, catheters, and digits |
| Securement device | Various | n/a | E.g., Guard360 by PrimeGuard Medical |
References
- Chan, P. S., Krumholz, H. M., Nichol, G., Nallamothu, B. K. Delayed time to defibrillation after in-hospital cardiac arrest. N Engl J Med. 358 (1), 9-17 (2008).
- Callans, D. J. Out-of-Hospital Cardiac Arrest — The Solution Is Shocking. N Engl J Med. 351 (7), 632-634 (2004).
- Kochanek, P. M., Jackson, T. C. The Brain and Hypothermia-From Aristotle to Targeted Temperature Management. Crit Care Med. 45 (2), 305-310 (2017).
- Laupland, K. B., et al. Occurrence and outcome of fever in critically ill adults. Crit Care Med. 36 (5), 1531-1535 (2008).
- Diringer, M. N., Reaven, N. L., Funk, S. E., Uman, G. C. Elevated body temperature independently contributes to increased length of stay in neurologic intensive care unit patients. Critical Care Medicine. 32 (7), 1489-1495 (2004).
- Laupland, K. B. Fever in the critically ill medical patient. Critical care medicine. 37 (Suppl 7), S273-S278 (2009).
- Mathias, J. M. Hospitals to report on normothermia. OR manager. 25 (9), 22-24 (2009).
- Rajagopalan, S., Mascha, E., Na, J., Sessler, D. I. The effects of mild perioperative hypothermia on blood loss and transfusion requirement. Anesthesiology. 108 (1), 71-77 (2008).
- Kurz, A., Sessler, D. I., Lenhardt, R. Perioperative normothermia to reduce the incidence of surgical-wound infection and shorten hospitalization. Study of Wound Infection and Temperature Group. N Engl J Med. 334 (19), 1209-1215 (1996).
- Sessler, D. I. New surgical thermal management guidelines. Lancet. 374 (9695), 1049-1050 (2009).
- Young, V. L., Watson, M. E. Prevention of perioperative hypothermia in plastic surgery. Aesthet Surg J. 26 (5), 551-571 (2006).
- Hedrick, T. L., et al. Efficacy of protocol implementation on incidence of wound infection in colorectal operations. J Am Coll Surg. 205 (3), 432-438 (2007).
- Forbes, S. S., et al. Implementation of evidence-based practices for surgical site infection prophylaxis: results of a pre- and postintervention study. J Am Coll Surg. 207 (3), 336-341 (2008).
- Sun, Z., et al. Intraoperative core temperature patterns, transfusion requirement, and hospital duration in patients warmed with forced air. Anesthesiology. 122 (2), 276-285 (2015).
- Leary, M., et al. The association of body mass index with time to target temperature and outcomes following post-arrest targeted temperature management. Resuscitation. 85 (2), 244-247 (2014).
- Naiman, M., Shanley, P., Garrett, F., Kulstad, E. Evaluation of advanced cooling therapy’s esophageal cooling device for core temperature control. Expert Rev Med Devices. 13 (5), 423-433 (2016).
- Naiman, M., Markota, A., Hegazy, A. F., Dingley, J., Kulstad, E. Temperature Management in Critical Care and Burn Patients using an Esophageal Heat Transfer Device. Military Medicine. , (2017).
- Hegazy, A. F., Lapierre, D. M., Butler, R., Martin, J., Althenayan, E. The esophageal cooling device: A new temperature control tool in the intensivist’s arsenal. Heart Lung. , (2017).
- Hegazy, A. F., Lapierre, D. M., Butler, R., Althenayan, E. Temperature control in critically ill patients with a novel esophageal cooling device: a case series. BMC Anesthesiol. 15, 152 (2015).
- Bukovnik, N., Markota, A., Velnar, T., Rebol, J., Sinkovic, A. Therapeutic hypothermia and inhalation anesthesia in a patient with severe pneumococcal meningitis and secondary cardiac arrest. Am J Emerg Med. 35 (4), 665.e665-665.e666 (2017).
- Markota, A., Fluher, J., Kit, B., Balazic, P., Sinkovic, A. The introduction of an esophageal heat transfer device into a therapeutic hypothermia protocol: A prospective evaluation. Am J Emerg Med. 34 (4), 741-745 (2016).
- Markota, A., Kit, B., Fluher, J., Sinkovic, A. Use of an oesophageal heat transfer device in therapeutic hypothermia. Resuscitation. 89, e1-e2 (2015).
- Schroeder, D. C., et al. Oesophageal heat exchangers with a diameter of 11mm or 14.7mm are equally effective and safe for targeted temperature management. PLoS One. 12 (3), e0173229 (2017).
- Williams, D., et al. Use of an Esophageal Heat Exchanger to Maintain Core Temperature during Burn Excisions and to Attenuate Pyrexia on the Burns Intensive Care Unit. Case Reports in Anesthesiology. 2016, 6 (2016).
- Khan, I., et al. . 14th Annual Neurocritical Care Society Meeting. , (2016).
- HACA. Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med. 346 (8), 549-556 (2002).
- Bernard, S. A., et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. N Engl J Med. 346 (8), 557-563 (2002).
- Callaway, C. W., et al. Part 8: Post-Cardiac Arrest Care: 2015 American Heart Association Guidelines Update for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 132 (18 Suppl 2), S465-S482 (2015).
- Wyckoff, M. H., et al. Part 13: Neonatal Resuscitation: 2015 American Heart Association Guidelines Update for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 132 (18 Suppl 2), S543-S560 (2015).
- Niemann, C. U., et al. Therapeutic Hypothermia in Deceased Organ Donors and Kidney-Graft Function. N Engl J Med. 373 (5), 405-414 (2015).
- Schortgen, F., et al. Fever control using external cooling in septic shock: a randomized controlled trial. Am J Respir Crit Care Med. 185 (10), 1088-1095 (2012).
- Reccius, A., Mercado, P., Vargas, P., Canals, C., Montes, J. Inferior Vena Cava Thrombosis Related to Hypothermia Catheter: Report of 20 Consecutive Cases. Neurocrit Care. 23 (1), 72-77 (2015).
- Maze, R., et al. Endovascular cooling catheter related thrombosis in patients undergoing therapeutic hypothermia for out of hospital cardiac arrest. Resuscitation. 85 (10), 1354-1358 (2014).
- Simosa, H. F., Petersen, D. J., Agarwal, S. K., Burke, P. A., Hirsch, E. F. Increased risk of deep venous thrombosis with endovascular cooling in patients with traumatic head injury. Am Surg. 73 (5), 461-464 (2007).
- Kulstad, E., et al. Induction, maintenance, and reversal of therapeutic hypothermia with an esophageal heat transfer device. Resuscitation. 84 (11), 1619-1624 (2013).
- van Zanten, A. R., Polderman, K. H. Blowing hot and cold? Skin counter warming to prevent shivering during therapeutic cooling. Crit Care Med. 37 (6), 2106-2108 (2009).
- Tommasi, E., et al. Cooling techniques in mild hypothermia after cardiac arrest. J Cardiovasc Med. , (2014).
- Diringer, M. N. Treatment of fever in the neurologic intensive care unit with a catheter-based heat exchange system. Crit Care Med. 32 (2), 559-564 (2004).
- Hegazy, A. F., Lapierre, D. M., Butler, R., Martin, J., Althenayan, E. The esophageal cooling device: A new temperature control tool in the intensivist’s arsenal. Heart Lung. 46 (3), 143-148 (2017).

