Optogenetisk manipulation av neuronal aktivitet för att modulera beteende i fritt rörliga möss
Summary
Med optogenetisk manipulation av specifika neuronala populationer eller regioner hjärnan, beteende kan ändras med hög tidsmässiga och rumsliga upplösning i fritt rörliga djur. Genom att använda olika optogenetiska verktyg i kombination med kroniskt implanterade optiska fibrer kan en mängd neuronal modulationer och beteendetestning utföras.
Abstract
Optogenetiska modulering av neuronal kretsar i fritt rörliga möss påverkar akut och långsiktigt beteende. Denna metod är i stånd att utföra manipulationer av enstaka nervceller och region-specifika sändare release, upp till hela neuronala kretsar i centrala nervsystemet, och möjliggör direkt mätning av beteendemässiga resultat. Nervceller uttrycker optogenetiska verktyg via en injektion av virala vektorer som bär DNA val, såsom Channelrhodopsin2 (ChR2). Ljus förs in i specifika hjärnregioner via kroniska optiska implantat som slutar direkt över målregionen. Efter två veckors återhämtning och korrekt verktyg-uttryck, möss kan upprepade gånger användas för beteendemässiga tester med optogenetisk stimulering av nervceller av intresse.
Optogenetiska modulation har en hög tidsmässig och rumslig upplösning som kan åstadkommas med hög cell specificitet, jämfört med de vanliga metoder som kemisk eller elektrisk stimulering. Ljuset skadar inte neuronal vävnad och kan därför användas för långsiktiga experiment samt för flera beteendeexperiment i en mus. Möjligheterna med optogenetiska verktyg är nästan obegränsade och möjliggör aktivering eller ljuddämpning av hela nervceller, eller till och med manipulering av en specifik receptortyp av ljus.
Resultaten av sådana beteendeexperiment med integrerad optogenetisk stimulering visualiserar direkt förändringar i beteende som orsakas av manipulationen. Beteendet hos samma djur utan ljusstimulering som en baslinje är en bra kontroll för inducerade förändringar. Detta möjliggör en detaljerad översikt av neuronala typer eller signalsubstanssystem som är involverade i specifika beteenden, såsom ångest. Den plasticitet av neuronala nätverk kan också undersökas i stor detalj genom långsiktig stimulering eller beteendemässiga observationer efter optisk stimulering. Optogenetik kommer att bidra till att upplysa neuronal signalering i flera typer av neurologiska sjukdomar.
Introduction
Moduleringen av neuronala kretsar i centrala nervsystemet och deras beteendemässiga resultat är viktiga för att förstå hur hjärnan fungerar, särskilt vid psykiatriska sjukdomar och kognitiva uppgifter som inlärning och minne. Med optogenetik kan enstaka celler eller cellpopulationer upp till hela kretsar moduleras av ljus. Vanliga optogenetiska verktyg som Channelrhodopsin2 (ChR2) eller Archaerhodopsin (Arch) kan aktivera eller tysta nervceller, eller öka eller hämma sändarutgåvan vid axonterminaler som projicerar till distinkta hjärnregioner1,2,3,4. Dock måste Arch användas försiktigt eftersom det visades att dess aktivering vid presynaptiska terminaler ökar spontan sändare release5. Arch är en utåt rättande protonpump som ändrar pH-värdet inuti cellen. Denna alkaliska miljö inducerar kalciumtillströmningen och förbättrar sändarutgåvan5. För att specifikt modulera intracellulära signalvägar, receptor chimeras består av ett ljus aktiveras optogenetiskt verktyg, såsom rhodopsin eller kon opsin, i samband med en adekvat G-protein kopplade receptor, kan skapas6,7,8. Mängden och variationen av optogenetiska verktyg som finns har ökat betydligt under det senaste decenniet9.
Syftet med optogenetik är att manipulera neuronal kretsar under beteende. Optogenetik möjliggör till exempel mätning av akuta beteendeförändringar såsom förändringar i ångestbeteende. Optogenetiska verktyg levereras till målregioner i hjärnan via virala vektorer. Med hjälp av särskilda tillskyndare och förstärkare, eller Cre-loxP-systemet, kan man säkerställa celltypsspecialitet för uttrycket av optogenetiska verktyg (Figur 1A). Det finns flera genetiskt modifierade muslinjer som uttrycker enzymet Cre-Recombinase i specifika celltyper endast. Till exempel, Nex-Cre möss uttrycka Cre-Rekombinas i pyramidala nervceller i cortex och hippocampus under kontroll av Nex-promotor10. Detta enzym är kompetent att invertera DNA-ordnar, som flankeras av loxP-sidor11. Följaktligen kan DNA-sekvensen av en dubbel-floxed optogenetiska verktyg, som är inverterad och flankerad av loxP sidor, endast transkriberas av nervceller som besitter Cre-Rekombinas, men inte av andra neuronala typer12,13. När det gäller Nex-Cre-möss kommer det optogenetiska verktyget enbart att uttryckas i pyramidala nervceller. Ljusstimulering av vissa hjärnregioner uppnås sedan via kronisk implantation av optiska fibrer direkt ovanför den region av intresse. Djur kan sedan kopplas till en lämplig ljuskälla och fritt bete sig i nästan alla typer av beteendemässiga tester.
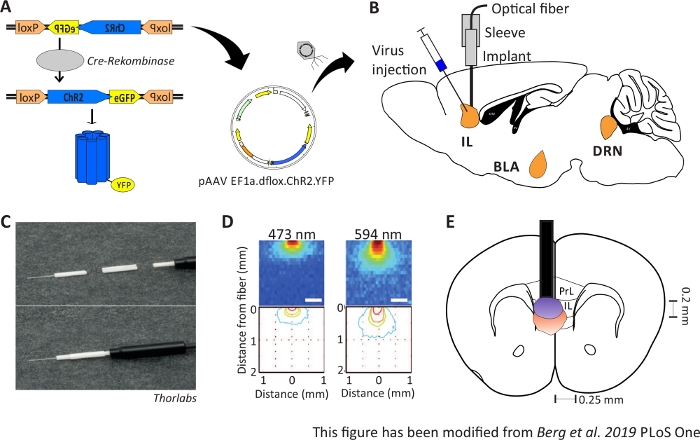
Bild 1: Injektion och implantation. A) Cre-loxP-system för ChR2-YFP. Dubbel floxed optogenetiska verktyget är förpackad i en adeno associerade virus (AAV) för injektion i hjärnvävnaden. B) Sagittal syn på virusinjektionen och implantationen av ett optiskt neuronalt gränssnitt in i/ovanför IL-regionen i mPFC. Injektion och implantation gjordes ovanifrån. Alla regioner av intresse, IL, BLA och DRN, visas. C) Detaljerad vy över den implanterade optiska fibern, hylsan och ljuskällan. D) Spridning av blå och röd laserljusstimulering i grå substans hjärnvävnad från en 200 μm ljusfiber (Yizhar et al. 2011). Blått ljus sprider sig, vid maximum, 0,5 mm in i vävnaden, rött ljus ca 1 mm. Färgkodning: röd 50%, gul 10%, grön 5%, blå 1% om ljus når detta område. E) Koronal syn på den ensidiga implantationen direkt ovanför vänster IL med en optisk fiber på 200 μm. IL-regionen har en bredd på 0,25 mm på varje halvklot och ett djup på 0,2 mm. Blå och röda glödlampor är boarder av 5% ljus spridning och överförs från Yizhar et al till rätt storlek. LoxP: locus av X-over P1; ChR2: Channelrhodopsin; YFP: gult fluorescerande protein; dflox: dubbel floxed; IL: infralimbic cortex; BLA: basolateral amygdala; DRN: dorsala raphe kärnor; PrL: prelimbic region. Denna siffra har ändrats från Berg 201948. Vänligen klicka här för att visa en större version av denna figur.
Optogenetiska tillvägagångssätt utnyttjas eftersom det möjliggör både hög tidsmässig och rumslig upplösning14 och celltyp specifik modulering. Dessutom är det möjligt att upprepat använda den implanterade enheten utan ytterligare behandling. Efter en stereotaktisk kirurgi, där injektionen av ett adeno-associerat virus som bär på det optogenetiska verktyget och implantationen av den optiska fibern utförs, kan möss återhämta sig i två veckor. Vi har valt en återhämtningstid på endast 2 veckor, eftersom detta är tillräckligt med tid att återhämta sig från operationen och för viruset att uttrycka. Eftersom beteendeexperimenten följs av immunohistokemi måste vi se till att möss inte blir för gamla under experimentet; annars minskas vävnadskvaliteten. De visar inga uppenbara beteendemässiga funktionsnedsättningar från implantatet och engagera sig i typiska bur beteende. Naturligtvis är implantationen åtföljd av en betydande kirurgisk lesion; därför övervakas mössen intensivt. Efter operationen måste möss enstaka inhysas, eftersom grupphusmöss tenderar att skada varandras färska sår och implantat. Men bostadsförhållanden har en stor inverkan på ångestnivån hos manliga möss, som enda inrymt möss visar lägre ångest nivåer15 och i allmänhet mindre depressiva-liknande symtom16.
Kemisk eller elektrisk manipulation av hjärnkretsar saknar optogenetikens höga celltypssärkalitet och har en lägre tidsmässig och rumslig upplösning14,17,18. Beroende på den experimentella frågan kan elektrisk eller kemisk stimulering ha olika fördelar. När passerar fiber terminaler i en specifik region måste också stimuleras, elektrisk stimulering är den bästa metoden. Kemisk stimulering är ett bra val för när sändarspecifika receptorer i en hel region ska aktiveras av agonister. En annan stor fördel med optogenetik jämfört med kemisk eller elektrisk stimulering är att endogent, nervceller är inte känsliga för ljus, som undviker förekomsten av biverkningar19. Faktum är att höga ljusintensiteter kan inducera värmeeffekter8,20, men på grund av rätt kontrollgrupper, de beteendemässiga effekter på grund av optogenetisk manipulation kan elimineras.
Undersökande gnagare beteende, särskilt i fråga om psykiatriska sjukdomar, har kraftigt förbättrats med optogenetik i fritt rörliga djur, eftersom det möjliggör direkt modulering av enstaka receptorer upp till specifika cellpopulationer21 och kretsar22. Möjligheten att mäta de akuta effekterna av sådana modulationer, liksom de långsiktiga beteendeeffekterna efter en definierad tid23 eller efter kroniskstimulering 24, möjliggör en bred flexibilitet av experimentella konstruktioner och ger mycket detaljerade insikter i hjärnkretsar. Ljusstimulering kan användas för att modulera nervceller som finns vid injektionsstället för det optogenetiska verktyget. När både injektion och implantation adress samma hjärnregionen, cell organ och tillbaka projicera axons av princip nervceller och interneurons i denna region kan riktas3,6,8. Men, den lätta fibern kan också implanteras i en region som skiljer sig från den injicerade. I detta fall kan ljusstimulering modulera sändarutgåva vid axonterminaler i projektionsområdena i den injicerade regionen25,26,27.
I studien här används optogenetik i kombination med experiment för att analysera ångestrelaterat beteende. Ångestrelaterade psykiatriska sjukdomar drabbar mer än en tredjedel av världens befolkning28,29,30 och orsakar en hög ekonomisk börda31. De som drabbas lider av en känsla av upphetsning, spänning och oro följt av undvikandebeteende 32,33. Dessa kroniskt förekommande negativa känslor, som huvudsakligen är inriktade på framtida händelser34, starkt störa det dagliga livet för patienter. Vanliga behandlingar som bensodiazepiner eller selektiva serotoninåterupptagshämmare (SSRI) är endast framgångsrika hos några av patienterna. En stor mängd människor svarar inte på behandlingen alls35, visar att den mekanism som ligger bakom sådana sjukdomar är ännu inte helt klarlagt. Den mediala prefrontala cortex (mPFC) är känd för att spela en viktig roll i utvecklingen och manifestation av ångest21,25,27,36,37,38. Specifikt kan överaktiveringen av den infralimbic cortex (IL) regionen i mPFC vara en del av ångest-relaterade sjukdomar39,40. Exemplet experimentet som beskrivs här skulle kunna bidra till att förstå hur modulationer i regionen IL i mPFC påverka ångest beteende. Dessutom kan utvecklingen av nya terapeutiska strategier för ångestrelaterade psykiatriska sjukdomar också potentiellt stödjas.
2-6 månader gamla manliga Nex-Cre möss används för att uttrycka ChR2 specifikt i pyramidala nervceller inom IL regionen av mPFC41. Nex-Cre möss har en C57Bl/6 bakgrund och uttrycka enzymet Cre-rekombinas specifikt i pyramidala nervceller. Under en stereotaktisk kirurgi injiceras dubbel floxed ChR2-DNA i IL-regionen via adeno associerade virala vektorer. Det optiska implantatet placeras direkt ovanför den region av intresse (Figur 1B) och implantatet är fast med tandcement. Kontroll djur får en injektion av dubbel floxed tdTomato-DNA i samma region att efterlikna cell specifika uttryck.
Djur är grupphus fram till operationsdagen och efteråt är enda inrymt för att undvika skador från andra möss. Möss är inhyst i enskilda ventilerade bur (IVC) rack i TypI-L burar för enkelhus möss. Den ljus-mörka cykeln följer en 12:12 h rytm, den ljusfas som börjar vid 10 AM. Alla beteendeexperiment utförs i den mörka fasen, som liknar den aktiva fasen av gnagare. Vatten och standardmatpellets finns ad libitum. Efter två veckors återhämtning, vilket säkerställer ett tillräckligt uttryck av ChR2 i pyramidala nervceller, används möss för beteendeexperiment.
Öppet fält (OF) är en 50 cm x 50 cm i kvadrat labyrint med sandblästrat 40 cm höga väggar. Marken är uppdelad i 16 rutor där den inre 4 representerar centrum. Det uppmätta beteendet är: 1) tid som tillbringas i centrum, 2) antal mittposter och 3) totalt avstånd flyttas. Under detta experiment, det finns 4 försök totalt 20 minuter. I försök 1 och 3 sker ingen ljusstimulering, och i försöken 2 och 4 utförs en 20 Hz-stimulering med 5 ms ljuspuls och 1 mW ljusintensitet på 473 nm (Figur 2A). I de senare försöken beaktades tillvänjning till testområdet, men användningen av skeninsprutade kontrolldjur anger hur tillvänjning uttrycks.
Barnes maze är ett experiment för inlärning och minne. Det är en cirkulär plattform som är 92 cm i diameter och innehåller 20 ekvidsliga hål runt omkretsen. 19 av hålen är stängda och under ett hål presenteras en utrymningsbox. För 4 dagar i följd har möss 4 träningsförsök för att lära sig platsen för utrymningslådan. På den5:e dagen tas utrymningsrutan bort, och möss testas på hur mycket tid de behöver för att hitta rätt hål. Det uppmätta beteendet är: 1) Tid tills utrymningsrutan/rätt hål hittas, 2) Antal målbesök och fel, och 3) Avstånd flyttat tills i utrymningsrutan. Ljusstimuleringen i olika grupper görs antingen under förvärv eller konsolidering, som sker på träningsdagarna 1-4, eller under hämtning på testdagen, som är dag 5 (Figur 2D).
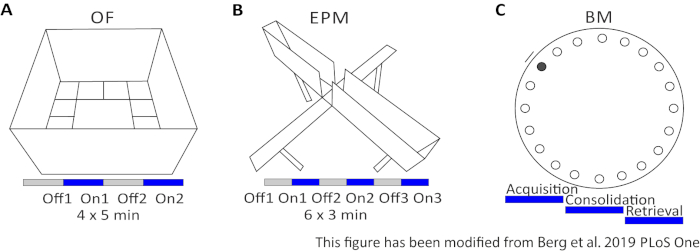
Figur 2: Beteendeexperiment med optogenetiska protokoll. A) Schematisk ritning av Open Field-experimentet med motsvarande ljusstimuleringsprotokoll. C) Schematisk ritning av Elevated-Plus Maze-experimentet med motsvarande ljusstimuleringsprotokoll. D) Schematisk ritning av Barnes Maze-experimentet med motsvarande ljusstimuleringsprotokoll. EPM: Förhöjd-Plus-labyrint; AV: Öppet sätta in; BM: Barnes labyrint test. Denna siffra har ändrats från Berg 201948. Vänligen klicka här för att visa en större version av denna figur.
För optogenetisk stimulering måste ljusintensiteten och frekvensen anpassas till det optogenetiska verktyg och neuronal typ som är under utredning. Lägsta möjliga ljusintensitet bör användas för att undvika skador på vävnaden, eftersom flera studier har visat att det finns möjliga uppvärmningseffekter på grund av stark ljusintensitet8,20. För ChR2 används vanligen en 20 Hz-stimulering med en 5 ms ljuspuls2. Som ChR2 är ganska ljuskänslig, är 1 mW ljusintensitet tillräcklig. Ljusstimuleringsprotokollet växlar mellan ljus från och på försök för att direkt mäta beteendeförändringar. De yttre rumsförhållandena för beteendeexperiment bör förbli stabila för hela gruppen av djur. Viktiga förutsättningar att tänka på är bullret (tänk på att enheterna själva kan göra ljud), lukten (rengör alltid beteendeuppställningarna med etanol), ljusintensiteten och experimentören. Försökspersonen ska alltid vara samma person. Dessutom bör tiden på dagen för experimenten vara densamma för alla djur i en grupp, några timmar efter starten av den mörka fasen i anläggningen är att föredra.
Målet med detta experiment är att öka excitation/ hämning (E / I) förhållandet i IL regionen genom stark aktivering av excitatoriska pyramidala nervceller. En förbättrad E / I-förhållande i denna speciella cortex regionen är känt för att öka ångest nivåer hos möss40,42,43,44.
Protocol
Representative Results
Discussion
Använda ljus för att manipulera neuronal signalering har varit metoden för val för nästan ett decennium nu. Sedan 2005, antalet publicerade artiklar om utvecklingen av nya optogenetiska verktyg 4,6,8,8,14,49,50,51 och studier där sådana verktyg utnyttjas för att undersöka hjärnkretsar21,23,40,43,52, kraftigt ökat. Å ena sidan, med den enorma mångfalden av injicerbara optogenetiska verktyg, implantationsvarianter, transgena muslinjer och beteendeexperiment, är möjligheten till experiment mångfald och obegränsad. Å andra sidan är möjligheten att göra fel i valet av experimentella förhållanden mycket hög och experimenten är så specifika, att ofta är jämförbarheten med andra studier svår.
Kritiska steg
Ett viktigt kritiskt steg i detta protokoll är korrekt planering. Valet av det optogenetiska verktyget bör matcha den vetenskapliga frågan. Är det bara nödvändigt att manipulera den totala aktiviteten hos en neuron eller synaps? Sedan kommersiellt tillhandahållna verktyg som ChR221,25,27 och Arch37 är ett bra val. Men bortsett från det, om en speciell signalsubstans system eller ens en enda receptor bör manipuleras, en individuell receptor chimera är ofta det bättre valet3,6. Flera receptor chimärer med GPCRs, den så kallade Opto-XRs, och riktlinjer för att producera dem finns redan4,50. Andra än valet av optogenetiska verktyg, muslinjen i kombination med beteendeexperimentet är också kritisk. Olika bakgrundsstammar, som till exempel C57Bl/6 och BALB/cByJ, visar olika beteendemässiga fenotyper i vissa avseenden53,54. C57Bl/6-möss har en låg baslinjeångest och kan användas för ångestdämpande manipulation, medan BALB/cByJ uppvisar högre ångestnivåer och därför är mer känsliga för ångestdämpande läkemedel. Dessutom kan de transgena varianterna av dessa bakgrundsstammar också variera i sin fenotyp48. Med en korrekt kombination av specifika initiativtagare i samband med ett optogenetiskt verktyg och transgen muslinje, kan nästan varje önskad cellpopulation riktas.
Ett kritiskt steg under operation riktar sig till rätt plats. Med hjälp av musen hjärnan atlas, korrekt koordinater för den främre-posterior axeln, och mediala-laterala axeln, och djup av strukturen kan upprättas45. I verkligheten har varje skalle en något annorlunda form och storlek. Således är F-faktor46 för att justera stereotaktiska koordinaterna ganska viktigt, liksom korrekt näsa och öra fixering under stereotaktisk kirurgi. Om musens huvud lutas, kommer injektionsbyulan att misslyckas med att rikta den önskade regionen av intresse.
Dessutom är injektionsbygelns diameter också kritisk. Om den är för liten kan inget virus släppas ut i vävnaden, om den är för bred kommer kanylen att läcka viruslösning på väg till intresseområdet. Om den implanterade optiska fibern upphör direkt över målregionen spelar virusuttrycket i cortexregionerna ovan ingen roll. Men om implantatet placeras över andra regioner för att stimulera axonterminaler, kommer axoner i övre hjärnbarken regioner också aktiveras av ljus och förfalska erhållna data. Som ett exempel: IL-regionen och den prelimba (PrL) regionen både projektet till den basala amygdala55,56 men har helt olika funktioner och roller i moduleringen av ångest26,57. Om implantatet placeras ovanför amygdala för att aktivera axonterminaler från IL-regionen, och under injektionsviruslösningen också placerades i PrL på grund av fel injektionskanula, är risken för att även aktivera axonterminaler från PrL mycket hög.
Under beredningen av skallen för fixering av implantatet är den glesa användningen av primer och bindning avgörande för en tillförlitlig och hållbar fixering. Om 2-komponenten vidhäftningssystemet inte appliceras tunt, kan tandcement lossna från skallen efter ett par dagar eller veckor. Dessutom måste skallen också torkas helt innan implantatet fixeras, eftersom cementen annars inte kommer att fästa ordentligt på skallen.
Kritiska steg finns också i beteendedelen av det här protokollet. Först är byggandet av labyrinten mycket viktigt. I varje beteendemässiga setup, finns flera varianter i litteraturen angående storlek och form, liksom för själva förfarandet58,59,60. Det är viktigt att välja en variant som gör uppgifterna jämförbara och reproducerbara. Också, särskilda krav för utnyttjade muslinjer bör beaktas43,48. I de representativa uppgifterna för EPM kan man se att flera Nex-Cre-möss föll från labyrinten eller halkade av flera gånger (Figur 2b). För dessa möss, en labyrint med en liten vägg runt de öppna armarna skulle ha varit ett bättre alternativ.
För det andra är det viktigt att hålla alla yttrerumsförhållanden konstant 61, annars skulle olika grupper av möss inte vara jämförbara alls. I detta avseende är det mycket viktigt att välja tidpunkten för experimentet som en där den experimentella setup är ledig och experimentören är alltid närvarande. Vidare bör händelser i byggnaden, såsom byggnadsarbeten, provning av eventuella system (brandlarm) eller rengöringsdagen för musanläggningen, övervägas för att undvika störningar i erhållna data.
Slutligen, hantering och bostäder villkor är avgörande för beteendemässiga experiment. När en implantation utförs, möss måste vara singel inrymt på grund av risken för skador från andra möss. För att säkerställa god jämförbarhet mellan grupper och ett lågt fel inom en grupp, måste varje mus ha samma burstorlek och berikning. För ångest-relaterade experiment, enda bostäder har vissa fördelar som singe inrymt manliga möss visar en lägre baslinje ångest nivå, mindre variation i deras ångest nivå, och mindre depressiva-liknande symtom15,16. Grupp inrymt manliga möss kan starkt skilja sig i sin ångest nivå på grund av hierarkin bland mössen. Förutom bostäder, en konstant och lika hantering av alla möss och grupper är också viktigt. Att ta tag i musen för att kunna koppla ihop ljusfibern på implantatet är mycket stressande. Därför måste denna procedur vara densamma för varje mus, vilket betyder samma teknik och samma experimenter. Dessutom måste tillvänjningstiden i vänteburen, som är tänkt att lugna ner musen från det stressiga anslutningsproceduren, också ha lika förhållanden i varaktighet, kull och position till labyrinten. Hanteringen inom musanläggningen är också avgörande för senare beteendeprestanda. Försöks- och kontrolldjur bör inte rengöras på olika dagar eller av olika människor, eftersom detta också är påfrestande för möss. Dessutom bör rengöringsdagen inte vara den experimentella dagen för att undvika skillnader i beteende.
Felsökning
Det finns flera problem som kan uppstå under protokollet. Till exempel, borrning en hel i skallen under stereotaktisk kirurgi kan skada blodkärlen. Vanligtvis uppträder stark blödning, särskilt ovanför bregma och lambda. Om detta händer, försök inte att stoppa blödningen med bomullspinnar eftersom de tenderar att förlänga ännu mer blödning ur kärlet på grund av deras absorbens, istället, direkt skölj med NaCl.
Det kan också hända att tryckinjektionen av viruslösningen inte fungerar. I det här fallet kan det vara så att parafilm, en sårskorpa från burrhålet eller hjärnvävnaden, täpper igen kanylens spets. I detta fall, ta bort kanylen långsamt ut ur hjärnan utan att ändra x- eller y-axeln och använd en pincett för att ta bort 1-2 mm av den främre delen av kanulaspetsen. Innan du sänker kanylen igen, testa för funktionalitet genom att applicera liten mängd tryck för att se om virus kommer ut ur kanulaspetsen. För att undvika förstoppning, sänk kanylen med en konstant hastighet och stoppa inte rörelsen förrän injektionssidans djupaste djup har uppnåtts. Om för mycket av kanylspetsen avlägsnas och diametern är för stor kommer kanylen att skada vävnaden och risken att applicera viruset på en gång kommer att ökas. Se således till att endast den igensatta delen av spetsen avlägsnas försiktigt.
Under beteendeexperimentet kan inställningen av experimentet i videospårningsprogrammet (t.ex. Ethovision XT) orsaka problem. Om ljusutmatningen till exempel inte fungerar som den ska kan detta bero på flera orsaker. Pulser måste öppnas, programmeras och startas innan Ethovision XT öppnas. Maskinvaran behöver väljas korrekt i “Experimental setup” (steg 3.2.2.4). Om fel IO-Box, eller något annat än “Costume Hardware” är valt, kan Pulser-enheten inte styras av Ethovision. Om testet av ljusutgången lyckas, men det programmerade ljusprotokollet i “Inställningar för kontroll av försök” inte fungerar under anskaffningen, kanske underregeln eller underregelreferensen finns felaktigt eller villkoren och åtgärderna är oklara. Till exempel: tillhör referensen rätt underregel? Är referensen korrekt programmerad (t.ex. hur ofta utförs underregeln)?
Dessutom kan det hända att under “detektionsinställningar” djuret spåras tillräckligt, men under förvärvet finns det prover där ämnet inte hittas. I det här fallet, kontrollera om belysningen i experimentrummet var förändrat, eller om något producerade oönskade skuggor i labyrinten. Hela botten av labyrinten måste ha samma färg, eftersom inställningen bara kommer att fungera för en specifik kombination. Om av någon anledning olika botten färger eller skuggor inte kan undvikas, definiera detektionsinställningen i den mörkaste delen av labyrinten.
För att ändra eventuella inställningar efter förvärvet av de första djuren, tillämpa inte dessa ändringar i de redan använda inställningarna. Duplicera dem för att justera dem. Detta innebär också att den redan registrerade rättegången inte är giltig längre för dataanalys. I ett sådant fall, spela in alla djur för denna experimentella grupp med de ursprungliga inställningarna, och skapa ett nytt experiment efteråt där de inspelade videorna analyseras i stället för livespårning. I detta “från video”-experiment kan flera inställningar användas för analys utan att förlora jämförbarheten mellan djur eller ens data.
Begränsningar och framtida tillämpningar
Denna metod att manipulera beteende med optogenetik i fritt rörliga djur inkluderar också begränsningar. Under operationen är närheten till de två implantaten begränsad. För dubbel implantation måste avståndet mellan de två implantaten minimalt vara bredden på apparaten för att hålla implantatet. Apparaten måste sänka det andra implantatet i burrhålet, medan de första implantaten redan är fixerade. En lösning för detta kan vara en vinklad implantation, där glasfiberns spetsar kan vara mycket nära medan de keramiska ferulesna ovanför skallen har störreavstånd 23,55,56,57,62,63. En nackdel med en vinklad implantation är ljuset sprider sig. När fiberspetsen är snedställd istället för rakt ovanifrån är det stimulerade området annorlunda. Vid två målregioner i nära anslutning behöver den ändrade positionen för ljusstimuleringen beaktas.
Under beteendeexperimentet kan labyrintens konstruktion störa den optiska kabeln som är ansluten till djuret. Vissa beteendetester, som den ljus-mörka lådan, innehåller ettinomhusområde 64,65, och andra labyrinter innehåller fack som musen behöver ange. Sådana experiment kan inte utföras med den här inställningen. Alternativt kan ett trådlöst system vara ett alternativ22,26,66. Men lyckligtvis vissa labyrinter, såsom Barnes Maze, kan ordnas på ett sådant sätt, att mössen kan komma in i relevanta fack67.
Förutom de med slutna zoner, labyrinter som är för breda kan orsaka också problem. Ju större område i labyrinten, desto längre kabel måste vara att låta djuret att gå till varje position i labyrinten. Försiktighet måste vidtas att djuret inte kan trampa på kabeln eller ta tag i den och bita den. En lösning för det kan vara en konstruktion som rullar upp den överflödiga kabeln. En nackdel är att dra för att rulla kabeln är svårt för möss. Denna lösning skulle bättre lämpad för råttor. Ett annat möjligt alternativ skulle kunna vara att göra ljusstimuleringen i förväg, istället för under försöket, naturligtvis är detta endast möjligt om en långsiktig effekt på grund av den lätta stimuleringensker 23.
Jämförelse med befintliga/alternativa metoder
Alternativa metoder skulle vara kemisk eller elektrisk stimulering underbeteende 8,18. Kemiska agonister eller antagonister har möjlighet att aktivera eller tysta nervceller via specifika receptorer och kan också manipulera enstaka signalsubstanssystem38,68. På ena sidan är receptor-specificiteten ganska hög för kemikalier, eftersom specifik agonist eller antagonist bara aktiverar vissa receptorer39. Å andra sidan är specificiteten för receptorsubtyper av samma neurotransmittorgrupp ofta otillräcklig. De flesta kemikalier binder till minst två undertyper med olika sannolikheter69. Dessutom, kemikalier kan inte skilja mellan neuronala celltyper så länge de har samma receptortyper. Utöver detta är tidsmässig och rumslig upplösning dålig för kemiska manipulationer i jämförelse med optogenetik. Agonister eller antagonister administreras ofta oralt35 eller via systemiska injektioner57,70. Om infusionen av kemikalien sker direkt i hjärnvävnaden, visas effekter snabbare än med orala tillämpningar, men fortfarande på en långsammare tidsskala än med ljusstimulering. Som de administrerade kemikalierna diffusa i hjärnan och är inte specifika för neuronala typer eller regioner hjärnan, manipulation av specifika hjärnkretsar det inte möjligt.
Elektrisk stimulering har en högre temporal upplösning än kemiskstimulering 9,14. Spridningen inom i neuronal vävnad är mindre än med kemisk stimulering och den rumsliga upplösningen är bättre än med kemisk stimulering. Emellertid, elektrisk stimulering saknar möjlighet att specifikt ta itu med olika neuronala celltyper eller receptortyper, som varje neuron i närheten av elektroden kommer att svara på den elektriska stimulering.
Alternativa metoder till uppförandet i fritt röra möss är for example electrophysiological inspelningar i hjärnsegment, var singel- neurons eller axons kan moduleras med optogenetics och elicited verkställer kan mätas via inspelningelektroder6,71. In vitro-experiment ger möjlighet att undersöka den molekylära och cellulära grunden för optogenetiska stimulering men har den begränsningen att inneboende anslutning och input från andra hjärnregioner saknas. Ett annat alternativ är att använda optogenetisk i samband med multiphotonbildbehandling 1,72. I det här fallet har möss huvudet fast och kan sövas eller vara vaken för att lösa enkla uppgifter.
För att utföra ett framgångsrikt optogenetiskt experiment finns ett brett utbud av verktyg och applikationer nuförtiden. Valet av optogenetiska verktyg och beteendemässiga set-up är avgörande för att besvara specifika forskningsfrågor. Om rätt kombination av verktyg och experiment väljs, optogenetik tillåter en aldrig tidigare skådad, djupgående undersökning av neuronala kretsar med hög tidsmässiga och rumsliga upplösning. Detta kommer att bidra till att förstå och utveckla nya terapeutiska strategier för psykiatriska sjukdomar och kognition.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Stort tack till prof Klaus-Armin Narve och Dr Sandra Goebbels (Max-Plank-Institute of Experimental Medicine, Goettingen, Tyskland) för vänligt tillhandahållaNde Nex-Cre möss. Också, Vi tackar vår video-team Yunus Dikici och Ruben Wiesner för inspelning och bearbetning av JoVE video för den här artikeln. Dessutom, stort tack till Kristin Claussen för hennes voice-over och Kimberly Anne Go för korrekturläsning av manuskriptet.
De presenterade resultaten erhölls vid Ruhr-universitetet i Bochum och videon spelades in vid universitetet i Bremen.
Detta arbete finansierades av Deutsche Forschungsgemeinschaft (DFG, Tyska forskningsstiftelsen) – Projektnummer 122679504 – SFB 874 och DFG MA 4692/3-2.
Materials
| Ketamin | Sigma-Aldrich | K2753-64 | Anestasia |
| 20 % Glucose | AlleMan Pharma | Injection s.c. for fast recovery | |
| Behavioral mazes | Costum made | Measure anxiety | |
| Bepanthen | Bayer | Ophthalmic oinment | |
| Betaisodona | Monodipharma | Sterilant containing iodine | |
| Betaisodona | Monodipharma | Iodine oinment | |
| Binocular | Olympus | SZ52, 110AL0.62x WD160 | Surgery |
| Ceramic ferrules | Thorlabs | CFLC230-10 | Implant |
| Ceramic Fiber Scribe | Thorlabs | CSW12.5 | Cutting of the glass fiber |
| Channelrhodopsin2-YFP virus | Penn Vector Core | Addgene 20298 | Optogenetic tool |
| Compressed air | Kontakt Chemie | Druckluft 67 | Drying of the skull |
| Coordinate system | Stoelting | Stereotactic coordinates for the surgery | |
| Correl Draw | Graphical software version 13 | ||
| Cryoslicer | MICROM | HM500OM | Production of brain slices for staining |
| Ethovision XT 14 | Noldus | Software for behavioral tracking | |
| Exel | Statistical Software | ||
| Ferrule Polishing Puck | Thorlabs | D50-F | Polishing implants round side |
| Fiber Patch Cord dual | Prizmatix | Optogenetics-Fiber 500, 1,20 m, Ferrule core 1,25 mm | Cables, which are connected with the two implants of a bilateral implantation |
| Fiber Patch Cord single | Prizmatix | Optogenetics-Fiber 500, 1,20 m, Ferrule core 1,25 mm | Cable, which is connected with the implant via a sleeve |
| Fiber Stripping Tool | Thorlabs | T06S13 | Stripping glass fiber for implant |
| Filter paper | VWR European | 516-0300 | Cut into pieces for the Novelty-Suppressed Feeding test |
| Food pellets | Mühle Levers | Höveler Nagerfutter | Nutrition for the mice |
| Glass pipettes | Harvard Apparatus | GC150-10 | Injection pipettes |
| Gradia direct-Flo | Henry Schein | 103322 | Fluid dental cementum |
| Heating lamp | efbe-Schott/Phillips | R95E | Prevent the mice from cooling after the surgery |
| Heating plate | Stoelting | Integrated into coordinate system | |
| Injection canula | Braun | 100 Sterican, 0,4 x 20 mm, Gr. 20 | All injections and to bore hole into the skull |
| Litter | T 1350 | Grounding for the Novelty-Supressed Feeding test | |
| Mouse cages | Zoonlab | 405 cm^2 | Single housing for experiments |
| Optibond FL | Kerr | 26684E | Preparation of the skull for implantation |
| Optical glass fiber | Thorlabs | FT200EMT | Light fiber for implant |
| Optogenetics-LED.STSI | Prizmatix | Optogenetic toolbox for light stimulation during behavioral experiments | |
| Paraformaldehyde | Sigma-Aldrich | 16005-1KG-R | Perfusion of mice to remove the brains |
| Polishing sheet 0.02 µm grit | Thorlabs | LFCF | Polishing implants round side |
| Polishing sheet 1 µm grit | Thorlabs | LF1D | Polishing implants round side |
| Polishing sheet 30 µm grit | Thorlabs | LF30D | Polishing implants round side |
| Polishing sheet 6 µm grit | Thorlabs | LF6D | Polishing implants round side |
| Pulser Software | Prizmatix | Software for light device control | |
| Rimadyl-Carprofen | Zoetis | Analgesia | |
| Sigma Plot | Software for statistics | ||
| Sleeve | Thorlabs | FT200EMT | Connection of implant and light cable |
| SodiumCloride (NaCl) | Braun | 3570410 | Rinsing of the skull |
| Superglue | Pattex Henkel | To Fix the glass fiber in the ferrule | |
| td-Tomato virus | Penn Vector Core | Addgene 51503 | Optogenetic tool |
| UV light | KoQGHJ | wireless, 1200 mW/cm^2 | Polymeration lamp for dental cementum |
| Xylavet-Xylazin | cp pharma | Anesthesia |
References
- Chow, B. Y., et al. High-performance genetically targetable optical neural silencing by light-driven proton pumps. Nature Letters. 463, 98-102 (2010).
- Zhao, S., et al. Cell type-specific channelrhodopsin-2 transgenic mice for optogenetic dissection of neural circuitry function. Nature Methods. 8, 745-752 (2011).
- Spoida, K., Masseck, O. A., Deneris, E. S., Herlitze, S. Gq/5-HT2c receptor signals activate a local GABAergic inhibitory feedback circuit to modulate serotonergic firing and anxiety in mice. Proceedings of the National Academy of Science of the United States of America. 111, 6479-6484 (2014).
- Kleinlogel, S. Optogenetic user’s guide to Opto-GPCRs modified GPCRs. Frontiers in Bioscience. 21, 794-805 (2016).
- Mahn, M., Prigge, M., Ron, S., Levy, R., Yizhar, O. Biophysical constraints of optogenetic inhibition at presynaptic terminals. Nature Neuroscience. 19, 554-556 (2016).
- Masseck, O. A., et al. Vertebrate Cone Opsins Enable Sustained and Highly Sensitive Rapid Control of Gi/o Signaling in Anxiety Circuitry. Neuron. 81, 1263-1273 (2014).
- Oh, E., Maejima, T., Liu, C., Deneris, E., Herlitze, S. Substitution of 5-HT 1A Receptor signaling by a light-activated G protein-coupled receptor. Journal of Biological Chemistry. 285, 30825-30836 (2010).
- Yizhar, O., Fenno, L. E., Davidson, T. J., Mogri, M., Deisseroth, K. Optogenetics in Neural Systems. Neuron Primer. 71, 9-34 (2011).
- Masseck, O. A., Manahan-Vaughan, D. A Guide to Optogenetic Applications, With special Focus on Behavioral and In Vivo Electrophysiological Experiments. HandboOk of In Vivo Neural Plasticity Techniques – A Systems Neuroscheince Approach to the Neural Basis of Memory and Cognition. , 557 (2019).
- Goebbels, S., et al. Genetic Targeting of Principal Neurons in Neocortex and Hippocampus of NEX-Cre Mice. Genesis. , 611-621 (2006).
- Yang, Y. S., Hughes, T. E. Cre Stoplight: A red/green fluorescent reporter of Cre recombinase expression in living cells. Biotechniques. 31, 1036-1041 (2001).
- Schnütgen, F., et al. A directional strategy for monitoring Cre-mediated recombination at the cellular level in the mouse. Nature Biotechnology. 21, 562-565 (2003).
- Taniguchi, H., et al. A Resource of Cre Driver Lines for Genetic Targeting of GABAergic Neurons in Cerebral Cortex. Neuron. 71, 995-1013 (2011).
- Deisseroth, K. Optogenetics. Nature Methods. 8, 268-273 (2011).
- Palanza, P., Gioiosa, L., Parmigiani, S. Social stress in mice: Gender differences and effects of estrous cycle and social dominance. Physiology and Behavior. 73, 411-420 (2001).
- Karolewicz, B., Paul, I. A. Group housing of mice increases immobility and antidepressant sensitivity in the forced swim and tail suspension tests. European Journal of Pharmacology. 415, 197-201 (2001).
- Masseck, O. A., Rubelowski, J. M., Spoida, K., Herlitze, S. Light- and drug-activated G-protein-coupled receptors to control intracellular signalling. Experimental Physiology. 96, 51-56 (2011).
- Aravanis, A. M., et al. An optical neural interface: in vivo control of rodent motor cortex with integrated fiberoptic and optogenetic technology. Journal of Neural Engineering. 4, (2007).
- Zhang, F., et al. Multimodal fast optical interrogation of neural circuitry. Nature Article. 446, 633-639 (2007).
- Owen, S. F., Liu, M. H., Kreitzer, A. C. Thermal constraints on in vivo optogenetic manipulations. Nature Neuroscience. 22, 1061-1065 (2019).
- Hare, B. D., et al. Optogenetic stimulation of medial prefrontal cortex Drd1 neurons produces rapid and long-lasting antidepressant effects. Nature Communication. 10, 1-12 (2019).
- Allsop, S. A., Vander Weele, C. M., Wichmann, R., Tye, K. M. Optogenetic insights on the relationship between anxiety-related behaviors and social deficits. Frontiers in Behavioral Neuroscience. 8, 1-14 (2014).
- Fuchikami, M., et al. Optogenetic stimulation of infralimbic PFC reproduces ketamine’s rapid and sustained antidepressant actions. Proceedings of the National Academy of Science of the United States of America. 112, 8106-8111 (2015).
- Correia, P. A., et al. Transient inhibition and long-term facilitation of locomotion by phasic optogenetic activation of serotonin neurons. Elife. 6, 1-26 (2017).
- Felix-Ortiz, A. C., Burgos-Robles, A., Bhagat, N. D., Leppla, C. A., Tye, K. M. Bidirectional modulation of anxiety-related and social behaviors by amygdala projections to the medial prefrontal cortex. Neuroscience. 321, 197-209 (2016).
- Marek, R., Xu, L., Sullivan, R. K. P., Sah, P. Excitatory connections between the prelimbic and infralimbic medial prefrontal cortex show a role for the prelimbic cortex in fear extinction. Nature Brief Communication. , (2018).
- Parfitt, G. M., et al. Bidirectional Control of Anxiety-Related Behaviors in Mice: Role of Inputs Arising from the Ventral Hippocampus to the Lateral Septum and Medial Prefrontal Cortex. Neuropsychopharmacology. 42, 1715-1728 (2017).
- Bandelow, B., Michaelis, S. Epidemiology of anxiety disorders in the 21st century. Dialogues in Clinical Neuroscience. 17, 327-335 (2015).
- Kessler, R. C., et al. Lifetime Prevalence and Age-of-Onset Distributions of DSM-IV Disorders in the National Comorbidity Survey Replication. Archives of General Psychiatry. 62, 593-602 (2005).
- Kessler, R. C., Petukhova, M., Sampson, N. A., Zaslavsky, A. M., Wittchen, H. U. Twelve-month and lifetime prevalence and lifetime morbid risk of anxiety and mood disorders in the United States. International Journal of Methods Psychiatric Research. 21, 169-184 (2014).
- Andlin-Sobocki, P., Wittchen, H. U. Cost of anxiety disorders in Europe. European Journal of Neurology. 12, 39-44 (2005).
- Forster, G. L., Novick, A. M., Scholl, J. L., Wall, M. J. The Role of the Amygdala in Anxiety Disorders. Intech. , 61-102 (2012).
- Liberzon, I. Neural circuits in anxiety and stress disorders a focused review. Therapeutics and Clinical Risk Management. 11, 115-126 (2015).
- Sylvers, P., Lilienfeld, S. O., LaPrairie, J. L. Differences between trait fear and trait anxiety: Implications for psychopathology. Clinical Psychology Review. 31, 122-137 (2011).
- Daws, L. C., Koek, W., Mitchell, N. C. Revisiting Serotonin Reuptake Inhibitors and the Therapeutic Potential of ‘Uptake-2’ in Psychiatric Disorders. ACS Chemical Neuroscience. 4, 16-21 (2013).
- Felix-Ortiz, A. C., et al. BLA to vHPC inputs modulate anxiety-related behaviors. Neuron Report. 79, 658-664 (2013).
- Padilla-Coreano, N., et al. Direct Ventral Hippocampal-Prefrontal Input Is Required for Anxiety-Related Neural Activity and Behavior. Neuron Article. 89, 857-866 (2016).
- Lisboa, S. F., Stecchini, M. F., Corrêa, F. M. A., Guimarães, F. S., Resstel, L. B. M. Different role of the ventral medial prefrontal cortex on modulation of innate and associative learned fear. Neuroscience. 171, 760-768 (2010).
- Bi, L. L., et al. Enhanced excitability in the infralimbic cortex produces anxiety-like behaviors. Neuropharmacology. 72, 148-156 (2013).
- Yizhar, O., et al. Neocortical excitation/inhibition balance in information processing and social dysfunction. Nature Article. 477, 171-178 (2011).
- Goebbels, S., et al. Genetic Targeting of Principal Neurons in Neocortex and Hippocampus of NEX-Cre Mice. Genesis. 44, 611-621 (2006).
- Rubenstein, J. L. R., Merzenich, M. M. Model of autism: increased ratio of excitation/ inhibition in key neural systems. Genes, Brain and Behavior. 2, 255-267 (2003).
- Berg, L., Eckardt, J., A, M. O. Enhanced activity of pyramidal neurons in the infralimbic cortex drives anxiety behavior. PLoS One. 14, 1-19 (2019).
- Meunier, C. N. J., Amar, M., Lanfumey, L., Hamon, M., Fossier, P. 5-HT1A receptors direct the orientation of plasticity in layer 5 pyramidal neurons of the mouse prefrontal cortex. Neuropharmacology. 71, 37-45 (2013).
- Paxinos, G., Franklin, K. B. J., Paxinos, G., Franklin, K. B. J., Paxinos, G., Franklin, K. B. J. . Mouse Brain in Stereotaxic Coordinates. 2, (2004).
- Gore, B. B., Soden, M. E., Zweifel, L. S. Manipulating gene expression in projection-specific neuronal populations using combinatorial viral approaches. Current Protocols in Neuroscience. 435, 1-6 (2014).
- Stujenske, J. M., Spellman, T., Gordon, J. A. Modeling the Spatiotemporal Dynamics of Light and Heat Propagation for InVivo Optogenetics. Cell Report. 12, 525-534 (2015).
- Berg, L. Imbalance of excitation and inhibition within the prefrontal cortex supports anxiety behavior. Ruhr-University Bochum. , (2019).
- Boyden, E. S. A history of optogenetics: The development of tools for controlling brain circuits with light. F1000 Biology Reports. 3, 1-12 (2011).
- Airan, R. D., Thompson, K. R., Fenno, L. E., Bernstein, H., Deisseroth, K. Temporally precise in vivo control of intracellular signalling. Nature. 458, 1025-1029 (2009).
- Sparta, D. R., et al. Construction of implantable optical fibers for long-term optogenetic manipulation of neural circuits. Nature Protocol. 7, 12-23 (2012).
- Covington, H. E., et al. Antidepressant Effect of Optogenetic Stimulation of the Medial Prefrontal Cortex. Journal of Neuroscience. 30, 16082-16090 (2010).
- Lepicard, E. M., Joubert, C., Hagneau, I., Perez-Diaz, F., Chapouthier, G. Differences in anxiety-related behavior and response to diazepam in BALB/cByJ and C57BL/6J strains of mice. Pharmacology, Biochemistry and Behavior. 67, 739-748 (2000).
- Schmidt, M. V., Müller, M. B. Animal models of anxiety. Elsevier. 3, 369-374 (2006).
- Cho, J. H., Deisseroth, K., Bolshakov, V. Y. Synaptic Encoding of Fear Extinction in mPFC-amygdala Circuits. Neuron Article. 80, 1491-1507 (2013).
- Adhikari, A., et al. Basomedial amygdala mediates top-down control of anxiety and fear. Nature. 527, 179-185 (2015).
- Suzuki, S., et al. The infralimbic and prelimbic medial prefrontal cortices have differential functions in the expression of anxiety-like behaviors in mice. Behavioural Brain Research. 304, 120-124 (2016).
- Carola, V., D’Olimpio, F., Brunamonti, E., Mangia, F., Renzi, P. Evaluation of the elevated plus-maze and open-field tests for the assessment of anxiety-related behaviour in inbred mice. Behavioural Brain Research. 134, 49-57 (2002).
- Prut, L., Belzung, C. The open field as a paradigm to measure the effects of drugs on anxiety-like behaviors: A review. European Journal of Pharmacology. 463, 3-33 (2003).
- Tye, K. M., et al. Amygdala circuitry mediating reversible and bidirectional control of anxiety. Nature Letter. 471, 358-362 (2011).
- Bouwknecht, J. A., et al. Differential effects of exposure to low-light or high-light open-field on anxiety-related behaviors: Relationship to c-Fos expression in serotonergic and non-serotonergic neurons in the dorsal raphe nucleus. Brain Research Bulletin. 72, 32-43 (2007).
- Overstreet, D. H., Knapp, D. J., Angel, R. A., Navarro, M., Breese, G. R. Reduction in repeated ethanol-withdrawal-induced anxiety-like behavior by site-selective injections of 5-HT1A and 5-HT2C ligands. Psychopharmacology. 187, 1-12 (2006).
- Takahashi, A., et al. Glutamate Input in the Dorsal Raphe Nucleus As a Determinant of Escalated Aggression in Male Mice. Journal of Neuroscience. 35, 6452-6463 (2015).
- Klemenhagen, K. C., Gordon, J. A., David, D. J., Hen, R., Gross, C. T. Increased Fear Response to Contextual Cues in Mice Lacking the 5-HT1A Receptor. Neuropsychopharmacology. 31, 101-111 (2006).
- Ramos, A. Animal models of anxiety: do I need multiple tests. Trends in Pharmacological Science. 29, 493-498 (2008).
- Isosaka, T., et al. Htr2a-Expressing Cells in the Central Amygdala Control the Hierarchy between Innate and Learned Fear. Cell. 163, 1153-1164 (2015).
- Regev, L., Goshen, I. Employing Optogenetics in Memory Research. Optogenetics: A Roadmap. , 219-256 (2017).
- Shah, A. A., Sjovold, T., Treit, D. Inactivation of the medial prefrontal cortex with the GABA A receptor agonist muscimol increases open-arm activity in the elevated plus-maze and attenuates shock-probe burying in rats. Brain Research. 1028, 112-115 (2004).
- Knight, A. R., et al. Pharmacological characterisation of the agonist radioligand binding site of 5-HT2A, 5-HT2B and 5-HT2C receptors. Naunyn-Schmiedebergs Archiv of Pharmacology. 370, 114-123 (2004).
- Graeff, F. G., Viana, M. B., Mora, P. O. Dual Role of 5-HT in Defense and Anxiety. Neuroscience and Biobehavioral Reviews. 21, 791-799 (1997).
- Cheriyan, J., Sheets, P. L. Altered Excitability and Local Connectivity of mPFC-PAG Neurons in a Mouse Model of Neuropathic Pain. Journal of Neuroscience. 38, 4829-4839 (2018).
- Boyden, E. S., Zhang, F., Bamberg, E., Nagel, G., Deisseroth, K. Millisecond-timescale, genetically targeted optical control of neural activity. Nature Neuroscience. 8, 1263-1268 (2005).

