Human lever mikrofysiologisk system til vurdering af lægemiddelinduceret levertoksicitet in vitro
Summary
Lægemiddelinduceret leverskade (DILI) er en væsentlig årsag til lægemiddelsvigt. En protokol er udviklet til nøjagtigt at forudsige DILI-ansvaret for en forbindelse ved hjælp af et levermikrofysiologisk system (MPS). Levermodellen bruger kokultur af primære leverceller og translationelt relevante endepunkter til at vurdere cellulære reaktioner på behandlingen.
Abstract
DILI er en væsentlig årsag til slid i lægemiddeludvikling med over 1000 FDA-godkendte lægemidler, der vides at potentielt forårsage DILI hos mennesker. Desværre opdages DILI ofte ikke, før lægemidlerne har nået kliniske stadier, hvilket risikerer patienternes sikkerhed og fører til betydelige tab for medicinalindustrien. I betragtning af at standard 2D-modeller har begrænsninger med hensyn til at detektere DILI, er det vigtigt at udvikle in vitro-modeller, der er mere forudsigelige for at forbedre dataoversættelsen. For at forstå kausalitet og mekanistiske aspekter af DILI i detaljer er der udviklet en human lever MPS bestående af humane primære leverparenkymale og ikke-parenkymale celler (NPC’er) og dyrket i 3D-mikrovæv på et konstrueret stillads under perfusion. Kryopræserverede primære humane hepatocytter (PHH’er) og Kupffer-celler (HKC’er) blev samdyrket som mikrovæv i MPS-platformen i op til to uger, og hver forbindelse af interesse blev gentagne gange doseret på levermikrovæv ved syv testkoncentrationer i op til fire dage. Funktionelle leverspecifikke endepunkter blev analyseret (herunder kliniske biomarkører såsom alaninaminotransferase, ALT) for at evaluere leverfunktionen. Akut og kronisk eksponering for forbindelser af forskellig DILI-sværhedsgrad kan vurderes ved at sammenligne respons på enkelt- og flerdoseret mikrovæv. Metoden er blevet valideret med et bredt sæt alvorlige og mildt hepatotoksiske forbindelser. Her viser vi dataene for pioglitazon og troglitazon, velkendte hepatotoksiske forbindelser, der er trukket tilbage fra markedet for at forårsage leversvigt. Samlet set har det vist sig, at lever-MPS-modellen kan være et nyttigt værktøj til at vurdere DILI og dets tilknytning til ændringer i leverfunktionen. Modellen kan desuden bruges til at vurdere, hvordan nye forbindelser opfører sig i forskellige patientundergrupper, og hvordan toksicitetsprofiler kan påvirkes af leversygdomstilstande (f.eks. viral hepatitis, fedtleversygdom).
Introduction
DILI er fortsat den hyppigste årsag til akut leversvigt i USA og Europa og er en førende årsag til nedslidning af forbindelser i lægemiddeludviklingsprocessen1. Næsten alle klasser af medicin kan forårsage hepatotoksicitet, hvor centralnervesystemet agenter og antibiotika er langt de mest almindelige behandlinger, der forårsager DILI hos patienter2. Lægemiddelinduceret hepatotoksicitet er forårsaget af en kompleks interaktion mellem genetiske, ikke-genetiske og miljømæssige faktorer, hvilket fører til død af hepatocytter og andre levercelletyper, herunder cholangiocytter og endotelceller 1,3.
DILI-fremkaldende midler kan klassificeres på to måder: dem, der forårsager forudsigelig dosisafhængig leverskade eller dem, der forårsager idiosynkratisk DILI, der er sjælden og udvikler sig uafhængigt af lægemiddeldosis eller indgivelsesvej, men er ansvarlig for op til en sjettedel af alle akutte leversvigt i USA kun4. Desværre opdages DILI ofte ikke, før lægemidlerne har nået de kliniske stadier af lægemiddeludviklingsprocessen. Lægemiddelinduceret leverskade rang (eller DILIrank) består af mere end tusind FDA-godkendte lægemidler, der er opdelt i fire klasser i henhold til deres potentiale for at forårsage DILI, og deres anvendelse hos patienter skal overvåges nøje5.
At studere mekanismer for lægemiddelhepatotoksicitet er fortsat meget udfordrende, og derfor er der udviklet mange prækliniske modeller til at udforske mekanismer for DILI. Nuværende in vitro- og in vivo-modeller, der bruges til at forudsige DILI i præklinisk udvikling, har flere begrænsninger for at give indsigt i de komplekse, mangesidede interaktioner i en levende menneskekrop. Kræftformede levercellelinjer (dvs. HepG2, HepaRG) dyrket i 2D anvendes stadig i de tidlige stadier af lægemiddeludvikling til evaluering af toksiciteten af kandidatforbindelser6. Alligevel kommer disse cellelinjer fra enkeltdonorer og viser unormale niveauer af leverfunktion og udviser ikke altid høj følsomhed til påvisning af DILI 7,8. Som et alternativ til kræftformede levercellelinjer repræsenterer PHH’er bedre human leverfysiologi, hvis de dyrkes korrekt in vitro, selvom der findes flere begrænsninger med deres kultur, som kort inkubationstid med lægemidler, relativt kort levetid, tab af levergenekspression og ændringer i lægemiddelmetaboliske funktioner 9,10,11 . PHH’er kan dyrkes på ekstracellulære matrixproteiner i standard 2D-cellekulturplader, men som en ulempe betyder det hurtige fald i deres funktion, at de har lav følsomhed (<50%) for DILI-forudsigelse12.
På den anden side er test på dyremodeller langsomme, dyre og har brug for en oversættelse på tværs af arter for at ekstrapolere forudsigelse til mennesker. De fleste nyudviklede lægemidler får ikke godkendelse, hvilket gør denne proces dyr og risikabel5. Desuden er dyremodeller mindre egnede til test af nye menneskespecifikke modaliteter på grund af gensekvenser eller immunologiske responsforskelle i forhold til mennesker13.
Derfor er interessen for mere avancerede tredimensionelle (3D) in vitro-levermodeller vokset eksponentielt. Dyrkning af PHH’er som sfæriske strukturer genereret af gravitationsaggregering i hængende dråber eller på ultralave fastgørelsesoverflader repræsenterer en metode med høj kapacitet til vurdering af sammensatte forpligtelser14. PHH sfæroider er blevet brugt til at vurdere DILI i en syg baggrund (fx steatose og kolestase)15. En bred vifte af modeller er blevet udviklet til at omfatte belagte mikromønstrede kokulturer af hepatocytter med stromale fibroblaster16, 3D bioprintet levervæv17, 3D sfæroidkulturer med eller uden hepatiske ikke-parenkymale celler15. Alle disse metoder har dog stadig ulemper, og dyrkning af PHH’er i et mere fysiologisk relevant mikromiljø kan give dem højere funktionalitetsniveauer i længere tid for at muliggøre undersøgelse af langvarig eksponering for potentielle hepatotoksiske stoffer. For at forbedre den translationelle relevans af enhver avanceret in vitro-PHH-kultur skal klinisk relevante funktionelle endepunkter eller biomarkører for toksicitetsoutput desuden anvendes til at gøre det muligt at sammenligne data in vivo eller kliniske scenarier18.
I denne undersøgelse vurderede vi, om en MPS, også kendt som en Organ-on-a-Chip (OOC), in vitro levermodel kunne bruges til at forstå de detaljerede mekanistiske aspekter af levertoksicitet. MPS har tidligere vist sig at opretholde yderst funktionelle 3D-levermikrovæv under flow i op til 4 uger19. Systemet er for nylig blevet testet af FDA og vist sig at have høj reproducerbarhed, når der udføres lægemiddeltoksicitet, metabolisme og intracellulær akkumulering20. Desuden havde systemet sammenlignet med sfæroider og sandwichkulturer en mere stabil funktion og højere følsomhed ved påvisning af toksiciteten af flere lægemidler20. Til dato er MPS blevet brugt i en lang række applikationer, der dækker ADME 21, sygdomsmodellering (HBV 22, NAFLD 23,24,25) og lægemiddelinteraktioner 26, hvilket potentielt gør det meget velegnet til vurdering af akut og kronisk DILI. Den teknologi, der præsenteres her, tilbyder et alternativ til at lukke kløften mellem mere traditionelle cellekulturer og dyremodeller og kliniske forsøg på mennesker og går videre mod simulering af humane biologiske tilstande for at understøtte vurderingen af kandidatforbindelsers levertoksicitet i prækliniske stadier af lægemiddeludviklingsprocessen.
Protocol
Representative Results
Discussion
MPS er designet til at rekapitulere funktionelle enheder af menneskelige organer in vitro og er udviklet til at tackle begrænsningerne i konventionelle 3D-cellekulturmodeller27. Leveren er et af de mest modellerede organer ved hjælp af MPS, og der er udviklet en lang række systemer. Den menneskelige lever er ansvarlig for lægemiddelmetabolisme og generering af giftige lægemiddelmetabolitter, og dens funktion er et nøgleelement i modellen for lægemiddeludvikling, herunder vurdering af DILI-ansvaret for forbindelser28. Her har vi introduceret en ny metode til vurdering af DILI ved hjælp af en lever MPS; protokollen gør det muligt at søge mekanistisk indsigt for hver forbindelse, der analyseres for at bestemme, hvordan det kan forårsage DILI såvel som at være et meget følsomt og robust assay. Levermikrovæv dannes i MPS-pladerne, som er en kokultur af PHH- og HKC’er og er yderst funktionelle med høje niveauer af albumin- og urinstofproduktion samt høj CYP3A4-aktivitet sammenlignet med standard in vitro-levermodeller 20.
Selvom DILI-modellen, der er beskrevet her, kan tjene som et nyttigt værktøj i senere stadier af præklinisk test i lægemiddeludviklingsprocessen, har den også flere begrænsninger. Da størstedelen af MPS i øjeblikket er tilgængelig på markedet, er det en platform med lav kapacitet og derfor vanskeligere at bruge til storstilede lægemiddelscreeningsaktiviteter. Bestående af mikrovæv dannet ved cokulturering af PHH’er og HKC’er kan DILI-modellen heller ikke helt fange kompleksiteten af den menneskelige lever, og yderligere optimering ved at inkorporere forskellige typer celler (f.eks. Immunceller) ville være gavnligt for at tilføje værdi til den eksisterende model. Denne enkeltorgans MPS kan også kombineres med andre organplatforme, der kan dele et fælles medium og tillade organkrydstale på cellulært eller endokrin niveau, og det kan bidrage til bedre at forstå den mekanistiske indsigt i toksicitet, der ikke kun er begrænset til selve leveren. Desuden kan den som enhver relativt ny teknologi betragtes som dyr og dermed med begrænset tilgængelighed.
MPS er en platform, der bruges til at udvikle organotypiske modeller af enkelt- eller multihumant væv. Systemet består af en controller, navlestrengskabel og MPS-driver, hvori pladen indsættes (figur 5A). Hver lever MPS-plade har 12 uafhængige åbne brønde til dyrkning af primære leverceller i 3D på konstruerede stilladser. Sammenfattende er systemet QC-kontrolleret, og pladerne er primet på dag -1, PHH’erne og HKC’erne er podet på pladerne på dag nul (figur 5B, se 1). Indlejrede mikropumper letter cirkulationen af cellekulturmedier gennem stilladserne for at lette dannelsen af 3D-mikrovæv (figur 5B, se 2). Dannede mikrovæv QC’s på dag 4, doseret med forskellige koncentrationer af hver forbindelse hver 48. time i 4 dage og analyseret for endepunktsbiomarkører på dag 8 (figur 5C). Den eksperimentelle tidslinje for DILI-analysen i MPS-pladen er afbildet i figur 5D.
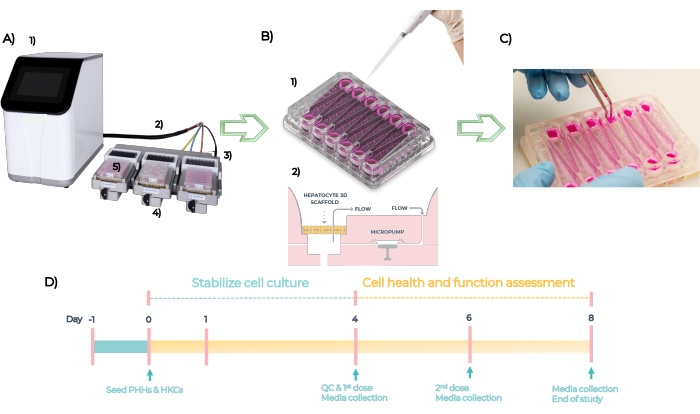
Figur 5: Det mikrofysiologiske system og den eksperimentelle tidslinje for et standard DILI-assay. (A) Det mikrofysiologiske system med dets komponenter: controller (1), navlestrengskabel (2), dockingstation (3), MPS-driver (4) og LC12-plade (5). (B) Såning af PHH’er og HKC’er på LC12-pladen på dag 1 (1) og indlejrede mikropumper letter cirkulationen af cellekulturmedier med indstillelige strømningshastigheder gennem 3D-mikrovæv, der er podet på stilladserne (2). (C) Nedtagning af stilladserne ved undersøgelsens afslutning. (D) Eksperimentel tidslinje. Klik her for at se en større version af denne figur.
Når du udfører protokollen, er det vigtigt, at der udføres en robust system QC-kontrol inden start, kontrol af, at systemet fungerer pneumatisk korrekt, og forbrugspladerne inspiceres visuelt og grundes effektivt for at sikre jævn funktionalitet på tværs af alle brønde. At have primære humane celler af høj kvalitet er afgørende for denne protokol, med hepatocytter, der vides at klæbe konsekvent i cellekultureksperimenter og danne 3D-interaktioner. Optøning af disse celler er også et kritisk trin, da primære hepatocytter ikke bør resuspenderes ved pipetteringsvirkning, da dette hurtigt kan føre til celledød. At have cellelevedygtighed over 85% er afgørende for vellykket såning, da store mængder cellulært affald vil forstyrre dannelsen af 3D-mikrovæv. QC-kontrollen af dannet levermikrovæv på dag 4 er også vigtig, og brugeren skal sikre, at acceptable niveauer af LDH og Urea måles, da parametre uden for rækkevidde kan være tegn på vævsdannelse af dårlig kvalitet og muliggøre ligetil fejlfinding. Endelig skal hydrocortisonen, der anvendes i cellekulturmediet, fremstilles frisk på brugsdagen for at forhindre uønsket nedbrydning, der kan påvirke cellekulturens funktionalitet, da det er nødvendigt for at opretholde hepatocytternes metaboliske funktionalitet.
På trods af at den har betydelig kompleksitet, indeholder leveren MPS ikke alle celletyper i den menneskelige lever. Det er muligt at tilføje yderligere celletyper til model24,29 for at øge den fysiologiske relevans, men disse bør kun tilføjes med en klar begrundelse for anvendelseskonteksten. Til undersøgelse af DILI PHH er nøglecelletypen, og inkorporeringen af HKC’er i denne model gør det muligt at bestemme nogle immunologiske reaktioner. Det skal også bemærkes, at PHH’er isoleret fra menneskelige lever og kommercielt tilgængelige kryopræserverede PHH’er har tendens til at demonstrere nogle variationer fra parti til parti. Vi har her vist, at denne protokol giver reproducerbare resultater, når den anvendes sammen med præparater af høj kvalitet af celler. Der forventes dog en vis variation mellem partier og partier, og dette kan yderligere overvindes ved at bruge samlede masser af flere donorer. Disse begrænsninger kan overvindes ved at bruge hepatocytlignende celler differentieret fra iPSC, der rekapitulerer mange funktionelle egenskaber ved PHH’er, og som er blevet brugt i lægemiddeludviklingsprocessen30. HKC’er viser også meget til meget variation og et højt niveau af aktivering ved optøning; derfor er HKC-donorer prævalideret internt inden brug i eksperimentel cellekultur (samkultur med validerede PHH’er) og skal have lave niveauer af aktivering efter optøning; dette vurderes ved at måle biomarkører IL-6 og TNF-alpha (se Supplerende materiale).
De data, der præsenteres her, bekræfter, at analysen kan detektere DILI nøjagtigt, hvilket hjælper med at identificere hepatotoksiske stoffer, der muligvis ikke opdages af 2D10,11 og endda nogle 3D-modeller. Data genereret fra MPS anvendes stadig ikke som standard af medicinalindustrien til lovgivningsmæssige indsendelser eller lægemiddelscreeningsformål på grund af manglende processtandardisering og harmonisering, herunder reproducerbarhed mellem steder20. De data og eksperimentelle tilgange, der er demonstreret her, adresserer dette og viser, at levermodellen kan bruges rutinemæssigt og robust i DILI-skærme til nøjagtigt at forudsige ansvaret for nye forbindelser.
Ved at måle en række endepunkter for at producere en “signatur af hepatotoksicitet”, hjælpe med at identificere forbindelser med forskellige niveauer af DILI-bekymring (herunder forbindelser, der ikke kan påvises ved andre in vitro-metoder) og deres toksicitetsmekanismer afsløret. Denne teknologi kan lukke kløften mellem traditionelle cellekultur- og dyremodeller på den ene side og humane kliniske forsøg og gå videre mod simulering af humane biologiske tilstande til præklinisk vurdering af levertoksicitet som en del af lægemiddeludviklingsprocessen.
Disclosures
The authors have nothing to disclose.
Acknowledgements
CN Bio Innovations Ltd. finansierede denne undersøgelse.
Materials
| 24 well cell culture cluster plates flat bottom | Corning | 3524 | |
| 96 well clear assay plates, flat bottom clear plastic | Greiner | 655101 | |
| 96 well plates black flat bottom | Corning | 3915 | |
| 96 Well White/Clear Bottom Plate, TC Surface | ThermoScientific | 165306 | |
| Advanced DMEM (1x) | Gibco | 12491015 | Cell culture media. |
| AssayMax Albumin ELISA Kit | AssayPro | EA3201-1 | Dilution 1:250. Time point Day 4, 6, and 8. |
| Cell Maintenance Cocktail B, (Primary Hepatocyte Maintenance Supplements) | Gibco | CM4000 | |
| CellTiter-Glo 3D Cell Viability Assay | Promega | G9682 | Dilution 1:1. Time point Day 8. |
| Chlorpromazine HCl | Sigma Aldrich | C8138 | |
| Chromacol blue lids, 9 mm Autosampler Vial Screw Thread Caps | ThermoScientific | 9-SCK(B)-ST1 | glass vial |
| Chromacol vials, 9 mm Clear Glass Screw Thread Vials | ThermoScientific | 2-SVW | |
| Class 2 Microbiological Safety Cabinets – Trimat2 1500 exhaust | Contained Air Solutions | ||
| Conical tubes 50 mL | Greiner | 227261 | |
| Cryopreserved Hepatocyte Recovery Medium (CHRM) | ThermoFisher Scientific | Gibco CM7000 | |
| Cryopreserved primary human hepatocytes | BioIVT Europe | Lot. RAS | |
| CytoTox 96 Cytotoxicty (LDH) Assay Kit | Promega | G1781 | Dilution – none. Time point Day 4, 6 and 8 |
| >Data analysis model used to generate the graph and EC:50 curves was nonlinear regression (curve fit) asymmetric sigmoidal, 5PL, where X is log(concentration | GraphPad Prism 9 | ||
| Disposable PES Filter Units 500mL | Fisher Scientific | 15913307 | |
| Disposable Pipette Basins 50ml | Fisher Scientific | 12369175 | |
| DMSO (Dimethyl sulfoxide) | Sigma-Aldrich | Sigma D2650 | |
| Dulbeco’s Phosphate Buffered Saline without Ca2+ and Mg2+ (D-PBS) | ThermoFisher Scientific | 14190-144 | |
| Easy Reader Conical Polypropylene Centrifuge Tubes 15 mL | Fisher Scientific | 11889640 | |
| Foetal bovine serum | Gibco | 10500064 | |
| Human ALT ELISA Kit | Abcam | ab 234578 | Dilution 1:5. Time point Day 6 and 8. |
| Human Cryopreserved Kupffer Cells | Lonza Europe | Lot. 190088KC | |
| hydrocortisone | Merck | H0888-1G | |
| Incubators models: New Brunswick Galaxy 170 S, New Brunswick Galaxy 170 R and CellXpert® C170. | Eppendorf | All serviced yearly; paperwork available upon request. | |
| Inverted Microscope | Leica DMIL LED | ||
| MPS know as Organ-on-a-Chip (OOC) | CN Bio Innovations Ltd. | ||
| MPS LC-12 plate | CN Bio Innovations Ltd. | ||
| Neubauer Improved C-Chip Disposable Haemocytometer (2 channel) | Cambridge Bioscience | DHC-N01-50 | |
| P450-Glo CYP3A4 Assay and Screening System | Promega | V9002 | Dilution – none. Time point Day 8 |
| PhysioMimix MPS platform | CN Bio Innovations Ltd. | ||
| Pioglitazone | MedChemExpress Tocris | HY-13956/CS-1700 | |
| Quantichrom Urea Assay Kit – Bioassay systems | Bioassay Systems | DY970-05 | Dilution 1:2 if initial reading is too high. Time point Day 4, 6 and 8. |
| Silica gel | Sigma-Aldrich | S7625 | |
| Software used to analyse and generate all the graphs was | GraphPad Prism 9 | ||
| Stripettes 10 mL | Fisher Scientific | 11839660 | |
| Stripettes 25 mL | Fisher Scientific | 11839181 | |
| Thawing plate Cocktail A, (Primary Hepatocyte Thawing and Plating Supplements) | Gibco | CM3000 | |
| Troglitazone | MedChemExpress Tocris | 97322-87-7 | |
| Trypan Blue Solution, 0.4% | Gibco | 15250061 | |
| Tubes 1.5 mL | Greiner | 616201 | |
| Weighing balance – model PA214C and AV213C | Ohaus Corp |
References
- Lisi, D. M. Drug-induced liver injury: An overview. US Pharmacist. 41 (12), 30-34 (2016).
- Kuna, L., et al. Models of drug induced liver injury (DILI)-current issues and future perspectives. Current Drug Metabolism. 19 (10), 830-838 (2018).
- Katarey, D., Verma, S. Drug-induced liver injury. Clinical Medicine. 16 (6), 104-109 (2016).
- Kullak-Ublick, G. A., et al. Drug-induced liver injury: recent advances in diagnosis and risk assessment Recent advances in clinical practice. Gut. 66, 1154-1164 (2017).
- Dirven, H., et al. Performance of pre-clinical models in predicting drug-induced liver injury in humans: a systematic review. Scientific Reports. 11 (1), 6403 (2021).
- Donato, M. T., Lahoz, A., Castell, J. V., Gomez-Lechon, M. J. Cell lines: a tool for in vitro drug metabolism studies. Current Drug Metabolism. 9 (1), 1-11 (2008).
- Wilkening, S., Stahl, F., Bader, A. Comparison of primary human hepatocytes and hepatoma cell line HepG2 with regard to their biotransformation properties. Drug Metabolism and Disposition. 31 (8), 1035-1042 (2003).
- Gerets, H. H. J., et al. Characterization of primary human hepatocytes, HepG2 cells, and HepaRG cells at the mRNA level and CYP activity in response to inducers and their predictivity for the detection of human hepatotoxins. Cell Biology and Toxicology. 28 (2), 69-87 (2012).
- Grainger, C. I., Greenwell, L. L., Lockley, D. J., Martin, G. P., Forbes, B. Culture of Calu-3 cells at the air interface provides a representative model of the airway epithelial barrier. Pharmaceutical Research. 23 (7), 1482-1490 (2006).
- Li, F., Cao, L., Parikh, S., Zuo, R. Three-dimensional spheroids with primary human liver cells and differential roles of kupffer cells in drug-induced liver injury. Journal of Pharmaceutical Sciences. 109 (6), 1912-1923 (2020).
- Proctor, W. R., et al. Utility of spherical human liver microtissues for prediction of clinical drug-induced liver injury. Archives of Toxicology. 91 (8), 2849-2863 (2017).
- Lin, C., Khetani, S. R. Advances in engineered liver models for investigating drug-induced liver injury. BioMed Research International. 2016, 1829148 (2016).
- Olson, H., et al. Concordance of the toxicity of pharmaceuticals in humans and in animals. Regulatory Toxicology and Pharmacology. 32 (1), 56-67 (2000).
- Bell, C. C., et al. Comparison of hepatic 2D sandwich cultures and 3D spheroids for long-term toxicity applications: A multicenter study. Toxicological Sciences. 162 (2), 655-666 (2018).
- Bell, C. C., et al. Characterization of primary human hepatocyte spheroids as a model system for drug-induced liver injury, liver function and disease. Scientific Reports. 6, 25187 (2016).
- Khetani, S. R., et al. Use of micropatterned co-cultures to detect compounds that cause drug-induced liver injury in humans. Toxicological Sciences. 132 (1), 107-117 (2013).
- Ma, X., et al. Deterministically patterned biomimetic human iPSC-derived hepatic model via rapid 3D bioprinting. Proceedings of the National Academy of Sciences of the united States of America. 113 (8), 2206-2211 (2016).
- Dieterle, P. Y. M., Dieterle, F. Tissue-specific, non-invasive toxicity biomarkers: translation from pre-clinical safety assessment to clinical safety monitoring. Expert Opinion on Drug Metabolism & Toxicology. 5 (9), 1023-1038 (2009).
- Rowe, C., et al. Perfused human hepatocyte microtissues identify reactive metabolite-forming and mitochondria-perturbing hepatotoxins. Toxicology in Vitro. 46, 29-38 (2018).
- Rubiano, A., et al. Characterizing the reproducibility in using a liver microphysiological system for assaying drug toxicity, metabolism, and accumulation. Clinical and Translational Science. 14 (3), 1049-1061 (2021).
- Tsamandouras, N., Kostrzewski, T., Stokes, C. L., Griffith, L. G., Hughes, D. J., Cirit, M. Quantitative assessment of population variability in hepatic drug metabolism using a perfused three-dimensional human liver microphysiological system. Journal of Pharmacology and Experimental Therapeutics. 360 (1), 95-105 (2017).
- Ortega-Prieto, A. M., et al. 3D microfluidic liver cultures as a physiological pre-clinical tool for hepatitis B virus infection. Nature Communications. 9 (1), 682 (2018).
- Kostrzewski, T., et al. Three-dimensional perfused human in vitro model of non-alcoholic fatty liver disease. World Journal of Gastroenterology. 23 (2), 204-215 (2017).
- Kostrzewski, T., et al. A microphysiological system for studying nonalcoholic steatohepatitis. Hepatology Communications. 4 (1), 77-91 (2020).
- Vacca, M., et al. Bone morphogenetic protein 8B promotes the progression of non-alcoholic steatohepatitis. Nature Metabolism. 2 (6), 514-531 (2020).
- Long, T. J., et al. Modeling therapeutic antibody-small molecule drug-drug interactions using a three-dimensional perfusable human liver co-culture platforms. Drug Metabolism and Disposition. 44, 1940-1948 (2016).
- Bai, J., Wang, C. Organoids and microphysiological systems: New tools for ophthalmic drug discovery. Frontiers in Pharmacology. 11, 407 (2020).
- Ribeiro, A. J. S., Yang, X., Patel, V., Madabushi, R., Strauss, D. G. Liver microphysiological systems for predicting and evaluating drug effects. Clinical Pharmacology & Therapeutics. 106 (1), 139-147 (2019).
- Clark, A. M., et al. A microphysiological system model of therapy for liver micrometastases hhs public access. Experimental Biology and Medicine (Maywood). 239 (9), 1170-1179 (2014).
- Qosa, H., Ribeiro, A. J. S., Hartman, N. R., Volpe, D. A. Characterization of a commercially available line of iPSC hepatocytes as models of hepatocyte function and toxicity for regulatory purposes. Journal of Pharmacological and Toxicological Methods. 110, 107083 (2021).

