Humant levermikrofysiologisk system for vurdering av legemiddelindusert levertoksisitet in vitro
Summary
Legemiddelindusert leverskade (DILI) er en viktig årsak til legemiddelsvikt. En protokoll er utviklet for å nøyaktig forutsi DILI-ansvaret til en forbindelse ved hjelp av et levermikrofysiologisk system (MPS). Levermodellen bruker kokulturen til primære leverceller og translasjonelt relevante endepunkter for å vurdere cellulær respons på behandling.
Abstract
DILI er en viktig årsak til slitasje i stoffutvikling med over 1000 FDA-godkjente legemidler som er kjent for å potensielt forårsake DILI hos mennesker. Dessverre oppdages DILI ofte ikke før medisinene har nådd kliniske stadier, noe som risikerer pasientenes sikkerhet og fører til betydelige tap for legemiddelindustrien. Tatt i betraktning at standard 2D-modeller har begrensninger i å oppdage DILI, er det viktig å utvikle in vitro-modeller som er mer prediktive for å forbedre dataoversettbarheten. For å forstå kausalitet og mekanistiske aspekter ved DILI i detalj, er det utviklet en human lever-MPS bestående av humane primære leverparenkymale og ikke-parenkymale celler (NPC) og dyrket i 3D-mikrovev på et konstruert stillas under perfusjon. Kryopreserverte primære humane hepatocytter (PHH) og Kupffer-celler (HKC) ble dyrket som mikrovev i MPS-plattformen i opptil to uker, og hver sammensetning av interesse ble gjentatt dosert på levermikrovev ved syv testkonsentrasjoner i opptil fire dager. Funksjonelle leverspesifikke endepunkter ble analysert (inkludert kliniske biomarkører som alaninaminotransferase, ALAT) for å evaluere leverfunksjonen. Akutt og kronisk eksponering for forbindelser av ulik DILI-alvorlighetsgrad kan vurderes ved å sammenligne respons på enkelt- og flerdosert mikrovev. Metodikken er validert med et bredt sett av alvorlige og mildt hepatotoksiske forbindelser. Her viser vi dataene for pioglitazon og troglitazon, kjente hepatotoksiske forbindelser trukket fra markedet for å forårsake leversvikt. Samlet sett har det vist seg at MPS-modellen i leveren kan være et nyttig verktøy for å vurdere DILI og dens tilknytning til endringer i leverfunksjon. Modellen kan i tillegg brukes til å vurdere hvordan nye forbindelser oppfører seg i forskjellige pasientundergrupper og hvordan toksisitetsprofiler kan påvirkes av leversykdomstilstander (f.eks. Viral hepatitt, fettleversykdom).
Introduction
DILI er fortsatt den vanligste årsaken til akutt leversvikt i USA og Europa og er en ledende årsak til slitasje av forbindelser i legemiddelutviklingsprosessen1. Nesten alle klasser av medisiner kan forårsake hepatotoksisitet, med sentralnervesystemet agenter og antibiotika er langt de vanligste behandlingene som forårsaker DILI hos pasienter2. Legemiddelindusert hepatotoksisitet er forårsaket av en kompleks interaksjon av genetiske, ikke-genetiske og miljømessige faktorer, noe som fører til død av hepatocytter og andre levercelletyper, inkludert kolangiocytter og endotelceller 1,3.
DILI-forårsakende stoffer kan klassifiseres på to måter: de som forårsaker forutsigbar doseavhengig leverskade eller de som forårsaker idiosynkratisk DILI som er sjelden og utvikler seg uavhengig av legemiddeldose, eller rute eller administrasjonsvarighet, men er ansvarlig for opptil en sjettedel av alle akutte leversvikt i USA bare4. Dessverre oppdages DILI ofte ikke før stoffene har nådd de kliniske stadiene av legemiddelutviklingsprosessen. Legemiddelindusert leverskaderangering (eller DILIrank) består av mer enn tusen FDA-godkjente medisiner som er delt inn i fire klasser i henhold til deres potensial for å forårsake DILI, og deres bruk hos pasienter må overvåkes nøye5.
Studier av mekanismer for legemiddel hepatotoksisitet er fortsatt svært utfordrende, og derfor har mange prekliniske modeller blitt utviklet for å utforske mekanismer for DILI. Nåværende in vitro og in vivo modeller som brukes til å forutsi DILI i preklinisk utvikling har flere begrensninger for å gi innsikt i de komplekse, mangefasetterte interaksjonene i en levende menneskekropp. Kreftfremkallende levercellelinjer (dvs. HepG2, HepaRG) dyrket i 2D brukes fortsatt i de tidlige stadiene av legemiddelutvikling for å evaluere toksisiteten til kandidatforbindelser6. Likevel kommer disse cellelinjene fra enkeltdonorer og viser unormale nivåer av leverfunksjon, og viser ikke alltid høy følsomhet for påvisning av DILI 7,8. Som et alternativ til kreft i levercellelinjer, representerer PHHs bedre menneskelig leverfysiologi hvis de dyrkes hensiktsmessig in vitro, selv om det finnes flere begrensninger med deres kultur, som kort inkubasjonstid med medisiner, relativt kort levetid, tap av hepatisk genuttrykk og endringer i stoffets metabolske funksjoner 9,10,11 . PHH kan dyrkes på ekstracellulære matriksproteiner i standard 2D-cellekulturplater, men som en ulempe betyr den raske nedgangen i funksjonen at de har lav følsomhet (<50%) for DILI-prediksjon12.
På den annen side er testing på dyremodeller langsom, dyrt og trenger en oversettelse på tvers av arter for å ekstrapolere prediksjon til mennesker. De fleste nyutviklede legemidler klarer ikke å få godkjenning, noe som gjør denne prosessen kostbar og risikabel5. Videre, for å teste nye menneskespesifikke modaliteter, er dyremodeller mindre egnet på grunn av gensekvens eller immunologiske responsforskjeller mot mennesker13.
Følgelig har interessen for mer avanserte tredimensjonale (3D) in vitro levermodeller eksponentielt vokst. Dyrking av PHH-er som sfæriske strukturer generert av gravitasjonsaggregering i hengende dråper eller på ultralave festeflater representerer en høy gjennomstrømningsmetode for å vurdere sammensatte forpliktelser14. PHH-sfæroider har blitt brukt til å vurdere DILI i en syk bakgrunn (f.eks. steatose og kolestase)15. Et bredt utvalg av modeller er utviklet for å inkludere belagte mikromønstrede kokulturer av hepatocytter med stromale fibroblaster16, 3D bioprintede levervev17, 3D-sfæroidkulturer med eller uten hepatiske ikke-parenkymale celler15. Imidlertid har alle disse metodene fortsatt ulemper, og dyrking av PHH i et mer fysiologisk relevant mikromiljø kan gi dem høyere nivåer av funksjonalitet i lengre perioder for å muliggjøre undersøkelse av langvarig eksponering for potensielle hepatotoksiske stoffer. I tillegg, for å forbedre translasjonsrelevansen av enhver avansert in vitro PHH-kultur, må klinisk relevante funksjonelle endepunkter eller biomarkører for toksisitetsutgang brukes for å tillate at data sammenlignes in vivo eller kliniske scenarier18.
I denne studien vurderte vi om en MPS, også kjent som en Organ-on-a-Chip (OOC), in vitro levermodell kunne brukes til å forstå de detaljerte mekanistiske aspektene ved levertoksisitet. MPS har tidligere vist seg å opprettholde svært funksjonelle 3D levermikrovev, under strømning, i opptil 4 uker19. Systemet har nylig blitt testet av FDA og vist seg å ha høy reproduserbarhet ved utførelse av legemiddeltoksisitet, metabolisme og intracellulær akkumulering20. Videre, sammenlignet med sfæroider og sandwichkulturer, hadde systemet en mer stabil funksjon og høyere følsomhet for å oppdage toksisiteten til flere stoffer20. Til dags dato har MPS blitt brukt i et bredt spekter av applikasjoner som dekker ADME 21, sykdomsmodellering (HBV 22, NAFLD 23,24,25) og legemiddelinteraksjoner 26, noe som potensielt gjør den svært egnet til å vurdere akutt og kronisk DILI. Teknologien som presenteres her tilbyr et alternativ for å lukke gapet mellom mer tradisjonelle cellekulturer og dyremodeller og menneskelige kliniske studier, og fremme mot simulering av humane biologiske forhold for å støtte vurderingen av kandidatforbindelsers levertoksisitet i prekliniske stadier av legemiddelutviklingsprosessen.
Protocol
Representative Results
Discussion
MPS er designet for å rekapitulere funksjonelle enheter av menneskelige organer in vitro og er utviklet for å adressere begrensningene i konvensjonelle 3D-cellekulturmodeller27. Leveren er et av de mest modellerte organene som bruker MPS, og et bredt utvalg av systemer er utviklet. Den humane leveren er ansvarlig for legemiddelmetabolisme og generering av toksiske legemiddelmetabolitter, og dens funksjon er et nøkkelelement for modell for legemiddelutvikling, inkludert vurdering av DILI-ansvar for forbindelser28. Her har vi introdusert en ny metode for å vurdere DILI ved hjelp av en lever-MPS; protokollen gjør det mulig å søke mekanistisk innsikt for hver forbindelse som analyseres for å bestemme hvordan den kan forårsake DILI, samt å være en svært sensitiv og robust analyse. Levermikrovev dannes i MPS-platene, som er en kokultur av PHH og HKC og er svært funksjonelle med høye nivåer av albumin- og ureaproduksjon samt høy CYP3A4-aktivitet sammenlignet med standard in vitro levermodeller20.
Selv om DILI-modellen beskrevet her kan tjene som et nyttig verktøy i senere stadier av preklinisk testing i legemiddelutviklingsprosessen, har den også flere begrensninger. Som flertallet av MPS som for tiden er tilgjengelig på markedet, er det en plattform med lav gjennomstrømning og derfor vanskeligere å bruke til store narkotikascreeningsaktiviteter. Bestående av mikrovev dannet ved å kokulere PHHs og HKCs, kan DILI-modellen heller ikke helt fange kompleksiteten til den menneskelige leveren, og ytterligere optimalisering ved å inkorporere forskjellige typer celler (f.eks. Immunceller) vil være gunstig for å tilføre verdi til den eksisterende modellen. Denne enkeltorgan-MPS kan også kombineres med andre organplattformer som kan dele et felles medium og tillate organkrysstale på cellulært eller endokrint nivå, og som kan bidra til å bedre forstå den mekanistiske innsikten om toksisitet, ikke bare begrenset til leveren selv. Videre, som enhver relativt ny teknologi, kan det betraktes som kostbart og dermed begrenset tilgjengelighet.
MPS er en plattform som brukes til å utvikle organotypiske modeller av enkelt eller multi- humant vev. Systemet består av en kontroller, navlestreng og MPS-driver som platen er satt inn i (figur 5A). Hver lever-MPS-plate har 12 uavhengige åpne brønner for dyrking av primære leverceller i 3D på konstruerte stillaser. Oppsummert er systemet QC-kontrollert, og platene er primet på dag -1, PHH-ene og HKC-ene er sådd på platene ved dag null (figur 5B, se 1). Innebygde mikropumper letter sirkulasjonen av cellekulturmedier gjennom stillasene for å lette dannelsen av 3D-mikrovev (figur 5B, se 2). Dannede mikrovev er QC’d på dag 4, dosert med forskjellige konsentrasjoner av hver forbindelse hver 48. time i 4 dager, og analysert for endepunktbiomarkører på dag 8 (figur 5C). Den eksperimentelle tidslinjen for DILI-analysen i MPS-platen er avbildet i figur 5D.
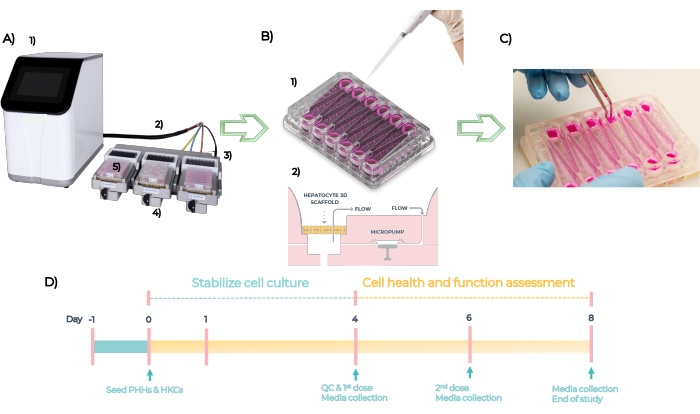
Figur 5: Det mikrofysiologiske systemet og eksperimentell tidslinje for en standard DILI-analyse. (A) Det mikrofysiologiske systemet med dets komponenter: kontroller (1), navlestreng (2), dokkingstasjon (3), MPS-driver (4) og LC12-plate (5). (B) Såing av PHH-er og HKC-er på LC12-plate på dag 1 (1) og innebygde mikropumper letter sirkulasjonen av cellekulturmedier med justerbare strømningshastigheter gjennom 3D-mikrovevene som er sådd på stillasene (2). (C) Ta ned stillasene på slutten av studien. (D) Eksperimentell tidslinje. Klikk her for å se en større versjon av dette tallet.
Når du utfører protokollen, er det viktig at en robust system QC-kontroll utføres før start, kontrollerer at systemet fungerer pneumatisk riktig og forbruksplatene blir visuelt inspisert og primet effektivt for å sikre jevn funksjonalitet på tvers av alle brønner. Å ha høykvalitets primære humane celler er avgjørende for denne protokollen, med hepatocytter kjent for å holde seg konsekvent i cellekultureksperimenter og danne 3D-interaksjoner. Tining av disse cellene er også et kritisk skritt, da primære hepatocytter ikke bør resuspenderes ved pipettering, da dette raskt kan føre til celledød. Å ha celle levedyktighet over 85% er avgjørende for vellykket såing, da store mengder cellulært rusk vil forstyrre 3D-mikrotissuedannelse. QC-kontroll av dannede levermikrovev på dag 4 er også viktig, og brukeren må sørge for at akseptable nivåer av LDH og urea måles, da parametere utenfor rekkevidde kan være en indikasjon på vevsdannelse av dårlig kvalitet og tillate enkel feilsøking. Endelig må hydrokortisonet som brukes i cellekulturmediet fremstilles friskt på bruksdagen for å forhindre uønsket nedbrytning som kan påvirke cellekulturens funksjonalitet, da det er nødvendig for å opprettholde hepatocyttenes metabolske funksjonalitet.
Til tross for å ha betydelig kompleksitet, inneholder leveren MPS ikke alle celletyper i den menneskelige leveren. Det er mulig å legge til flere celletyper i modellen24,29 for å øke fysiologisk relevans, men disse bør bare legges til med en klar begrunnelse for brukskonteksten. For å studere DILI PHH er nøkkelcelletypen, og inkorporering av HKC i denne modellen gjør det mulig å bestemme noen immunologiske responser. Det skal også bemerkes at PHH isolert fra humane lever og kommersielt tilgjengelige kryopreserverte PHH-er har en tendens til å demonstrere noen variasjoner fra parti til parti. Vi har vist her at denne protokollen gir reproduserbare resultater når den brukes med høykvalitets preparater av celler. Imidlertid forventes det noe mye variasjon, og dette kan overvinnes ytterligere ved å bruke mange flere givere. Disse begrensningene kan overvinnes ved å bruke hepatocyttlignende celler differensiert fra iPSC som rekapitulerer mange funksjonelle egenskaper til PHH, og som har blitt brukt i stoffutviklingsprosessen30. HKC-er viser også mye for mye variasjon og et høyt aktiveringsnivå ved tining; Derfor er HKC-givere forhåndsvalidert internt før bruk i eksperimentell cellekultur (kokultur med validerte PHH-er) og må ha lave nivåer av aktivering etter tining; Dette vurderes ved å måle biomarkørene IL-6 og TNF-alfa (se Tilleggsmateriale).
Dataene som presenteres her bekrefter at analysen kan oppdage DILI nøyaktig, noe som bidrar til å identifisere hepatotoxicants som kanskje ikke oppdages av 2D10,11 og til og med noen 3D-modeller. Data generert fra MPS brukes fortsatt ikke som standard av farmasøytisk industri for regulatoriske innleveringer eller legemiddelscreeningsformål på grunn av mangel på prosessstandardisering og harmonisering, inkludert reproduserbarhetmellom steder 20. Dataene og eksperimentelle tilnærminger som er demonstrert her, adresserer dette, og viser at levermodellen kan brukes rutinemessig og robust i DILI-skjermer for å nøyaktig forutsi ansvaret for nye forbindelser.
Ved å måle en rekke endepunkter for å produsere en “signatur av hepatotoksisitet”, som bidrar til å identifisere forbindelser med forskjellige nivåer av DILI-bekymring (inkludert forbindelser som ikke kan påvises ved andre in vitro-metoder) og deres mekanismer for toksisitet avslørt. Denne teknologien kan lukke gapet mellom tradisjonell cellekultur og dyremodeller på den ene siden og menneskelige kliniske studier, og fremme mot simulering av humane biologiske forhold for preklinisk vurdering av levertoksisitet som en del av legemiddelutviklingsprosessen.
Disclosures
The authors have nothing to disclose.
Acknowledgements
CN Bio Innovations Ltd. finansierte denne studien.
Materials
| 24 well cell culture cluster plates flat bottom | Corning | 3524 | |
| 96 well clear assay plates, flat bottom clear plastic | Greiner | 655101 | |
| 96 well plates black flat bottom | Corning | 3915 | |
| 96 Well White/Clear Bottom Plate, TC Surface | ThermoScientific | 165306 | |
| Advanced DMEM (1x) | Gibco | 12491015 | Cell culture media. |
| AssayMax Albumin ELISA Kit | AssayPro | EA3201-1 | Dilution 1:250. Time point Day 4, 6, and 8. |
| Cell Maintenance Cocktail B, (Primary Hepatocyte Maintenance Supplements) | Gibco | CM4000 | |
| CellTiter-Glo 3D Cell Viability Assay | Promega | G9682 | Dilution 1:1. Time point Day 8. |
| Chlorpromazine HCl | Sigma Aldrich | C8138 | |
| Chromacol blue lids, 9 mm Autosampler Vial Screw Thread Caps | ThermoScientific | 9-SCK(B)-ST1 | glass vial |
| Chromacol vials, 9 mm Clear Glass Screw Thread Vials | ThermoScientific | 2-SVW | |
| Class 2 Microbiological Safety Cabinets – Trimat2 1500 exhaust | Contained Air Solutions | ||
| Conical tubes 50 mL | Greiner | 227261 | |
| Cryopreserved Hepatocyte Recovery Medium (CHRM) | ThermoFisher Scientific | Gibco CM7000 | |
| Cryopreserved primary human hepatocytes | BioIVT Europe | Lot. RAS | |
| CytoTox 96 Cytotoxicty (LDH) Assay Kit | Promega | G1781 | Dilution – none. Time point Day 4, 6 and 8 |
| >Data analysis model used to generate the graph and EC:50 curves was nonlinear regression (curve fit) asymmetric sigmoidal, 5PL, where X is log(concentration | GraphPad Prism 9 | ||
| Disposable PES Filter Units 500mL | Fisher Scientific | 15913307 | |
| Disposable Pipette Basins 50ml | Fisher Scientific | 12369175 | |
| DMSO (Dimethyl sulfoxide) | Sigma-Aldrich | Sigma D2650 | |
| Dulbeco’s Phosphate Buffered Saline without Ca2+ and Mg2+ (D-PBS) | ThermoFisher Scientific | 14190-144 | |
| Easy Reader Conical Polypropylene Centrifuge Tubes 15 mL | Fisher Scientific | 11889640 | |
| Foetal bovine serum | Gibco | 10500064 | |
| Human ALT ELISA Kit | Abcam | ab 234578 | Dilution 1:5. Time point Day 6 and 8. |
| Human Cryopreserved Kupffer Cells | Lonza Europe | Lot. 190088KC | |
| hydrocortisone | Merck | H0888-1G | |
| Incubators models: New Brunswick Galaxy 170 S, New Brunswick Galaxy 170 R and CellXpert® C170. | Eppendorf | All serviced yearly; paperwork available upon request. | |
| Inverted Microscope | Leica DMIL LED | ||
| MPS know as Organ-on-a-Chip (OOC) | CN Bio Innovations Ltd. | ||
| MPS LC-12 plate | CN Bio Innovations Ltd. | ||
| Neubauer Improved C-Chip Disposable Haemocytometer (2 channel) | Cambridge Bioscience | DHC-N01-50 | |
| P450-Glo CYP3A4 Assay and Screening System | Promega | V9002 | Dilution – none. Time point Day 8 |
| PhysioMimix MPS platform | CN Bio Innovations Ltd. | ||
| Pioglitazone | MedChemExpress Tocris | HY-13956/CS-1700 | |
| Quantichrom Urea Assay Kit – Bioassay systems | Bioassay Systems | DY970-05 | Dilution 1:2 if initial reading is too high. Time point Day 4, 6 and 8. |
| Silica gel | Sigma-Aldrich | S7625 | |
| Software used to analyse and generate all the graphs was | GraphPad Prism 9 | ||
| Stripettes 10 mL | Fisher Scientific | 11839660 | |
| Stripettes 25 mL | Fisher Scientific | 11839181 | |
| Thawing plate Cocktail A, (Primary Hepatocyte Thawing and Plating Supplements) | Gibco | CM3000 | |
| Troglitazone | MedChemExpress Tocris | 97322-87-7 | |
| Trypan Blue Solution, 0.4% | Gibco | 15250061 | |
| Tubes 1.5 mL | Greiner | 616201 | |
| Weighing balance – model PA214C and AV213C | Ohaus Corp |
References
- Lisi, D. M. Drug-induced liver injury: An overview. US Pharmacist. 41 (12), 30-34 (2016).
- Kuna, L., et al. Models of drug induced liver injury (DILI)-current issues and future perspectives. Current Drug Metabolism. 19 (10), 830-838 (2018).
- Katarey, D., Verma, S. Drug-induced liver injury. Clinical Medicine. 16 (6), 104-109 (2016).
- Kullak-Ublick, G. A., et al. Drug-induced liver injury: recent advances in diagnosis and risk assessment Recent advances in clinical practice. Gut. 66, 1154-1164 (2017).
- Dirven, H., et al. Performance of pre-clinical models in predicting drug-induced liver injury in humans: a systematic review. Scientific Reports. 11 (1), 6403 (2021).
- Donato, M. T., Lahoz, A., Castell, J. V., Gomez-Lechon, M. J. Cell lines: a tool for in vitro drug metabolism studies. Current Drug Metabolism. 9 (1), 1-11 (2008).
- Wilkening, S., Stahl, F., Bader, A. Comparison of primary human hepatocytes and hepatoma cell line HepG2 with regard to their biotransformation properties. Drug Metabolism and Disposition. 31 (8), 1035-1042 (2003).
- Gerets, H. H. J., et al. Characterization of primary human hepatocytes, HepG2 cells, and HepaRG cells at the mRNA level and CYP activity in response to inducers and their predictivity for the detection of human hepatotoxins. Cell Biology and Toxicology. 28 (2), 69-87 (2012).
- Grainger, C. I., Greenwell, L. L., Lockley, D. J., Martin, G. P., Forbes, B. Culture of Calu-3 cells at the air interface provides a representative model of the airway epithelial barrier. Pharmaceutical Research. 23 (7), 1482-1490 (2006).
- Li, F., Cao, L., Parikh, S., Zuo, R. Three-dimensional spheroids with primary human liver cells and differential roles of kupffer cells in drug-induced liver injury. Journal of Pharmaceutical Sciences. 109 (6), 1912-1923 (2020).
- Proctor, W. R., et al. Utility of spherical human liver microtissues for prediction of clinical drug-induced liver injury. Archives of Toxicology. 91 (8), 2849-2863 (2017).
- Lin, C., Khetani, S. R. Advances in engineered liver models for investigating drug-induced liver injury. BioMed Research International. 2016, 1829148 (2016).
- Olson, H., et al. Concordance of the toxicity of pharmaceuticals in humans and in animals. Regulatory Toxicology and Pharmacology. 32 (1), 56-67 (2000).
- Bell, C. C., et al. Comparison of hepatic 2D sandwich cultures and 3D spheroids for long-term toxicity applications: A multicenter study. Toxicological Sciences. 162 (2), 655-666 (2018).
- Bell, C. C., et al. Characterization of primary human hepatocyte spheroids as a model system for drug-induced liver injury, liver function and disease. Scientific Reports. 6, 25187 (2016).
- Khetani, S. R., et al. Use of micropatterned co-cultures to detect compounds that cause drug-induced liver injury in humans. Toxicological Sciences. 132 (1), 107-117 (2013).
- Ma, X., et al. Deterministically patterned biomimetic human iPSC-derived hepatic model via rapid 3D bioprinting. Proceedings of the National Academy of Sciences of the united States of America. 113 (8), 2206-2211 (2016).
- Dieterle, P. Y. M., Dieterle, F. Tissue-specific, non-invasive toxicity biomarkers: translation from pre-clinical safety assessment to clinical safety monitoring. Expert Opinion on Drug Metabolism & Toxicology. 5 (9), 1023-1038 (2009).
- Rowe, C., et al. Perfused human hepatocyte microtissues identify reactive metabolite-forming and mitochondria-perturbing hepatotoxins. Toxicology in Vitro. 46, 29-38 (2018).
- Rubiano, A., et al. Characterizing the reproducibility in using a liver microphysiological system for assaying drug toxicity, metabolism, and accumulation. Clinical and Translational Science. 14 (3), 1049-1061 (2021).
- Tsamandouras, N., Kostrzewski, T., Stokes, C. L., Griffith, L. G., Hughes, D. J., Cirit, M. Quantitative assessment of population variability in hepatic drug metabolism using a perfused three-dimensional human liver microphysiological system. Journal of Pharmacology and Experimental Therapeutics. 360 (1), 95-105 (2017).
- Ortega-Prieto, A. M., et al. 3D microfluidic liver cultures as a physiological pre-clinical tool for hepatitis B virus infection. Nature Communications. 9 (1), 682 (2018).
- Kostrzewski, T., et al. Three-dimensional perfused human in vitro model of non-alcoholic fatty liver disease. World Journal of Gastroenterology. 23 (2), 204-215 (2017).
- Kostrzewski, T., et al. A microphysiological system for studying nonalcoholic steatohepatitis. Hepatology Communications. 4 (1), 77-91 (2020).
- Vacca, M., et al. Bone morphogenetic protein 8B promotes the progression of non-alcoholic steatohepatitis. Nature Metabolism. 2 (6), 514-531 (2020).
- Long, T. J., et al. Modeling therapeutic antibody-small molecule drug-drug interactions using a three-dimensional perfusable human liver co-culture platforms. Drug Metabolism and Disposition. 44, 1940-1948 (2016).
- Bai, J., Wang, C. Organoids and microphysiological systems: New tools for ophthalmic drug discovery. Frontiers in Pharmacology. 11, 407 (2020).
- Ribeiro, A. J. S., Yang, X., Patel, V., Madabushi, R., Strauss, D. G. Liver microphysiological systems for predicting and evaluating drug effects. Clinical Pharmacology & Therapeutics. 106 (1), 139-147 (2019).
- Clark, A. M., et al. A microphysiological system model of therapy for liver micrometastases hhs public access. Experimental Biology and Medicine (Maywood). 239 (9), 1170-1179 (2014).
- Qosa, H., Ribeiro, A. J. S., Hartman, N. R., Volpe, D. A. Characterization of a commercially available line of iPSC hepatocytes as models of hepatocyte function and toxicity for regulatory purposes. Journal of Pharmacological and Toxicological Methods. 110, 107083 (2021).

