骨格筋中の脂肪滴含量の線維タイプおよび細胞下特異的分析
Summary
増加する証拠は、骨格筋内の脂質の過剰な浸潤が脂肪毒性および糖尿病をもたらすことを示している。ここでは、線維型特異的な方法で脂肪滴のサイズ、密度、および細胞内分布を定量化するために、組織処理、Bodipyによる染色、画像取得、および分析を含む完全なプロトコルを提示する。
Abstract
筋症として知られている骨格筋脂質浸潤は、肥満および老化とともに増加する。筋症はまた、心血管疾患および癌のようないくつかの他の障害のための負の予後因子として最近発見されている。過剰な脂質浸潤は筋肉量と強度を低下させます。それはまた、総筋細胞内脂質含量、脂肪滴(LD)形態、および細胞内分布に依存して脂肪毒性およびインスリン抵抗性をもたらす。酸化繊維は脂質を利用する能力が大きいため、繊維タイプ(酸化性対解糖系)も重要です。病態生理学におけるそれらの決定的な意味合いのために、LDのダイナミクスおよび繊維タイプ特異的な方法での機能に関する詳細な研究が正当化される。
本明細書では、筋細胞内脂質含量の定量化およびLD形態および細胞内分布の分析をファイバータイプ特異的な様式で分析するための完全なプロトコールが提示される。この目的のために、連続筋凍結切片を、蛍光色素Bodipyおよびミオシン重鎖アイソフォームに対する抗体で染色した。このプロトコルは、異なる筋肉の同時処理を可能にし、時間を節約し、可能性のあるアーチファクトを回避し、フィジーで作成されたパーソナライズされたマクロのおかげで、LD分析の自動化も可能です。
Introduction
筋症として知られている骨格筋脂質浸潤は、肥満および老化とともに増加する。筋症は、筋肉量および強度およびインスリン感受性1と負の相関がある。さらに、最近の研究は、筋食症の程度が心血管疾患2、非アルコール性脂肪性肝疾患3、または癌4などの他の状態の予後因子として使用できることを示している。脂質は、筋細胞外脂質として、または筋線維内の骨格筋に筋細胞内脂質(IMCL)として蓄積することができる。IMCLsは、主に脂肪滴(LD)中のトリグリセリドとして貯蔵され、身体運動中に代謝燃料として使用される5,6。しかし、脂質供給が需要を上回ったり、ミトコンドリアが機能不全になったりすると、IMCLは代謝的に不健康な肥満の個人や2型糖尿病患者に見られるように、筋肉インスリン抵抗性に関与します7。興味深いことに、持久力アスリートは、高いインスリン感受性を維持しながら、2型糖尿病の肥満患者に見られるものと同様のレベルのIMCLを有する。この現象は「アスリートのパラドックス」8,9として記述され、筋肉LDのサイズ、密度、局在化、動態、脂質種の組成に関連する筋肉LDのより微妙な評価によって説明される。
第1に、LDサイズはインスリン感受性および体力に反比例する10、11。実際、より小さいLDは、リパーゼ作用に対して比較的大きな表面積を示し、したがって、潜在的に、脂質12を動員するより大きな能力を有する。第二に、LD密度(数/表面)は、インスリン作用において物議を醸す役割を果たしている8,10;しかし、アスリートでは増えているようです。第3に、表面膜のすぐ下に位置するLDs(サルコレマール下または末梢)は、中心膜よりもインスリン感受性に対してより有害な影響を及ぼすので、LDの細胞内局在化は重要である8、9、13。後者は、より大きな呼吸活動を有し、収縮に必要な高いエネルギー需要を満たすためにより専門化された中枢ミトコンドリアに燃料を供給する14。対照的に、末梢LDは、膜関連プロセスに関与するサルコレンマル下ミトコンドリアを供給する8。最後に、トリグリセリドを超えて、筋肉内の特定の複合脂質は、他の脂質よりも有害であり得る。例えば、ジアシルグリセロール、長鎖アシルCoA、およびセラミドは、トリグリセリドの代謝回転率が低いときに筋肉に蓄積し、それによってインスリンシグナル伝達を損なう9、15。「アスリートのパラドックス」に戻ると、持久力アスリートはI型(酸化)線維において高い回転率を有する多数のより小さな中枢LDを有するが、肥満および糖尿病患者は、II型(解糖系)線維において低いターンオーバー率を有するより大きな末梢LDを有する8,15,16。エネルギー貯蔵および放出におけるそれらの役割に加えて、誘導脂肪酸(FA)およびコートタンパク質(ペリリピン5)を介したLDは、FA酸化およびミトコンドリア生合成の転写調節に関与する重要なプレーヤーとしても機能し得る8。生理学および病態生理学におけるそれらの決定的な意味合いのために、LDsのダイナミクスおよび機能に関する詳細な研究が正当化される。
IMCLを研究するにはいくつかの手法がありますが、繊維固有の方法でLDのサイズ、密度、および分布を正確に定量化するのには適していません。例えば、磁気共鳴分光法によるIMCLの評価は、非侵襲的でありながら、繊維内のLDのサイズおよび正確な位置を研究するのに十分ではないレベルの分解能を提供し、繊維タイプ特異的ではない17,18。同様に、全筋ホモジネート19に対して行われる生化学的技術は、脂質の位置およびサイズを評価することができない。したがって、LDの形態および位置を分析するための最も適切な方法は、定量的透過電子顕微鏡13であるが、この技術は高価で時間がかかる。したがって、オイルレッドO(ORO)20,21、モノダンシルペンタン(MDH)22、またはボディピー23,24,25などの色素を含む調製物に対する共焦点蛍光イメージングは、これらの研究のための最良のツールとして浮上している。
ここでは、組織サンプリングと処理、ボディ染色、共焦点画像の取得と分析を含む完全なプロトコルが説明され、マウス筋肉凍結切片におけるLDのサイズ、数、および局在を定量化します。IMCLは酸化性繊維と解糖系繊維の間で均等に分布しておらず、各繊維タイプはLDダイナミクスを異なる方法で調節するので、IMCLの研究は繊維タイプ特異的でなければならない16,25,26,27。したがって、このプロトコルは、シリアルセクションの免疫蛍光を使用して、各ファイバーによって発現されるミオシン重鎖(MyHC)アイソフォームを同定します。このプロトコルのもう1つの利点は、解糖系(伸筋デジトルムロンガス、EDL)と酸化的(ヒラメ)筋肉を同時に処理して凍結前に並べて配置することです(図1)。この同時処理により、時間を節約できるだけでなく、サンプルの個別の処理による変動も回避されます。
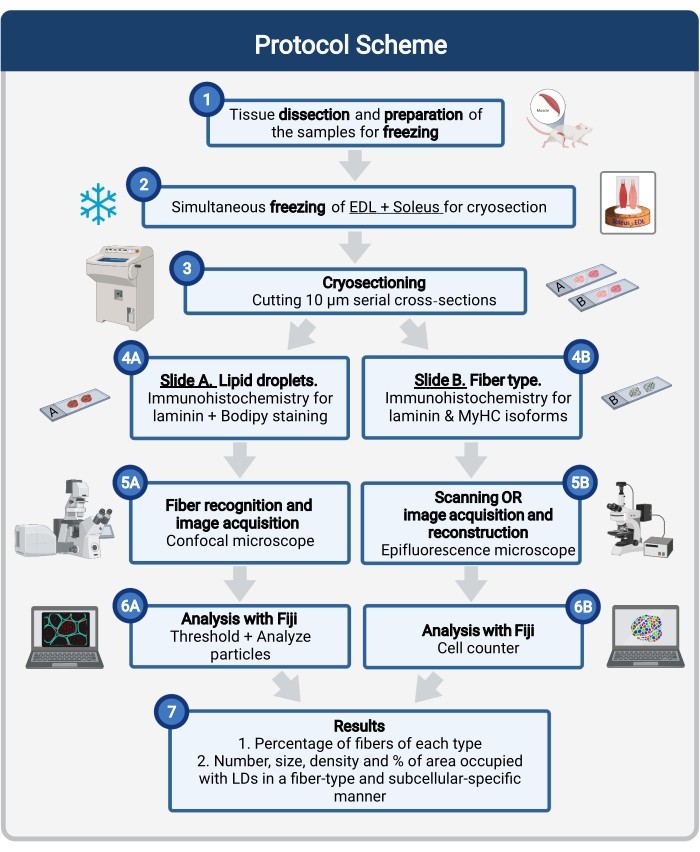
図1:手順の概略概要 筋肉解剖(1)後、類似の大きさの選択された筋肉が調製され、一緒に凍結される(2)。10μmの連続横切片は、クライオスタットを使用して得られ、接着スライドに直接取り付けられる(3)。2つの連続スライドから、第1の(4A)はラミニンについて免疫標識され、LDを認識するためにボディピーで染色され、第2の(4B)は筋線維タイプの認識のためにMyHCに対する抗体で免疫染色される。画像は、ボディピーの共焦点顕微鏡(5A)および筋線維タイプの落射蛍光顕微鏡(5B)を使用して取得される。フィジーでは、閾値を適用し、粒子(6A)を定量化して、LD(7)または計数細胞(6B)が占める総面積の数、平均サイズ、密度、および割合を取得して、セクション(7)内の各タイプの繊維の割合を得ることによって、画像が分析されます。略語: LDs = 脂肪滴;EDL = 伸筋デジトーラム・ロンガス;MyHCs=ミオシン重鎖アイソフォーム。 この図の拡大版を表示するには、ここをクリックしてください。
Protocol
Representative Results
Discussion
ここで詳述するプロトコルは、繊維タイプおよびサブセルラー特異的にBodipyでタグ付けされたLDを定量する効率的な方法を説明しています。近年、OROやスーダンブラックBなどの古典的な脂質色素は、中性脂質に結合する細胞透過性、親油性、蛍光色素(例えば、Bodipy)の新しい配列で置き換えられています。異なるコンジュゲートとして利用可能なBodipyは、異なる固定組織および細胞23、<sup clas…
Disclosures
The authors have nothing to disclose.
Acknowledgements
この研究は 、Fonds National de la Recherche Scientifique (FNRS-Crédit de Recherche J.0022.20)と Société Francophone du Diabète (SFD-Roche Diabetes Care)からの助成金によって支援されました。M.A.D.-L.d.C.はワロニー・ブリュッセル国際エクセレンス・プログラムからフェローシップを受けました。
著者らは、このプロトコルの開発に貢献したアリス・モニエと、画像取得プロセスにおける彼女の専門知識と技術的支援に対してキャロライン・ブーザンに感謝します。我々はまた、クライオスタット及び顕微鏡へのアクセスについて、2IP-IRECイメージングプラットフォーム(2IP-IRECイメージングプラットフォーム、実験臨床研究所、ルーヴァンカトリック大学、1200ブリュッセル、ベルギー)にも感謝する。最後に、著者らは、原稿の建設的な批判に対して、ニコラ・デュビュイソン、ロマン・ヴェルセル、ミシェル・アブー=サムラに感謝したい。これらの記事の数字のいくつかは、BioRender.com で作成されました。
Materials
| Equipment | |||
| AxioCam 506 mono 6 Mpix camera | Zeiss | ||
| AxioCam MRm 1.4MPix CCD camera | Zeiss | ||
| Chemical hood | Potteau Labo | EN-14175 | |
| Confocal microscope | Zeiss | LSM800 | |
| Cork discs (ø 20 mm, 3 mm thick) | Electron Microscopy Sciences | 63305 | |
| Cryo-Gloves | Tempshield | 16072252 | |
| Cryostat | Thermo Scientific | Microm Cryo Star HM 560 | |
| Dissecting Stereo Microscope SMZ745 | Nikon | ||
| Dry Ice | |||
| Dumont Forceps | F.S.T | 11295-10 | |
| Epifluorescence microscope | Zeiss | AxioImage-Apotome Z1 | |
| Extra Fine Bonn Scissors | F.S.T | 14084-08 | |
| FisherBrand Disposable Base Molds (0.7 x 0.7 cm) | ThermoFisher | 22-363-552 | Used to cut a piece to hold the muscle on the cork for freezing |
| Glass petri dish (H 25 mm, ø 150 mm) | BRAND Petri dish, MERK | BR455751 | Used to place the muscles on ice during dissection |
| ImmEdge Hydrophobic barrier PAP Pen | Vector Labs | H-4000 | Used to create an hidrophobic barrier around the muscle sections |
| Incubator | MMM Medcenter | Incucell 707 | |
| Microscope Cover Glasses (24×50 mm) | Assistent | 40990151 | |
| Microscope Slide Boxes | Kartell | 278 | Used as humid chambers for immunohistochemistry |
| Neck holder | Linie zwo | SB-035X-02 | Used as strap to hold the stainless steel tumbler |
| No 15 Sterile Carbon Steel Scalpel Blade | Swann-Morton | 0205 | |
| Paint brushes | Van Bleiswijck | Amazon B07W7KJQ2X | Used to handle cryosections |
| Permanent Marker Pen Black | Klinipath/VWR | 98307-R | Used to label slides |
| Pierce Fixation Forceps | F.S.T | 18155-13 | |
| Polystyrene Box | H 12 cm x L 25 cm x W 18 cm, used as a liquid nitrogen container and to transport the samples to the cryostat | ||
| Scalpel Handle, 125 mm (5"), No. 3 | Aesculap | BB073R | |
| Stainless Steel Cup 10oz | Eboxer | B07GFCBPFH | Tumbler to fill with isopentene for muscle freezing |
| Superfrost Ultra Plus slides | ThermoFisher | J1800AMNZ | |
| Surgical tweezers 1/2 teeth | Medische Vakhandel | 1303152 | Also called "Rat teeth tweezers" |
| Vannas Spring Scissors – 3 mm Cutting Edge | F.S.T | 15000-00 | |
| Weighing boats | VWR international | 611-2249 | |
| Whole-Slide Scanner for Fluorescence | Zeiss | Axio Scan.Z1 | |
| Reagents | |||
| Alexa Fluor 405 Goat Anti-Mouse IgG2b | Sigma-Aldrich | SAB4600477 | Used at a final concentration of 1:500 |
| Alexa Fluor 488 Goat Anti-Mouse IgG1 | ThermoFisher | A-21121 | Used at a final concentration of 1:500 |
| Alexa Fluor 568 Goat Anti-Mouse IgM | Abcam | ab175702 | Used at a final concentration of 1:1,000 |
| Alexa Fluor 647 goat anti rat-IgG (H+L) secondary antibody | ThermoFisher | A-21247 | Used at a final concentration of 1:500 |
| BODIPY-493/503 (4,4-difluoro-1,3,5,7,8-pentametil-4-bora-3a,4a-diaza-s-indaceno) | ThermoFisher | D3922 | Used at a final concentration of 1 µg/mL |
| BODIPY-558/568 C12 (4,4-Difluoro-5-(2-Thienyl)-4-Bora-3a,4a-Diaza-s-Indacene-3-Dodecanoic Acid) | ThermoFisher | D3835 | Used at a final concentration of 1 µg/mL |
| DAPI (4',6-diamidino-2-phenylindole) | ThermoFisher | D1306 | Used at a final concentration of 0.5 µg/mL |
| Dimethyl Sulfoxide (DMSO) | Sigma-Aldrich | D-8418 | Used to solve Bodipy for the 1 mg/mL stock solution. CAUTION: Toxic and flammable. Vapors may cause irritation. Manipulate in a fume hood. Avoid direct contact with skin. Wear rubber gloves, protective eye goggles. |
| Formaldehyde solution 4%, buffered, pH 6.9 | Sigma-Aldrich | 1004969011 | CAUTION: May cause an allergic skin reaction. Suspected of causing genetic defects. May cause cancer. Manipulate in a fume hood. Avoid direct contact with skin. Wear rubber gloves, protective eye goggles. |
| Isopentane GPR RectaPur | VWR international | 24872.298 | CAUTION: Extremely flammable liquid and vapor. May be fatal if swallowed and enters airways. May cause drowsiness or dizziness. Repeated exposure may cause skin dryness or cracking. Wear protective gloves/protective clothing/eye protection/face protection. |
| Liquid Nitrogen | CAUTION: Extremely cold. Wear gloves. Handle slowly to minimize boiling and splashing and in well ventilated areas. Use containers designed for low-temperature liquids. | ||
| Mouse on mouse Blocking Reagent | Vector Labs | MKB-2213-1 | Used at concentration of 1:30 |
| Myosin heavy chain Type I (BA-D5-s Primary Antibody) Gene: MYH7, monoclonal bovine anti mouse IgG2b | DSHB University of Iowa | BA-D5-supernatant | Used at a final concentration of 1:10 |
| Myosin heavy chain Type IIA (SC-71-s Primary Antibody) Gene: MYH2, Monoclonal bovine anti mouse IgG1 | DSHB University of Iowa | SC-71-supernatant | Used at a final concentration of 1:10 |
| Myosin heavy chain Type IIX (6H1-s Primary Antibody), Gene: MYH1, Monoclonal rabbit anti mouse IgM | Developmental Studies Hybridoma Bank, University of Iowa | 6H1-supernatant | Used at a final concentration of 1:5 |
| Normal Goat Serum (NGS) | Vector Labs | S-1000 | |
| PBS 0.1 M | Commonly used on histology laboratories | ||
| ProLong Gold Antifade Mountant | Invitrogen | P36930 | |
| Rat anti-Laminin-2 (α-2 Chain) primary antibody (monoclonal) | Sigma-Aldrich | L0663 | Used at a final concentration of 1:1,000 |
| Tissue-Tek O.C.T compound | Sakura | 4583 | |
| Software | |||
| Adobe Illustrator CC | Adobe Inc. | Used to design the figures | |
| Adobe Photoshop | Adobe Inc. | Confocal software | |
| BioRender | https://biorender.com/ | Used to design the figures | |
| Fiji/ImageJ | https://imagej.net/software/fiji/ | Used to analyse the acquired images | |
| Microsoft PowerPoint | Microsoft | Used to reconstruct the histology of the whole muscle after scanning the fiber types | |
| Zen Blue 2.6 | Zeiss | Used to reconstruct the histology of the whole muscle after scanning the fiber types |
References
- Correa-de-Araujo, R., et al. Myosteatosis in the context of skeletal muscle function deficit: an interdisciplinary workshop at the National Institute on Aging. Frontiers in Physiology. 11, 963 (2020).
- Miljkovic, I., et al. Greater skeletal muscle fat infiltration is associated with higher all-cause and cardiovascular mortality in older men. Journals of Gerontology Series A: Biomedical Sciences and Medical Sciences. 70 (9), 1133-1140 (2015).
- Nachit, M., et al. Myosteatosis rather than sarcopenia associates with non-alcoholic steatohepatitis in non-alcoholic fatty liver disease preclinical models. Journal of Cachexia, Sarcopenia, and Muscle. 12 (1), 144-158 (2021).
- Aleixo, G. F. P., et al. Myosteatosis and prognosis in cancer: Systematic review and meta-analysis. Critical Reviews in Oncology/Hematolgoy. 145, 102839 (2020).
- Gemmink, A., Schrauwen, P., Hesselink, M. K. C. Exercising your fat (metabolism) into shape: a muscle-centred view. Diabetologia. 63 (8), 1453-1463 (2020).
- van Loon, L. J. Use of intramuscular triacylglycerol as a substrate source during exercise in humans. Journal of Applied Physiology. 97 (4), 1170-1187 (2004).
- Coen, P. M., Goodpaster, B. H. Role of intramyocelluar lipids in human health. Trends in Endocrinology and Metabolism. 23 (8), 391-398 (2012).
- Seibert, J. T., Najt, C. P., Heden, T. D., Mashek, D. G., Chow, L. S. Muscle lipid droplets: cellular signaling to exercise physiology and beyond. Trends in Endocrinology and Metabolism. 31 (12), 928-938 (2020).
- Bergman, B. C., Goodpaster, B. H. Exercise and muscle lipid content, composition, and localization: influence on muscle insulin sensitivity. Diabetes. 69 (5), 848-858 (2020).
- Nielsen, J., Christensen, A. E., Nellemann, B., Christensen, B. Lipid droplet size and location in human skeletal muscle fibers are associated with insulin sensitivity. American Journal of Physiology-Endocrinology and Metabolism. 313 (6), 721-730 (2017).
- Covington, J. D., et al. Intramyocellular lipid droplet size rather than total lipid content is related to insulin sensitivity after 8 weeks of overfeeding. Obesity (Silver Spring). 25 (12), 2079-2087 (2017).
- Bosma, M. Lipid droplet dynamics in skeletal muscle). Experimental Cell Research. 340 (2), 180-186 (2016).
- Nielsen, J., et al. Increased subsarcolemmal lipids in type 2 diabetes: effect of training on localization of lipids, mitochondria, and glycogen in sedentary human skeletal muscle. American Journal of Physiology-Endocrinology and Metabolism. 298 (3), 706-713 (2010).
- Ferreira, R., et al. Subsarcolemmal and intermyofibrillar mitochondria proteome differences disclose functional specializations in skeletal muscle. Proteomics. 10 (17), 3142-3154 (2010).
- Barrett, J. S., Whytock, K. L., Strauss, J. A., Wagenmakers, A. J. M., Shepherd, S. O. High intramuscular triglyceride turnover rates and the link to insulin sensitivity: influence of obesity, type 2 diabetes and physical activity. Applied Physiology, Nutrition and Metabolism. , 1-14 (2022).
- Daemen, S., et al. Distinct lipid droplet characteristics and distribution unmask the apparent contradiction of the athlete’s paradox. Molecular Metabolism. 17, 71-81 (2018).
- Bredella, M. A., Ghomi, R. H., Thomas, B. J., Miller, K. K., Torriani, M. Comparison of 3.0 T proton magnetic resonance spectroscopy short and long echo-time measures of intramyocellular lipids in obese and normal-weight women. Journal of Magnetic Resonance Imaging. 32 (2), 388-393 (2010).
- Schrauwen-Hinderling, V. B., Hesselink, M. K., Schrauwen, P., Kooi, M. E. Intramyocellular lipid content in human skeletal muscle. Obesity (Silver Spring). 14 (3), 357-367 (2006).
- De Bock, K., et al. Evaluation of intramyocellular lipid breakdown during exercise by biochemical assay, NMR spectroscopy, and Oil Red O staining. American Journal of Physiology-Endocrinology and Metabolism. 293 (1), 428-434 (2007).
- Koopman, R., Schaart, G., Hesselink, M. K. Optimisation of oil red O staining permits combination with immunofluorescence and automated quantification of lipids. Histochemistry and Cell Biology. 116 (1), 63-68 (2001).
- Gueugneau, M., et al. Skeletal muscle lipid content and oxidative activity in relation to muscle fiber type in aging and metabolic syndrome. Journal of Gerontology Series A: Biomedical Sciences and Medical Sciences. 70 (5), 566-576 (2015).
- Gemmink, A., et al. Super-resolution microscopy localizes perilipin 5 at lipid droplet-mitochondria interaction sites and at lipid droplets juxtaposing to perilipin 2. Biochimica et Biophysica Acta-Molecular and Cell Biology of Lipids. 1863 (11), 1423-1432 (2018).
- Spangenburg, E. E., Pratt, S. J. P., Wohlers, L. M., Lovering, R. M. Use of BODIPY (493/503) to visualize intramuscular lipid droplets in skeletal muscle. Journal of Biomedicine and Biotechnology. 598358, (2011).
- Prats, C., et al. An optimized histochemical method to assess skeletal muscle glycogen and lipid stores reveals two metabolically distinct populations of type I muscle fibers. PLoS One. 8 (10), 77774 (2013).
- Strauss, J. A., Shepherd, D. A., Macey, M., Jevons, E. F. P., Shepherd, S. O. Divergence exists in the subcellular distribution of intramuscular triglyceride in human skeletal muscle dependent on the choice of lipid dye. Histochemistry and Cell Biology. 154 (4), 369-382 (2020).
- Shepherd, S. O., et al. Sprint interval and traditional endurance training increase net intramuscular triglyceride breakdown and expression of perilipin 2 and 5. Journal of Physiology. 591 (3), 657-675 (2013).
- Whytock, K. L., et al. A 7-day high-fat, high-calorie diet induces fibre-specific increases in intramuscular triglyceride and perilipin protein expression in human skeletal muscle. Journal of Physiology. 598 (6), 1151-1167 (2020).
- Wang, C., Yue, F., Kuang, S. Muscle histology characterization using h&e staining and muscle fiber type classification using immunofluorescence staining. Bio-Protocol. 7 (10), (2017).
- Meng, H., et al. Tissue triage and freezing for models of skeletal muscle disease. Journal of Visualized Experiments: JoVE. (89), e51586 (2014).
- Kumar, A., Accorsi, A., Rhee, Y., Girgenrath, M. Do’s and don’ts in the preparation of muscle cryosections for histological analysis. Journal of Visualized Experiments: JoVE. (99), e52793 (2015).
- Leiva-Cepas, F., et al. Laboratory methodology for the histological study of skeletal muscle. Archivos de Medicina del Deporte. 35 (186), 254-262 (2018).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Schiaffino, S., et al. Three myosin heavy chain isoforms in type 2 skeletal muscle fibres. Journal of Muscle Research & Cell Motility. 10 (3), 197-205 (1989).
- Komiya, Y., et al. Mouse soleus (slow) muscle shows greater intramyocellular lipid droplet accumulation than EDL (fast) muscle: fiber type-specific analysis. Journal of Muscle Research & Cell Motility. 38 (2), 163-173 (2017).
- Andrich, D. E., et al. Altered lipid metabolism impairs skeletal muscle force in young rats submitted to a short-term high-fat diet. Frontiers in Physiology. 9, 1327 (2018).
- Schiaffino, S. Fibre types in skeletal muscle: a personal account. Acta Physiologica. 199 (4), 451-463 (2010).
- Bloemberg, D., Quadrilatero, J. Rapid determination of myosin heavy chain expression in rat, mouse, and human skeletal muscle using multicolor immunofluorescence analysis. PLoS One. 7 (4), 35273 (2012).
- Gemmink, A., et al. Decoration of intramyocellular lipid droplets with PLIN5 modulates fasting-induced insulin resistance and lipotoxicity in humans. Diabetologia. 59 (5), 1040-1048 (2016).
- Askinas, C., et al. . Biophotonics Congress: Biomedical Optics Congress 2018 (Microscopy/Translational/Brain/OTS). , (2018).
- Morén, B., et al. EHD2 regulates adipocyte function and is enriched at cell surface-associated lipid droplets in primary human adipocytes. Molecular Biology of the Cell. 30 (10), 1147-1159 (2019).
- Benador, I. Y., et al. Mitochondria bound to lipid droplets have unique bioenergetics, composition, and dynamics that support lipid droplet expansion. Cell Metabolism. 27 (4), 869-885 (2018).
- de la Rosa Rodriguez, M. A., et al. Hypoxia-inducible lipid droplet-associated induces DGAT1 and promotes lipid storage in hepatocytes. Molecular Metabolism. 47, 101168 (2021).
- Jevons, E. F. P., Gejl, K. D., Strauss, J. A., Ørtenblad, N., Shepherd, S. O. Skeletal muscle lipid droplets are resynthesized before being coated with perilipin proteins following prolonged exercise in elite male triathletes. American Journal of Physiology-Endocrinology and Metabolism. 318 (3), 357-370 (2020).
- Ohsaki, Y., Maeda, T., Fujimoto, T. Fixation and permeabilization protocol is critical for the immunolabeling of lipid droplet proteins. Histochemistry and Cell Biology. 124 (5), 445-452 (2005).
- Prats, C., et al. Decrease in intramuscular lipid droplets and translocation of HSL in response to muscle contraction and epinephrine. Journal of Lipid Research. 47 (11), 2392-2399 (2006).
- Listenberger, L. L., Brown, D. A. Fluorescent detection of lipid droplets and associated proteins. Current Protocols in Cell Biology. , (2007).
- Xue, Y., Lim, S., Bråkenhielm, E., Cao, Y. Adipose angiogenesis: quantitative methods to study microvessel growth, regression and remodeling in vivo. Nature Protocols. 5 (5), 912-920 (2010).
- Muliyil, S., et al. ADAM17-triggered TNF signalling protects the ageing Drosophila retina from lipid droplet-mediated degeneration. The EMBO Journal. 39 (17), 104415 (2020).
- Yan, Q., et al. Autophagy activation contributes to lipid accumulation in tubular epithelial cells during kidney fibrosis. Cell Death Discovery. 4, 2 (2018).
- Coassin, S., et al. Investigation and functional characterization of rare genetic variants in the adipose triglyceride lipase in a large healthy working population. PLoS Genetics. 6 (12), 1001239 (2010).
- Daemen, S., van Zandvoort, M., Parekh, S. H., Hesselink, M. K. C. Microscopy tools for the investigation of intracellular lipid storage and dynamics. Molecular Metabolism. 5 (3), 153-163 (2016).
- Chen, Q., et al. Rab8a deficiency in skeletal muscle causes hyperlipidemia and hepatosteatosis by impairing muscle lipid uptake and storage. Diabetes. 66 (9), 2387-2399 (2017).
- Gemmink, A., et al. Decoration of myocellular lipid droplets with perilipins as a marker for in vivo lipid droplet dynamics: A super-resolution microscopy study in trained athletes and insulin resistant individuals. Biochimica et Biophysica Acta (BBA)-Molecular and Cell Biology of Lipids. 1866 (2), 158852 (2021).
- Bergman, B. C., Hunerdosse, D. M., Kerege, A., Playdon, M. C., Perreault, L. Localisation and composition of skeletal muscle diacylglycerol predicts insulin resistance in humans. Diabetologia. 55 (4), 1140-1150 (2012).

