Fibertype og subcellulær-spesifikk analyse av lipiddråpeinnhold i skjelettmuskulatur
Summary
Økende bevis indikerer at overdreven infiltrasjon av lipider inne i skjelettmuskulaturen resulterer i lipotoksisitet og diabetes. Her presenterer vi en komplett protokoll, inkludert vevsbehandling, farging med Bodipy, bildeanskaffelse og analyse, for å kvantifisere størrelsen, tettheten og subcellulær distribusjon av lipiddråper på en fiberspesifikk måte.
Abstract
Skjelettmuskel lipidinfiltrasjon, kjent som myosteatose, øker med fedme og aldring. Myosteatose har også nylig blitt oppdaget som en negativ prognostisk faktor for flere andre lidelser som kardiovaskulær sykdom og kreft. Overdreven lipidinfiltrasjon reduserer muskelmasse og styrke. Det resulterer også i lipotoksisitet og insulinresistens avhengig av totalt intramyocellulært lipidinnhold, lipiddråpe (LD) morfologi og subcellulær distribusjon. Fibertype (oksidativ vs glykolytisk) er også viktig, siden oksidative fibre har større kapasitet til å bruke lipider. På grunn av deres avgjørende implikasjoner i patofysiologi, er grundige studier på LD-dynamikk og funksjon på en fibertypespesifikk måte berettiget.
Heri presenteres en komplett protokoll for kvantifisering av intramyocellulært lipidinnhold og analyse av LD-morfologi og subcellulær distribusjon på en fibertypespesifikk måte. Til dette formål ble serielle muskelkryoser farget med fluorescerende fargestoff Bodipy og antistoffer mot myosin tunge kjede isoformer. Denne protokollen muliggjør samtidig behandling av forskjellige muskler, sparer tid og unngår mulige gjenstander, og takket være en personlig makro opprettet i Fiji, er automatisering av LD-analyse også mulig.
Introduction
Skjelettmuskel lipidinfiltrasjon, kjent som myosteatose, øker med fedme og aldring. Myosteatose er negativt korrelert med muskelmasse og styrke og med insulinfølsomhet1. Videre indikerer nyere studier at graden av myosteatose kan brukes som en prognostisk faktor for andre forhold som kardiovaskulær sykdom2, alkoholfri fettleversykdom3 eller kreft4. Lipider kan akkumuleres i skjelettmuskulatur mellom muskelfibre som ekstramyocellulære lipider eller i fibrene, som intramyocellulære lipider (IMCLer). IMCLer lagres hovedsakelig som triglyserider i lipiddråper (LDer) som brukes som metabolsk drivstoff under fysisk trening 5,6. Men når lipidforsyningen overstiger etterspørselen, eller når mitokondrier blir dysfunksjonelle, vil IMCLer bli implisert i muskelinsulinresistens, sett hos metabolsk usunne, overvektige individer og hos type 2 diabetespasienter7. Interessant nok har utholdenhetsutøvere lignende, om ikke høyere, nivåer av IMCLer til de som finnes hos overvektige pasienter med type 2 diabetes mellitus, samtidig som de opprettholder høy insulinfølsomhet. Dette fenomenet er beskrevet som “idrettsutøverens paradoks”8,9, og forklares av en mer nyansert vurdering av muskel-ID-er, relatert til deres størrelse, tetthet, lokalisering, dynamikk og lipidartsammensetning.
For det første er LD-størrelsen omvendt korrelert med insulinfølsomhet og fysisk form10,11. Faktisk viser mindre LP-er et relativt større overflateareal for lipasevirkning og har dermed potensielt større kapasitet til å mobilisere lipider12. For det andre spiller LD-tetthet (antall/overflate) en kontroversiell rolle i insulinvirkning 810; likevel ser det ut til å økes hos idrettsutøvere. For det tredje er subcellulær lokalisering av LP-er viktig, siden LP-er som ligger like under overflatemembranen (subsarcolemmal eller perifer) utøver en mer skadelig effekt på insulinfølsomhet enn sentrale 8,9,13. Sistnevnte gir drivstoff til sentrale mitokondrier, som har større åndedrettsaktivitet og er mer spesialiserte for å møte den høye energietterspørselen som kreves for sammentrekning14. Til sammenligning leverer perifere LDer subsarcolemmal mitokondrier, som er involvert i membranrelaterte prosesser8. Til slutt, utover triglyserider, kan spesifikke komplekse lipider i muskelen være mer skadelige enn andre. For eksempel kan diacylglyserol, langkjedet acyl-CoA og ceramider akkumuleres i muskel når triglyseridomsetningen er lav, og dermed svekke insulinsignalering 9,15. Tilbake til “idrettsutøverens paradoks”, utholdenhet idrettsutøvere har et høyt antall mindre sentrale ID-er med forhøyede omsetningshastigheter i type I (oksidative) fibre, mens overvektige og diabetikere har større perifere ID-er med lave omsetningshastigheter i type II (glykolytiske) fibre 8,15,16. I tillegg til deres rolle i energilagring og frigjøring, kan ID-er via avledede fettsyrer (FA) og et frakkprotein (perilipin 5) også fungere som kritiske aktører involvert i transkripsjonsreguleringen av FA-oksidasjon og mitokondriebiogenese8. På grunn av deres avgjørende implikasjoner i fysiologi og patofysiologi, er grundige studier av LDs dynamikk og funksjoner berettiget.
Selv om det finnes flere teknikker for å studere IMCLer, er de ikke alle egnet til å nøyaktig kvantifisere LD-størrelse, tetthet og distribusjon på en fiberspesifikk måte. For eksempel tilbyr vurderingen av IMCLer ved magnetisk resonansspektroskopi, mens den ikke er invasiv, et oppløsningsnivå som ikke er tilstrekkelig til å studere størrelsen og den nøyaktige plasseringen av LP-er i fiberen, og den er ikke fibertypespesifikk17,18. På samme måte kan biokjemiske teknikker utført på helmuskel homogenater19 ikke vurdere plasseringen og størrelsen på lipider. Følgelig er den mest tilstrekkelige metoden for å analysere LD morfologi og plassering kvantitativ overføring elektronisk mikroskopi13, men denne teknikken er dyr og tidkrevende. Derfor har konfekt fluorescensavbildning på preparater med fargestoffer som Oil Red O (ORO)20,21, monodansylpentane (MDH)22 eller Bodipy 23,24,25, dukket opp som det beste verktøyet for disse studiene.
Her beskrives en komplett protokoll, inkludert vevsprøvetaking og -behandling, Bodipy-farging og konfokal bildeanskaffelse og analyse for å kvantifisere LD-størrelse, antall og lokalisering i musemuskelroposer. Siden IMCLer ikke er jevnt fordelt mellom oksidative og glykolytiske fibre, og hver fibertype regulerer LD-dynamikken annerledes, må studien av IMCLer være fibertypespesifikk 16,25,26,27. Derfor bruker denne protokollen immunfluorescens på serielle seksjoner for å identifisere myosin heavy chain (MyHC) isoform(er) uttrykt av hver fiber. En annen fordel med denne protokollen er samtidig behandling av en glykolytisk (extensor digitorum longus, EDL) og en oksidativ (soleus) muskel plassert side om side før frysing (figur 1). Denne samtidige behandlingen sparer ikke bare tid, men unngår også variasjon på grunn av separat behandling av prøvene.
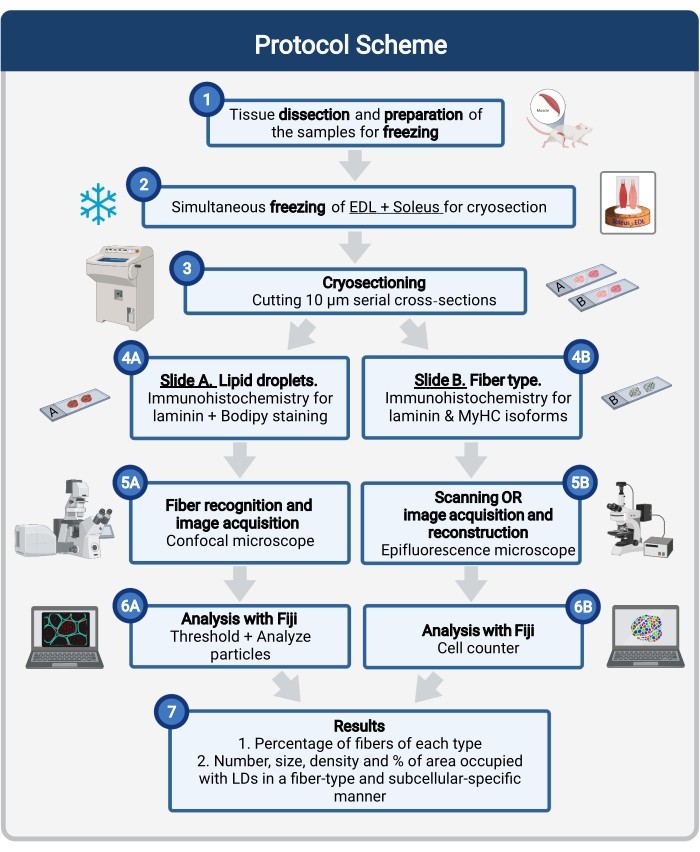
Figur 1: Skjematisk oversikt over prosedyren. Etter muskel disseksjon (1) fremstilles og fryses utvalgte muskler i tilsvarende størrelse sammen (2). Serielle tverrgående deler på 10 μm oppnås ved hjelp av en kryostat og monteres direkte på vedheftsskred (3). Fra to serielle lysbilder er den første (4A) immunmerket for laminin og farget med Bodipy for å gjenkjenne LD-er, og den andre (4B) er immunostert med antistoffer mot MyHCer for anerkjennelse av muskelfibertyper. Bilder er anskaffet ved hjelp av et konfokalt mikroskop for Bodipy (5A) og et epifluorescensmikroskop for muskelfibertyper (5B). Bilder analyseres i Fiji ved å bruke en terskel og kvantifiserende partikler (6A) for å oppnå tall, gjennomsnittlig størrelse, tetthet og prosentandel av det totale området okkupert av LP-er (7) eller telleceller (6B) for å oppnå prosentandelen fibre av hver type i seksjonen (7). Forkortelser: LDer = lipiddråper; EDL = extensor digitorum longus; MyHCs = myosin tunge kjede isoformer. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Protokollen som er beskrevet her beskriver en effektiv metode for å kvantifisere LDer merket med Bodipy på fiber- og subcellulær-spesifikk basis. De siste årene har klassiske lipidfarger, som ORO eller Sudan Black B, blitt erstattet med et nytt utvalg av cellegjennomtrengelige, lipofile, fluorescerende fargestoffer som binder seg til nøytrale lipider (f.eks. Bodipy). Tilgjengelig som forskjellige konjugater, bodipy har vist seg svært effektiv til å merke LD-er for å studere deres morfologi, dynamikk og interaksjo…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av tilskudd fra Fonds National de la Recherche Scientifique (FNRS-Crédit de Recherche J.0022.20) og Société Francophone du Diabète (SFD-Roche Diabetes Care).C.M.S. er mottaker av et ph.d.-stipend fra FRIA (FNRS). M.A.D.-L.d.C. fikk et stipend fra Wallonie-Bruxelles International Excellence Program.
Forfatterne takker Alice Monnier for hennes bidrag til utviklingen av denne protokollen og Caroline Bouzin for hennes ekspertise og tekniske hjelp i bildeoppkjøpsprosessen. Vi takker også 2IP-IREC bildeplattform for tilgang til kryostaten og mikroskopene (2IP-IREC Imaging Platform, Institute of Experimental and Clinical Research, Université Catholique de Louvain, 1200 Brussels, Belgia). Til slutt vil forfatterne takke Nicolas Dubuisson, Romain Versele og Michel Abou-Samra for konstruktiv kritikk av manuskriptet. Noen av tallene i denne artikkelen ble opprettet med BioRender.com.
Materials
| Equipment | |||
| AxioCam 506 mono 6 Mpix camera | Zeiss | ||
| AxioCam MRm 1.4MPix CCD camera | Zeiss | ||
| Chemical hood | Potteau Labo | EN-14175 | |
| Confocal microscope | Zeiss | LSM800 | |
| Cork discs (ø 20 mm, 3 mm thick) | Electron Microscopy Sciences | 63305 | |
| Cryo-Gloves | Tempshield | 16072252 | |
| Cryostat | Thermo Scientific | Microm Cryo Star HM 560 | |
| Dissecting Stereo Microscope SMZ745 | Nikon | ||
| Dry Ice | |||
| Dumont Forceps | F.S.T | 11295-10 | |
| Epifluorescence microscope | Zeiss | AxioImage-Apotome Z1 | |
| Extra Fine Bonn Scissors | F.S.T | 14084-08 | |
| FisherBrand Disposable Base Molds (0.7 x 0.7 cm) | ThermoFisher | 22-363-552 | Used to cut a piece to hold the muscle on the cork for freezing |
| Glass petri dish (H 25 mm, ø 150 mm) | BRAND Petri dish, MERK | BR455751 | Used to place the muscles on ice during dissection |
| ImmEdge Hydrophobic barrier PAP Pen | Vector Labs | H-4000 | Used to create an hidrophobic barrier around the muscle sections |
| Incubator | MMM Medcenter | Incucell 707 | |
| Microscope Cover Glasses (24×50 mm) | Assistent | 40990151 | |
| Microscope Slide Boxes | Kartell | 278 | Used as humid chambers for immunohistochemistry |
| Neck holder | Linie zwo | SB-035X-02 | Used as strap to hold the stainless steel tumbler |
| No 15 Sterile Carbon Steel Scalpel Blade | Swann-Morton | 0205 | |
| Paint brushes | Van Bleiswijck | Amazon B07W7KJQ2X | Used to handle cryosections |
| Permanent Marker Pen Black | Klinipath/VWR | 98307-R | Used to label slides |
| Pierce Fixation Forceps | F.S.T | 18155-13 | |
| Polystyrene Box | H 12 cm x L 25 cm x W 18 cm, used as a liquid nitrogen container and to transport the samples to the cryostat | ||
| Scalpel Handle, 125 mm (5"), No. 3 | Aesculap | BB073R | |
| Stainless Steel Cup 10oz | Eboxer | B07GFCBPFH | Tumbler to fill with isopentene for muscle freezing |
| Superfrost Ultra Plus slides | ThermoFisher | J1800AMNZ | |
| Surgical tweezers 1/2 teeth | Medische Vakhandel | 1303152 | Also called "Rat teeth tweezers" |
| Vannas Spring Scissors – 3 mm Cutting Edge | F.S.T | 15000-00 | |
| Weighing boats | VWR international | 611-2249 | |
| Whole-Slide Scanner for Fluorescence | Zeiss | Axio Scan.Z1 | |
| Reagents | |||
| Alexa Fluor 405 Goat Anti-Mouse IgG2b | Sigma-Aldrich | SAB4600477 | Used at a final concentration of 1:500 |
| Alexa Fluor 488 Goat Anti-Mouse IgG1 | ThermoFisher | A-21121 | Used at a final concentration of 1:500 |
| Alexa Fluor 568 Goat Anti-Mouse IgM | Abcam | ab175702 | Used at a final concentration of 1:1,000 |
| Alexa Fluor 647 goat anti rat-IgG (H+L) secondary antibody | ThermoFisher | A-21247 | Used at a final concentration of 1:500 |
| BODIPY-493/503 (4,4-difluoro-1,3,5,7,8-pentametil-4-bora-3a,4a-diaza-s-indaceno) | ThermoFisher | D3922 | Used at a final concentration of 1 µg/mL |
| BODIPY-558/568 C12 (4,4-Difluoro-5-(2-Thienyl)-4-Bora-3a,4a-Diaza-s-Indacene-3-Dodecanoic Acid) | ThermoFisher | D3835 | Used at a final concentration of 1 µg/mL |
| DAPI (4',6-diamidino-2-phenylindole) | ThermoFisher | D1306 | Used at a final concentration of 0.5 µg/mL |
| Dimethyl Sulfoxide (DMSO) | Sigma-Aldrich | D-8418 | Used to solve Bodipy for the 1 mg/mL stock solution. CAUTION: Toxic and flammable. Vapors may cause irritation. Manipulate in a fume hood. Avoid direct contact with skin. Wear rubber gloves, protective eye goggles. |
| Formaldehyde solution 4%, buffered, pH 6.9 | Sigma-Aldrich | 1004969011 | CAUTION: May cause an allergic skin reaction. Suspected of causing genetic defects. May cause cancer. Manipulate in a fume hood. Avoid direct contact with skin. Wear rubber gloves, protective eye goggles. |
| Isopentane GPR RectaPur | VWR international | 24872.298 | CAUTION: Extremely flammable liquid and vapor. May be fatal if swallowed and enters airways. May cause drowsiness or dizziness. Repeated exposure may cause skin dryness or cracking. Wear protective gloves/protective clothing/eye protection/face protection. |
| Liquid Nitrogen | CAUTION: Extremely cold. Wear gloves. Handle slowly to minimize boiling and splashing and in well ventilated areas. Use containers designed for low-temperature liquids. | ||
| Mouse on mouse Blocking Reagent | Vector Labs | MKB-2213-1 | Used at concentration of 1:30 |
| Myosin heavy chain Type I (BA-D5-s Primary Antibody) Gene: MYH7, monoclonal bovine anti mouse IgG2b | DSHB University of Iowa | BA-D5-supernatant | Used at a final concentration of 1:10 |
| Myosin heavy chain Type IIA (SC-71-s Primary Antibody) Gene: MYH2, Monoclonal bovine anti mouse IgG1 | DSHB University of Iowa | SC-71-supernatant | Used at a final concentration of 1:10 |
| Myosin heavy chain Type IIX (6H1-s Primary Antibody), Gene: MYH1, Monoclonal rabbit anti mouse IgM | Developmental Studies Hybridoma Bank, University of Iowa | 6H1-supernatant | Used at a final concentration of 1:5 |
| Normal Goat Serum (NGS) | Vector Labs | S-1000 | |
| PBS 0.1 M | Commonly used on histology laboratories | ||
| ProLong Gold Antifade Mountant | Invitrogen | P36930 | |
| Rat anti-Laminin-2 (α-2 Chain) primary antibody (monoclonal) | Sigma-Aldrich | L0663 | Used at a final concentration of 1:1,000 |
| Tissue-Tek O.C.T compound | Sakura | 4583 | |
| Software | |||
| Adobe Illustrator CC | Adobe Inc. | Used to design the figures | |
| Adobe Photoshop | Adobe Inc. | Confocal software | |
| BioRender | https://biorender.com/ | Used to design the figures | |
| Fiji/ImageJ | https://imagej.net/software/fiji/ | Used to analyse the acquired images | |
| Microsoft PowerPoint | Microsoft | Used to reconstruct the histology of the whole muscle after scanning the fiber types | |
| Zen Blue 2.6 | Zeiss | Used to reconstruct the histology of the whole muscle after scanning the fiber types |
References
- Correa-de-Araujo, R., et al. Myosteatosis in the context of skeletal muscle function deficit: an interdisciplinary workshop at the National Institute on Aging. Frontiers in Physiology. 11, 963 (2020).
- Miljkovic, I., et al. Greater skeletal muscle fat infiltration is associated with higher all-cause and cardiovascular mortality in older men. Journals of Gerontology Series A: Biomedical Sciences and Medical Sciences. 70 (9), 1133-1140 (2015).
- Nachit, M., et al. Myosteatosis rather than sarcopenia associates with non-alcoholic steatohepatitis in non-alcoholic fatty liver disease preclinical models. Journal of Cachexia, Sarcopenia, and Muscle. 12 (1), 144-158 (2021).
- Aleixo, G. F. P., et al. Myosteatosis and prognosis in cancer: Systematic review and meta-analysis. Critical Reviews in Oncology/Hematolgoy. 145, 102839 (2020).
- Gemmink, A., Schrauwen, P., Hesselink, M. K. C. Exercising your fat (metabolism) into shape: a muscle-centred view. Diabetologia. 63 (8), 1453-1463 (2020).
- van Loon, L. J. Use of intramuscular triacylglycerol as a substrate source during exercise in humans. Journal of Applied Physiology. 97 (4), 1170-1187 (2004).
- Coen, P. M., Goodpaster, B. H. Role of intramyocelluar lipids in human health. Trends in Endocrinology and Metabolism. 23 (8), 391-398 (2012).
- Seibert, J. T., Najt, C. P., Heden, T. D., Mashek, D. G., Chow, L. S. Muscle lipid droplets: cellular signaling to exercise physiology and beyond. Trends in Endocrinology and Metabolism. 31 (12), 928-938 (2020).
- Bergman, B. C., Goodpaster, B. H. Exercise and muscle lipid content, composition, and localization: influence on muscle insulin sensitivity. Diabetes. 69 (5), 848-858 (2020).
- Nielsen, J., Christensen, A. E., Nellemann, B., Christensen, B. Lipid droplet size and location in human skeletal muscle fibers are associated with insulin sensitivity. American Journal of Physiology-Endocrinology and Metabolism. 313 (6), 721-730 (2017).
- Covington, J. D., et al. Intramyocellular lipid droplet size rather than total lipid content is related to insulin sensitivity after 8 weeks of overfeeding. Obesity (Silver Spring). 25 (12), 2079-2087 (2017).
- Bosma, M. Lipid droplet dynamics in skeletal muscle). Experimental Cell Research. 340 (2), 180-186 (2016).
- Nielsen, J., et al. Increased subsarcolemmal lipids in type 2 diabetes: effect of training on localization of lipids, mitochondria, and glycogen in sedentary human skeletal muscle. American Journal of Physiology-Endocrinology and Metabolism. 298 (3), 706-713 (2010).
- Ferreira, R., et al. Subsarcolemmal and intermyofibrillar mitochondria proteome differences disclose functional specializations in skeletal muscle. Proteomics. 10 (17), 3142-3154 (2010).
- Barrett, J. S., Whytock, K. L., Strauss, J. A., Wagenmakers, A. J. M., Shepherd, S. O. High intramuscular triglyceride turnover rates and the link to insulin sensitivity: influence of obesity, type 2 diabetes and physical activity. Applied Physiology, Nutrition and Metabolism. , 1-14 (2022).
- Daemen, S., et al. Distinct lipid droplet characteristics and distribution unmask the apparent contradiction of the athlete’s paradox. Molecular Metabolism. 17, 71-81 (2018).
- Bredella, M. A., Ghomi, R. H., Thomas, B. J., Miller, K. K., Torriani, M. Comparison of 3.0 T proton magnetic resonance spectroscopy short and long echo-time measures of intramyocellular lipids in obese and normal-weight women. Journal of Magnetic Resonance Imaging. 32 (2), 388-393 (2010).
- Schrauwen-Hinderling, V. B., Hesselink, M. K., Schrauwen, P., Kooi, M. E. Intramyocellular lipid content in human skeletal muscle. Obesity (Silver Spring). 14 (3), 357-367 (2006).
- De Bock, K., et al. Evaluation of intramyocellular lipid breakdown during exercise by biochemical assay, NMR spectroscopy, and Oil Red O staining. American Journal of Physiology-Endocrinology and Metabolism. 293 (1), 428-434 (2007).
- Koopman, R., Schaart, G., Hesselink, M. K. Optimisation of oil red O staining permits combination with immunofluorescence and automated quantification of lipids. Histochemistry and Cell Biology. 116 (1), 63-68 (2001).
- Gueugneau, M., et al. Skeletal muscle lipid content and oxidative activity in relation to muscle fiber type in aging and metabolic syndrome. Journal of Gerontology Series A: Biomedical Sciences and Medical Sciences. 70 (5), 566-576 (2015).
- Gemmink, A., et al. Super-resolution microscopy localizes perilipin 5 at lipid droplet-mitochondria interaction sites and at lipid droplets juxtaposing to perilipin 2. Biochimica et Biophysica Acta-Molecular and Cell Biology of Lipids. 1863 (11), 1423-1432 (2018).
- Spangenburg, E. E., Pratt, S. J. P., Wohlers, L. M., Lovering, R. M. Use of BODIPY (493/503) to visualize intramuscular lipid droplets in skeletal muscle. Journal of Biomedicine and Biotechnology. 598358, (2011).
- Prats, C., et al. An optimized histochemical method to assess skeletal muscle glycogen and lipid stores reveals two metabolically distinct populations of type I muscle fibers. PLoS One. 8 (10), 77774 (2013).
- Strauss, J. A., Shepherd, D. A., Macey, M., Jevons, E. F. P., Shepherd, S. O. Divergence exists in the subcellular distribution of intramuscular triglyceride in human skeletal muscle dependent on the choice of lipid dye. Histochemistry and Cell Biology. 154 (4), 369-382 (2020).
- Shepherd, S. O., et al. Sprint interval and traditional endurance training increase net intramuscular triglyceride breakdown and expression of perilipin 2 and 5. Journal of Physiology. 591 (3), 657-675 (2013).
- Whytock, K. L., et al. A 7-day high-fat, high-calorie diet induces fibre-specific increases in intramuscular triglyceride and perilipin protein expression in human skeletal muscle. Journal of Physiology. 598 (6), 1151-1167 (2020).
- Wang, C., Yue, F., Kuang, S. Muscle histology characterization using h&e staining and muscle fiber type classification using immunofluorescence staining. Bio-Protocol. 7 (10), (2017).
- Meng, H., et al. Tissue triage and freezing for models of skeletal muscle disease. Journal of Visualized Experiments: JoVE. (89), e51586 (2014).
- Kumar, A., Accorsi, A., Rhee, Y., Girgenrath, M. Do’s and don’ts in the preparation of muscle cryosections for histological analysis. Journal of Visualized Experiments: JoVE. (99), e52793 (2015).
- Leiva-Cepas, F., et al. Laboratory methodology for the histological study of skeletal muscle. Archivos de Medicina del Deporte. 35 (186), 254-262 (2018).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Schiaffino, S., et al. Three myosin heavy chain isoforms in type 2 skeletal muscle fibres. Journal of Muscle Research & Cell Motility. 10 (3), 197-205 (1989).
- Komiya, Y., et al. Mouse soleus (slow) muscle shows greater intramyocellular lipid droplet accumulation than EDL (fast) muscle: fiber type-specific analysis. Journal of Muscle Research & Cell Motility. 38 (2), 163-173 (2017).
- Andrich, D. E., et al. Altered lipid metabolism impairs skeletal muscle force in young rats submitted to a short-term high-fat diet. Frontiers in Physiology. 9, 1327 (2018).
- Schiaffino, S. Fibre types in skeletal muscle: a personal account. Acta Physiologica. 199 (4), 451-463 (2010).
- Bloemberg, D., Quadrilatero, J. Rapid determination of myosin heavy chain expression in rat, mouse, and human skeletal muscle using multicolor immunofluorescence analysis. PLoS One. 7 (4), 35273 (2012).
- Gemmink, A., et al. Decoration of intramyocellular lipid droplets with PLIN5 modulates fasting-induced insulin resistance and lipotoxicity in humans. Diabetologia. 59 (5), 1040-1048 (2016).
- Askinas, C., et al. . Biophotonics Congress: Biomedical Optics Congress 2018 (Microscopy/Translational/Brain/OTS). , (2018).
- Morén, B., et al. EHD2 regulates adipocyte function and is enriched at cell surface-associated lipid droplets in primary human adipocytes. Molecular Biology of the Cell. 30 (10), 1147-1159 (2019).
- Benador, I. Y., et al. Mitochondria bound to lipid droplets have unique bioenergetics, composition, and dynamics that support lipid droplet expansion. Cell Metabolism. 27 (4), 869-885 (2018).
- de la Rosa Rodriguez, M. A., et al. Hypoxia-inducible lipid droplet-associated induces DGAT1 and promotes lipid storage in hepatocytes. Molecular Metabolism. 47, 101168 (2021).
- Jevons, E. F. P., Gejl, K. D., Strauss, J. A., Ørtenblad, N., Shepherd, S. O. Skeletal muscle lipid droplets are resynthesized before being coated with perilipin proteins following prolonged exercise in elite male triathletes. American Journal of Physiology-Endocrinology and Metabolism. 318 (3), 357-370 (2020).
- Ohsaki, Y., Maeda, T., Fujimoto, T. Fixation and permeabilization protocol is critical for the immunolabeling of lipid droplet proteins. Histochemistry and Cell Biology. 124 (5), 445-452 (2005).
- Prats, C., et al. Decrease in intramuscular lipid droplets and translocation of HSL in response to muscle contraction and epinephrine. Journal of Lipid Research. 47 (11), 2392-2399 (2006).
- Listenberger, L. L., Brown, D. A. Fluorescent detection of lipid droplets and associated proteins. Current Protocols in Cell Biology. , (2007).
- Xue, Y., Lim, S., Bråkenhielm, E., Cao, Y. Adipose angiogenesis: quantitative methods to study microvessel growth, regression and remodeling in vivo. Nature Protocols. 5 (5), 912-920 (2010).
- Muliyil, S., et al. ADAM17-triggered TNF signalling protects the ageing Drosophila retina from lipid droplet-mediated degeneration. The EMBO Journal. 39 (17), 104415 (2020).
- Yan, Q., et al. Autophagy activation contributes to lipid accumulation in tubular epithelial cells during kidney fibrosis. Cell Death Discovery. 4, 2 (2018).
- Coassin, S., et al. Investigation and functional characterization of rare genetic variants in the adipose triglyceride lipase in a large healthy working population. PLoS Genetics. 6 (12), 1001239 (2010).
- Daemen, S., van Zandvoort, M., Parekh, S. H., Hesselink, M. K. C. Microscopy tools for the investigation of intracellular lipid storage and dynamics. Molecular Metabolism. 5 (3), 153-163 (2016).
- Chen, Q., et al. Rab8a deficiency in skeletal muscle causes hyperlipidemia and hepatosteatosis by impairing muscle lipid uptake and storage. Diabetes. 66 (9), 2387-2399 (2017).
- Gemmink, A., et al. Decoration of myocellular lipid droplets with perilipins as a marker for in vivo lipid droplet dynamics: A super-resolution microscopy study in trained athletes and insulin resistant individuals. Biochimica et Biophysica Acta (BBA)-Molecular and Cell Biology of Lipids. 1866 (2), 158852 (2021).
- Bergman, B. C., Hunerdosse, D. M., Kerege, A., Playdon, M. C., Perreault, L. Localisation and composition of skeletal muscle diacylglycerol predicts insulin resistance in humans. Diabetologia. 55 (4), 1140-1150 (2012).

