توصيف رواية الإنسان Organotypic تقنية ثقافة الشبكية
Summary
تهدف هذه الدراسة إلى تطوير نموذج جديد لثقافة الشبكية العضوية البشرية (HORC) يمنع المساس بسلامة الشبكية أثناء المناولة العرضية. ويتحقق ذلك عن طريق زراعة شبكية العين مع الزجاجية الزائدة وظهارة الصباغ الشبكية الكامنة (RPE-choroid) والشد.
Abstract
استخدمت نماذج سابقة لثقافة الشبكية العضوية البشرية (HORC) شبكية العين المنفصلة. ومع ذلك ، من دون الدعم الهيكلي الذي يمنحه ظهارة صبغ الشبكية المشيمية (RPE -choroid) والشد ، يمكن بسهولة اختراق سلامة الشبكية الهشة. وكان الهدف من هذه الدراسة لتطوير نموذج HORC الرواية التي تحتوي على شبكية العين، RPE-المشيمية والشدة للحفاظ على سلامة الشبكية عند زراعة النباتات الشبكية.
بعد قطع محيط على طول الحويزل لإزالة القزحية والعدسة ، تم إجراء أربعة شقوق عميقة لتسطيح فنجان العين. على النقيض من بروتوكولات HORC السابقة ، تم استخدام التريفين لقطع ليس فقط من خلال شبكية العين ولكن أيضا RPE – المشيمية والشد. وقد تم استزراع النباتات ثلاثية الطبقات الناتجة عن ذلك لمدة 72 ساعة. تم استخدام تلطيخ الهيماتوكسيلين واليوسين (H &؛ E) لتقييم الهياكل التشريحية وتميزت النباتات السابقة الشبكية كذلك بالكيمياء المناعية (IHC) لخلايا المبرمج وسلامة خلايا مولر والتهاب الشبكية. لتأكيد إمكانية تحريض المرض ، تعرضت النباتات السابقة لارتفاع الجلوكوز (HG) والسيتوكينات المؤيدة للالتهابات (Cyt) ، لمحاكاة اعتلال الشبكية السكري (DR). تم استخدام فحص حبة Luminex المغناطيسي لقياس السيتوكينات ذات الصلة DR التي تم إطلاقها في وسيط الثقافة.
كشفت تلطيخ H &؛ E لاميلا الشبكية متميزة ونوى مدمجة في النباتات الشبكية مع الكامنة RPE-المشيمية والشديد، في حين أظهرت شبكية العين دون الهياكل الأساسية انخفاض سمك وفقدان النوى الشديدة. أشارت نتائج IHC إلى عدم وجود موت الخلايا المبرمج والتهاب الشبكية بالإضافة إلى الحفاظ على سلامة خلايا مولر. أظهرت فحوصات Luminex زيادة كبيرة في إفراز السيتوكينات المؤيدة للالتهابات المرتبطة ب DR في النباتات الشبكية المكشوفة ل HG + Cyt نسبة إلى مستويات خط الأساس عند 24 ساعة.
نجحنا في تطوير وتميز بروتوكول HORC جديد تم فيه الحفاظ على سلامة الشبكية دون موت الخلايا المبرمج أو التهاب الشبكية. وعلاوة على ذلك، فإن إفراز المؤشرات الحيوية المؤيدة للالتهابات المرتبطة ب DR عند تعريض النباتات الشبكية ل HG + Cyt يشير إلى أن هذا النموذج يمكن استخدامه لدراسات أمراض الشبكية القابلة للترجمة سريريا.
Introduction
شبكية العين هي بنية عين متخصصة للغاية مسؤولة عن تحويل الطاقة الضوئية الواردة إلى إشارات كهربائية ، والتي يتم معالجتها بعد ذلك من قبل الدماغ للإدراك البصري. شبكية العين البشرية يحتوي على مجموعة ديناميكية من أنواع الخلايا، نظمت للغاية في هيكل lamellar فريدة من نوعها تتكون من طبقتين متشابك وثلاث طبقات نواة1 (الشكل 1). يستمر التوازن الشبكي من خلال الاتصالات المعقدة بين الخلايا العصبية الشبكية والأوعية الدموية والأعصاب والأنسجة الضامة وRPE1. بسبب تشريح الشبكية المتطورة وعلم وظائف الأعضاء، وآليات العديد من أمراض الشبكية لا تزال غير مفهومة بشكل جيد2،3،4،5. لدراسة أمراض الشبكية بشكل أفضل ، تم تطوير نماذج HORC6و7و8و9. بالمقارنة مع الدراسات الحيوانية والثقافات المختبرية ، فإن نماذج HORC مفيدة لأنها تحتفظ بالبيئة الخلوية الديناميكية والتفاعلات العصبية الوعائية المعقدة في الموقع ، مما يوفر نموذجا جيدا للترجمة السريرية.
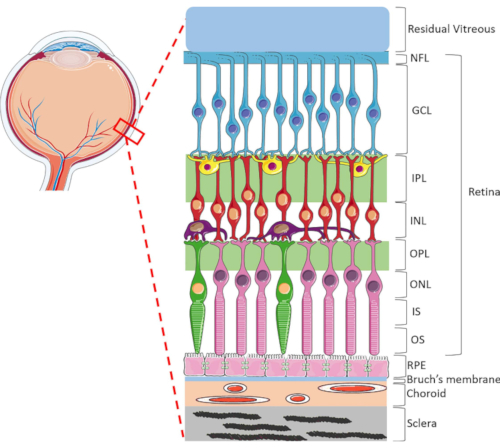
الشكل 1: هياكل العين الخلفية للعين البشرية. من الخلف إلى الخلف ، تكون طبقات الشبكية: طبقة الألياف العصبية (NFL) ، وطبقة خلايا العقدة (GCL) ، وطبقة شكل شبكي داخلي (IPL) ، وطبقة نووية داخلية (INL) ، وطبقة شكل شبكي خارجية (OPL) ، وطبقة نووية خارجية (ONL) ، والجزء الداخلي من المستقبل الضوئي (IS) ، وطبقة خارجية مستقبلات ضوئية (OS). وتشمل الخلايا داخل شبكية العين خلايا العقدة (الأزرق)، وخلايا الأماكرين (الصفراء)، والخلايا ثنائية القطب (الحمراء)، والخلايا الأفقية (الأرجواني)، وقضبان مستقبلات ضوئية (الوردي) ومخروط مستقبلات ضوئية (الأخضر). يقع الزجاجي الأمامي إلى شبكية العين. وRPE، غشاء بروش،choroid والشدة وتقع الخلفي إلى شبكية العين. لاحظ أن الصورة المعروضة هي مجرد تمثيل تخطيطي للشبكية وأن نسبة اتصال الخلايا/الشبكية داخل كل طبقة قد لا تكون مؤشرا على الإعداد في الجسم الحي. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
وقد تضمنت بروتوكولات HORC التي تم توصيفها سابقا6و7و8و9 فصل الشبكية عن RPE-choroid وsclera باستخدام التريفين الجراحي. ومع ذلك ، من دون الدعم الذي تقدمه هذه الهياكل الأساسية ، تصبح شبكية العين الشفافة واهية ، ويصعب التعامل معها ، ويمكن لأدوات مثل ملقط تعطيل سلامتها بسهولة. وعلاوة على ذلك، عزل شبكية العين في الثقافة دون RPE وقد ثبت أن يسبب موت الخلايا العقدية وانحطاط مستقبلات ضوئية10،11،12. وبالتالي، فإن بروتوكول HORC البديل الذي يقلل من فقدان سلامة الشبكية ويحااكي بشكل أفضل البيئة في الجسم الحي سيكون مفيدا. وهذا مهم بشكل خاص عند دراسة آليات أمراض الشبكية، حيث أن الإصابة الجسدية أثناء المناولة الإكسبلانت يمكن أن تدخل القطع الأثرية. لذلك ، كان الهدف من هذه الدراسة هو تطوير نموذج HORC جديد يتضمن RPE-choroid و sclera من أجل حماية سلامة الشبكية أثناء المناولة والثقافة.
من أجل تحقيق هذا الهدف، تم استخراج النباتات الشبكية “تقع” بين الزجاجي المتبقية وRPE-المشيمية الكامنة والصلابة. في النباتات الساندوتشات ، ويزن الزجاجي أسفل شبكية العين لمنع انفصال الشبكية وقابلة للطي ، في حين أن الصلبة الليفية الصعبة تعمل سقالة للدعم الهيكلي ونقطة اتصال للملقط. وعلاوة على ذلك، أظهرت النماذج الحيوانية أن الإبقاء على RPE في الثقافة يمكن أن يمنع انحطاط الشبكية وانتشار الدبقية، استجابة من خلايا مولر لإشارات الخطر مثل نقص الأكسيجة والالتهاب10،11،12.
لتوصيف النموذج، كانت ملطخة explants شبكية الساقين مع Hematoxylin وEosin (H & E) لتقييم الهياكل التشريحية والكيمياء المناعية (IHC) تم تنفيذها، وضع العلامات على النباتات السابقة مع محطة deoxynucleotidyl transferase dUTP وضع العلامات النهائية (TUNEL، علامة الخلية المبرمج)، البروتين الحمضي الرجفان الدبقية (GFAP، التهاب الشبكية وعلامة تنشيط الخلية مولر)، وفيمينتين، علامة على سلامة الخلية مولر. لتحديد ما إذا كان يمكن حث هذا النموذج لتطوير علامات المرض الجزيئي، تعرضت النباتات السابقة لارتفاع الجلوكوز (HG) مع السيتوكينات المؤيدة للالتهابات (Cyt) ، interleukin-1β (IL-1β) وعوامل نخر الورم α (TNF-α) ، وهي بيئة زراعة ثبت أنها تحاكي اعتلال الشبكية السكري (DR) في كل من نماذج الأمراض الخلوية والحيوانية13و14و15. استخدمت المقايسات Luminex في نموذج DR لقياس السيتوكينات الصادرة في الوسط الثقافي.
Protocol
Representative Results
Discussion
HORC هو حاليا النموذج الأكثر قابلية للترجمة سريريا في أبحاث الشبكية قبل السريرية. بالمقارنة مع نماذج زراعة الخلايا المختبرية ، يمكن أن يمثل HORC بشكل أفضل تشريح شبكية العين البشرية في الموقع ، من خلال الاحتفاظ بأنواع خلايا الشبكية الديناميكية واتصالاتها بالخلايا العصبية ، الأوعية الدموية و?…
Divulgations
The authors have nothing to disclose.
Acknowledgements
ويود المؤلفون أن يشكروا المتبرعين السخيين لأنسجة العيون والفريق من بنك العيون الوطني النيوزيلندي على دعمهم. وقد دعم هذا العمل ماليا بمنح مشاريع من صندوق موريس وفيليس بايكل ومؤسسة أوكلاند للبحوث الطبية (1117015). وتدعم مؤسسة بوكانان الخيرية إدارة المعهد. تقدم منحة CK من قبل جمعية نيوزيلندا لصندوق التعليم والبحوث لعلماء العيون (CC36812) ويتم تقديم منحة HHL من قبل مؤسسة بوكانان الخيرية.
Materials
| Disposable Biopsy Punches (5 mm) | Integra York PA Inc., USA | 21909-142 | Referred as surgical trephines in this article |
| Human Recombinant IL-1β | Peprotech, USA | 200-01B | Working concentration: 10 ng/mL |
| Human Recombinant TNF-a | Peprotech, USA | 300-01A | Working concentration: 10 ng/mL |
| DAPI (1 µg/mL) | Sigma Aldrich, Germany | #D9542 | Nuclear stain. Working dilution 1:1000 |
| DMEM/F-12, GlutaMAX supplement | Gibco, Thermofisher, Scientific Inc., USA | 10565018 | Dulbecco’s Modified Eagle Medium nutrient mixture F-12 containing a 1× antibiotics and antimycotics mixture (AA, 100× stock) |
| Fine Scissors – Sharp-Blunt | Fine Science Tools (F.S.T) | 14028-10 | Tips: Sharp-Blunt, Cutting Edge: 27mm, Length: 10cm, Alloy/Material: Stainless Steel, Serrated: No, Tip Shape: Straight |
| Graefe Forceps | Fine Science Tools (F.S.T) | 11050-10 | Length:10cm, Tip shape: Straight, Tips: Serrated, Tip Width: 0.8mm, Tip Dimensions:0.8 x 0.7mm, Alloy/Materials: Stainless Steel |
| Mouse monoclonal GFAP-Cy3 | Sigma Aldrich, Germany | #C9205 | Primary antibody conjugated to Cy3. Working dilution 1:1000. |
| Mouse monoclonal Vimentin-Cy3 | Sigma Aldrich, Germany | #C9080 | Primary antibody conjugated to Cy3. Working dilution 1:50. |
| Rabbit polyclonal TUNEL (In Situ Cell Death Detection Kit, Fluorescein) | Sigma Aldrich, Germany | #11684795910 | Primary antibody conjugated to Fluorescein-dUTP. Working dilution 1:10 with enzyme-buffer solution. |
References
- Kolb, H., Fernandez, E., Nelson, R. Facts and Figures Concerning the Human Retina. Webvision-The Organization of the Retina and Visual System. , (2005).
- Gemenetzi, M., De Salvo, G., Lotery, A. Central serous chorioretinopathy: an update on pathogenesis and treatment. Eye. 24 (12), 1743-1756 (2010).
- Buschini, E., Piras, A., Nuzzi, R., Vercelli, A. Age related macular degeneration and drusen: neuroinflammation in the retina. Progress in Neurobiology. 95 (1), 14-25 (2011).
- Chen, S. -. Y., et al. Current concepts regarding developmental mechanisms in diabetic retinopathy in Taiwan. Biomedicine. 6 (2), (2016).
- Kaaja, R., Loukovaara, S. Progression of retinopathy in type 1 diabetic women during pregnancy. Current Diabetes Reviews. 3 (2), 85-93 (2007).
- Azizzadeh Pormehr, L., et al. Human organotypic retinal flat-mount culture (HORFC) as a model for retinitis pigmentosa11. Journal of Cellular Biochemistry. 119 (8), 6775-6783 (2018).
- Fernandez-Bueno, I., et al. Time course modifications in organotypic culture of human neuroretina. Experimental Eye Research. 104, 26-38 (2012).
- Niyadurupola, N., Sidaway, P., Osborne, A., Broadway, D. C., Sanderson, J. The development of human organotypic retinal cultures (HORCs) to study retinal neurodegeneration. British Journal of Ophthalmology. 95 (5), 720-726 (2011).
- Osborne, A., Hopes, M., Wright, P., Broadway, D. C., Sanderson, J. Human organotypic retinal cultures (HORCs) as a chronic experimental model for investigation of retinal ganglion cell degeneration. Experimental Eye Research. 143, 28-38 (2016).
- Caffe, A., Visser, H., Jansen, H., Sanyal, S. Histotypic differentiation of neonatal mouse retina in organ culture. Current Eye Research. 8 (10), 1083-1092 (1989).
- Kaempf, S., Walter, P., Salz, A. K., Thumann, G. Novel organotypic culture model of adult mammalian neurosensory retina in co-culture with retinal pigment epithelium. Journal of Neuroscience Methods. 173 (1), 47-58 (2008).
- Liu, L., Cheng, S. -. H., Jiang, L. -. Z., Hansmann, G., Layer, P. G. The pigmented epithelium sustains cell growth and tissue differentiation of chicken retinal explants in vitro. Experimental Eye Research. 46 (5), 801-812 (1988).
- Kuo, C., Green, C. R., Rupenthal, I. D., Mugisho, O. O. Connexin43 hemichannel block protects against retinal pigment epithelial cell barrier breakdown. Acta Diabetologica. 57 (1), 13-22 (2020).
- Mugisho, O. O., et al. The inflammasome pathway is amplified and perpetuated in an autocrine manner through connexin43 hemichannel mediated ATP release. Biochimica et Biophysica Acta (BBA)-General Subjects. 1862 (3), 385-393 (2018).
- Mugisho, O. O., et al. Intravitreal pro-inflammatory cytokines in non-obese diabetic mice: Modelling signs of diabetic retinopathy. PLoS ONE. 13 (8), 0202156 (2018).
- . R&D Systems, I Available from: https://www.rndsystems.com/protocol-types/luminex (2020)
- Nakazawa, T., et al. Attenuated glial reactions and photoreceptor degeneration after retinal detachment in mice deficient in glial fibrillary acidic protein and vimentin. Investigative Ophthalmology, Visual Science. 48 (6), 2760-2768 (2007).
- Okada, M., Matsumura, M., Ogino, N., Honda, Y. Müller cells in detached human retina express glial fibrillary acidic protein and vimentin. Graefe’s Archive for Clinical and Experimental Ophthalmology. 228 (5), 467-474 (1990).
- Murali, A., Ramlogan-Steel, C. A., Andrzejewski, S., Steel, J. C., Layton, C. J. Retinal explant culture: A platform to investigate human neuro-retina. Clinical & Experimental Ophthalmology. 47 (2), 274-285 (2019).
- Koleva-Georgieva, D. N., Sivkova, N. P., Terzieva, D. Serum inflammatory cytokines IL-1beta, IL-6, TNF-alpha and VEGF have influence on the development of diabetic retinopathy. Folia Medica (Plovdiv). 53 (2), 44-50 (2011).
- Lee, J. -. H., et al. Cytokine profile of peripheral blood in type 2 diabetes mellitus patients with diabetic retinopathy. Annals of Clinical & Laboratory Science. 38 (4), 361-367 (2008).
- Chorostowska-Wynimko, J., et al. In vitro angiomodulatory activity of sera from type 2 diabetic patients with background retinopathy. Journal of Physiology and Pharmacology: An Official Journal of the Polish Physiological Society. 56, 65-70 (2005).
- Khalifa, R. A., Khalef, N., Moemen, L. A., Labib, H. M. The role interleukin 12 (IL-12), interferon-inducible protein 10 (IP-10) and Interleukin 18 (IL-18) in the angiogenic activity of diabetic retinopathy. Research Journal of Medicine and Medical Sciences. 4, 510-514 (2009).
- Zhou, J., Wang, S., Xia, X. Role of intravitreal inflammatory cytokines and angiogenic factors in proliferative diabetic retinopathy. Current Eye Research. 37 (5), 416-420 (2012).
- Song, Z., et al. Increased intravitreous interleukin-18 correlated to vascular endothelial growth factor in patients with active proliferative diabetic retinopathy. Graefe’s Archive for Clinical and Experimental Ophthalmology. 252 (8), 1229-1234 (2014).
- Louie, H. H., Shome, A., Kuo, C. Y. J., Rupenthal, I. D., Green, C. R., Mugisho, O. O. Connexin43 hemichannel block inhibits NLRP3 inflammasome activation in a human retinal explant model of diabetic retinopathy. Experimental Eye Research. , (2020).

