Unchelated 가돌리늄위한 앱 타머 기반 센서 (III)
Summary
The use of polydeoxynucleotide (44-mer aptamer) molecules for sensing unchelated gadolinium(III) ion in an aqueous solution is described. The presence of the ion is detected via an increase in the fluorescence emission of the sensor.
Abstract
A method for determining the presence of unchelated trivalent gadolinium ion (Gd3+) in aqueous solution is demonstrated. Gd3+ is often present in samples of gadolinium-based contrast agents as a result of incomplete reactions between the ligand and the ion, or as a dissociation product. Since the ion is toxic, its detection is of critical importance. Herein, the design and usage of an aptamer-based sensor (Gd-sensor) for Gd3+ are described. The sensor produces a fluorescence change in response to increasing concentrations of the ion, and has a limit of detection in the nanomolar range (~100 nM with a signal-to-noise ratio of 3). The assay may be run in an aqueous buffer at ambient pH (~7 – 7.4) in a 384-well microplate. The sensor is relatively unreactive toward other physiologically relevant metal ions such as sodium, potassium, and calcium ions, although it is not specific for Gd3+ over other trivalent lanthanides such as europium(III) and terbium(III). Nevertheless, the lanthanides are not commonly found in contrast agents or the biological systems, and the sensor may therefore be used to selectively determine unchelated Gd3+ in aqueous conditions.
Introduction
기술의 고유의 감도에 의해 제한된다 임상 진단에서 자기 공명 영상 (MRI)의 중요성이 증가는 신규 가돌리늄 계 조영제 (GBCAs 1)의 개발에 대한 연구의 빠른 성장을 가져왔다. GBCAs은 이미지 품질을 개선하기 위해 투여되는 분자이며, 그들은 일반적으로 여러 자리 리간드에 배위 3가 가돌리늄 이온 (하나님 3+)의 화학 구조를 갖는다. 이 복합체는 독성 3+ unchelated 하나님으로 매우 중요합니다; 이는 신장 질환 또는 장애이 일부 환자에서 신원 성 전신 섬유증의 발병과 연관되어있다. 따라서, 수성 자유 이온을 검출하는 GBCAs의 안전을 확보하는 수단이있다. GBCA 솔루션 unchelated 하나님 3+의 존재는 종종 리간드 및 이온 복합체의 해리 또는 displacemen 간의 불완전한 반응의 결과다른 생물학적 금속 양이온 (3)에 의한 t.
현재 하나님 3+, 융통성 및 적응성 (4)의 측면에서 크로마토 그래피 및 / 또는 분광 최고 순위를 의존들의 존재를 결정하기 위해 사용하는 여러 기술 중. 강점 중 높은 감도 및 정확도 (리스트를, 복수 하나님 3+ 복합체의 동시 정량 (인간 혈청 5 소변 헤어 6 폐수 7 및 조영제 제제 8 등) 다양한 시료 매트릭스를 분석하는 능력이다 연구의 2013 년 이전은 Telgmann 등.) (4)에 의해 종합적인 검토에 설명되어 있습니다. 유일한 단점은 이들 방법 중 몇몇은 몇몇 실험실에 액세스 할 수있다 (예 : 유도 결합 플라즈마 질량 분석)을 측정 장치 (4)를 필요로한다는 것이다. 연구 및 개념 증명 수준 AR에 참신한 GBCA 검색의 맥락elatively 더욱 편리하고 신속하고 비용 효율적인 분광 기반 방법 (예 : 비스 – UV 흡수 또는 형광 등) 유용한 대안이 될 수있다. 마음에 이러한 응용 프로그램으로, 수성 하나님 3+에 대한 형광 앱 타머 기반 센서 (9)을 개발 하였다.
앱 타머 (GD-앱 타머)는 지수 농축 (SELEX) (9)에 의한 리간드의 체계적인 진화의 과정을 통해 분리하여 염기의 특정 순서와 44 염기 길이의 단일 가닥 DNA 분자이다. 형광 센서에 앱 타머에 적응하기 위해, 형광 물질은 13 상보적인 염기 (도 1)를 통해 급냉 스트랜드 (QS)와 혼성화되는 가닥의 5 '말단에 부착된다. QS는 3 '말단에 어두운 소광 분자 태그입니다. 1 이루어지는 하나님 3+ 센서 (GD-센서)의 부재에있어서 : 각각 GD-앱 타머 및 QS 2 몰비 최소 형광 방출 인해 t있을 것이다소광에 형광에서 오 에너지 전달. 수성 하나님 3+의 첨가는 형광 방출 증가의 결과로, GD-앱 타머에서 QS를 대체 할 것이다.
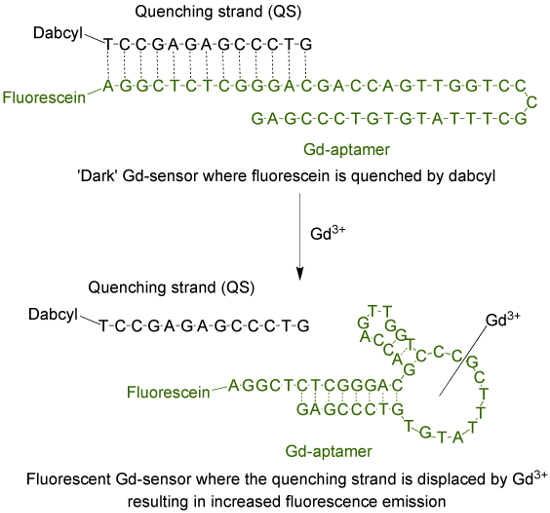
형광 (형광)과 dabcyl 태그로 13베이스 긴 담금질 가닥 (QS) 태그로 44베이스 긴 앱 타머 (GD-앱 타머) (어두운 소광)로 구성되어 그림 1. 센서 (하나님 센서) . unchelated 하나님 3+의 부재에서, 센서의 형광이 최소이다. 하나님 3+의 첨가에 의해, QS의 변위가 발생하고, 형광 발광의 증가가 관찰된다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
현재 존재 한 일반적으로 사용되는 광학적 기반 방법에 대한 검출수성 하나님의 3 이상을 보내고. 이 분석은 이온 10 킬에 따라 433 nm의 573에서 최대 흡수 파장의 변화를 겪는다 분자 크 실레 놀 오렌지를 사용합니다. 이들 두 흡수 최대 값의 비율은 unchelated 하나님 3+의 양을 정량화 할 수있다. 두 가지 방법은, 타겟 선택도, 정량 분석의 선형 범위 및 검출 양상 (예 : pH 및 사용되는 버퍼 용액의 조성과 같은) 상이한 반응 조건을 가지고, 상기 앱 타머 센서는 크 실레 놀 오렌지 분석에 대한 대안 (또는 보완 될 수있다)는 9.
Protocol
Representative Results
Discussion
앱타 머는 기반 GD-센서 관측 unchelated 하나님 3+의 농도에 비례하는 형광 방출의 증가 사용. 사용한 시료의 양을 최소화하기 위해, 분석은 웰 당 45 μL의 총 샘플 부피의 384 웰 마이크로 플레이트에서 실행될 수있다. 이 설계에서, 플루오 레세 인 (FAM) 및 dabcyl DAB ()의 선택은 주로 시약의 비용에 기초 하였다 발광 파장, 형광의 다른 쌍을 수정 및 소광 제 (11)를 사용할 수있다.
<p class…Divulgazioni
The authors have nothing to disclose.
Acknowledgements
We would like to gratefully acknowledge Dr. Milan N Stojanovic from Columbia University, New York, NY for valuable scientific input. This work is supported by funding from the California State University East Bay (CSUEB) and the CSUEB Faculty Support Grant-Individual Researcher. O.E., T.C., and A.L. were supported by the CSUEB Center for Student Research (CSR) Fellowship.
Materials
| Gd-aptamer | IDTDNA | Input sequence and fluorophore modification in the order form | A fluorophore with a different emission wavelength may be used. The aptamer may also be ordered from another company. |
| Quenching strand | IDTDNA | Input sequence and quencher modification in the order form | A different quencher for optimal energy transfer from the fluorophore may be used. The aptamer may also be ordered from another company. |
| Molecular biology grade water | No specific manufacturer, both DEPC or non-DEPC treated work equally well | ||
| Gadolinium(III) chloride anhydrous | Strem | 936416 | Toxic |
| HEPES | Fisher Scientific | BP310-500 | |
| Magnesium chloride anhydrous | MP Biomedicals | 0520984480 – 100 g | |
| Sodium Chloride | Acros Organics | 327300025 | |
| Potassium chloride | Fisher Scientific | P333-500 | |
| Sodium hydroxide, pellets | Fisher Scientific | BP359 | Corrosive |
| Hydrochloric acid | Fisher Scientific | SA49 | Toxic and corrosive |
| 384-well low flange black flat bottom polystyrene NBS plates | Corning | 3575 | Plates which are suitable for fluorescence reading are required. |
| Nalgene Rapid-Flow sterile disposable bottle top filter | Thermo Scientific | 5680020 | The bottle top is fitted with 0.2 micron PES membrane |
| Disposable sterile bottles 250 mL | Corning | 430281 | A larger or smaller bottle may be used |
| 1.5 mL microcentrifuge tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| 0.2 mL PCR tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Micropipets | No specific manufacturer | ||
| Pipet tips (non filter) of appropriate sizes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Name of Equipment | |||
| Plate reader | Biotek Synergy H1 | Plate readers from other manufacturers would work equally well |
Riferimenti
- Shen, C., New, E. J. Promising strategies for Gd-based responsive magnetic resonance imaging contrast agents. Curr. Opin. Chem. Biol. 17 (2), 158-166 (2013).
- Cheong, B. Y. C., Muthupillai, R. Nephrogenic systemic fibrosis: a concise review for cardiologists. Tex. Heart Inst. J. 37 (5), 508-515 (2010).
- Hao, D., Ai, T., Goerner, F., Hu, X., Runge, V. M., Tweedle, M. MRI contrast agents: basic chemistry and safety. J Magn. Reson. Imaging. 36 (5), 1060-1071 (2012).
- Telgmann, L., Sperling, M., Karst, U. Determination of gadolinium-based MRI contrast agents in biological and environmental samples: a review. Anal. Chim. Acta. 764, 1-16 (2013).
- Frenzel, T., Lengsfeld, P., Schirmer, H., Hütter, J., Weinmann, H. -. J. Stability of gadolinium-based magnetic resonance imaging contrast agents in human serum at 37 degrees C. Invest. Radiol. 43 (12), 817-828 (2008).
- Loreti, V., Bettmer, J. Determination of the MRI contrast agent Gd-DTPA by SEC-ICP-MS. Anal. Bioanal. Chem. 379 (7), 1050-1054 (2004).
- Telgmann, L., et al. Speciation and isotope dilution analysis of gadolinium-based contrast agents in wastewater. Environ. Sci. Technol. 46 (21), 11929-11936 (2012).
- Cleveland, D., et al. Chromatographic methods for the quantification of free and chelated gadolinium species in MRI contrast agent formulations. Anal. Bioanal. Chem. 398 (7), 2987-2995 (2010).
- Edogun, O., Nguyen, N. H., Halim, M. Fluorescent single-stranded DNA-based assay for detecting unchelated gadolinium(III) ions in aqueous solution. Anal. Bioanal. Chem. 408 (15), 4121-4131 (2016).
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Med. Mol. Imaging. 1 (5), 184-188 (2006).
- Johansson, M. K. Choosing reporter-quencher pairs for efficient quenching through formation of intramolecular dimers. Methods Mol. Biol. 335, 17-29 (2006).
- Sherry, A. D., Caravan, P., Lenkinski, R. E. A primer on gadolinium chemistry. J. Magn. Reson. Imaging. 30 (6), 1240-1248 (2009).
- Shakhverdov, T. A. A cross-relaxation mechanism of fluorescence quenching in complexes of lanthanide ions with organic ligands. Opt. Spectrosc. 95 (4), 571-580 (2003).
- Brittain, H. G. Submicrogram determination of lanthanides through quenching of calcein blue fluorescence. Anal. Chem. 59 (8), 1122-1125 (1987).

