Questo protocollo dimostra l'attività chaperone della proteina da shock termico 70 (Hsp70). Le cellule dnaK756 di E. coli fungono da modello per il test in quanto ospitano un Hsp70 nativo e funzionalmente compromesso, che le rende suscettibili allo stress termico. L'introduzione eterologa di Hsp70 funzionale salva il deficit di crescita delle cellule.
Research Article
Test di complementazione basato su Escherichia coli per studiare la funzione chaperone della proteina da shock termico 70
In This Article
Summary
Abstract
La proteina da shock termico 70 (Hsp70) è una proteina conservata che facilita il ripiegamento di altre proteine all'interno della cellula, rendendola uno chaperone molecolare. Mentre Hsp70 non è essenziale per le cellule di E. coli che crescono in condizioni normali, questo chaperone diventa indispensabile per la crescita a temperature elevate. Poiché Hsp70 è altamente conservato, un modo per studiare la funzione chaperone dei geni Hsp70 di varie specie è quello di esprimerli eterologamente in ceppi di E. coli che sono carenti di Hsp70 o che esprimono un Hsp70 nativo che è funzionalmente compromesso. Le cellule dnaK756 di E. coli non sono in grado di supportare il DNA del batteriofago λ. Inoltre, il loro Hsp70 nativo (DnaK) mostra un'elevata attività ATPasica mentre dimostra una ridotta affinità per GrpE (fattore di scambio nucleotidico Hsp70). Di conseguenza, le cellule di E. coli dnaK756 crescono adeguatamente a temperature comprese tra 30 °C e 37 °C, ma muoiono a temperature elevate (>40 °C). Per questo motivo, queste cellule fungono da modello per lo studio dell'attività chaperone di Hsp70. Qui, descriviamo un protocollo dettagliato per l'applicazione di queste cellule per condurre un saggio di complementazione, consentendo lo studio della funzione chaperone nella cellulo di Hsp70.
Introduction
Le proteine da shock termico svolgono un ruolo importante come chaperoni molecolari facilitando il ripiegamento delle proteine, prevenendo l'aggregazione proteica e invertendo il misfolding proteico 1,2. La proteina da shock termico 70 (Hsp70) è uno dei più importanti chaperoni molecolari, che svolge un ruolo centrale nell'omeostasi proteica 3,4. DnaK è l'omologo5 di E. coli Hsp70.
Sono stati sviluppati vari saggi biofisici, biochimici e cellulari per esplorare l'attività chaperone di Hsp70 e per lo screening degli inibitori che hanno come bersaglio questo chaperone 6,7,8. Hsp70 è una proteina altamente conservata. Per questo motivo, diversi Hsp70 di organismi eucarioti, come il Plasmodium falciparum (il principale agente della malaria), sono stati segnalati per sostituire la funzione del DnaK in E. coli 6,9. In questo modo, è stato sviluppato un saggio di complementazione basato su E. coli che coinvolge l'espressione eterologa di Hsp70s in E. coli per esplorare la loro funzione citoprotettiva. Tipicamente, questo test prevede l'utilizzo di cellule di E. coli che sono carenti di DnaK o che esprimono un DnaK nativo che è funzionalmente compromesso. Sebbene il DnaK non sia essenziale per la crescita di E. coli in condizioni normali, diventa essenziale quando le cellule vengono coltivate in condizioni di stress come temperature elevate o altre forme di stress10,11.
I ceppi di E. coli che sono stati sviluppati per studiare la funzione di Hsp70 utilizzando un saggio di complementazione includono E. coli dnaK103 (BB2393 [C600 dnaK103(Am) thr::Tn10]) ed E. coli dnaK756. Le cellule dnaK103 di E. coli producono un DnaK troncato che non è funzionale e, come tale, le cellule crescono adeguatamente a 30 °C, mentre il ceppo è sensibile allo stress da freddo e da caldo12,13. Analogamente, il ceppo di E. coli dnaK756/BB2362 (dnaK756 recA::TcR Pdm1,1) non cresce oltre i 40 °C14,15. Il ceppo dnaK756 di E. coli esprime un mutante nativo di DnaK (DnaK756) caratterizzato da tre sostituzioni glicina-aspartato nelle posizioni 32, 455 e 468, dando luogo a esiti proteostatici compromessi. Di conseguenza, questo ceppo è resistente al batteriofago λ DNA14. Inoltre, E. coli dnaK756 mostra un'elevata attività dell'ATPasi, mentre la sua affinità per il fattore di scambio nucleotidico, GrpE, è ridotta16. Coli I ceppi mutanti di DnaK fungono da modelli ideali per studiare l'attività chaperone di Hsp70 attraverso un approccio di complementazione. Poiché il DnaK è essenziale solo in condizioni di stress, il test di complementazione viene generalmente condotto a temperature elevate (Figura 1). Alcuni vantaggi dell'utilizzo di E. coli per questo studio includono il suo genoma ben caratterizzato, la rapida crescita e il basso costo di coltura e manutenzione17.
In questo articolo, descriviamo in dettaglio un protocollo che prevede l'uso di cellule dnaK756 di E. coli per studiare la funzione di Hsp70. Gli Hsp70 che abbiamo impiegato nel saggio sono DnaK wild-type e il suo derivato chimerico, KPf (costituito dal dominio ATPasi di DnaK fuso al dominio di legame del substrato C-terminale di Plasmodium falciparum Hsp70-1 6,18). KPf-V436F è stato eterologamente espresso come controllo negativo poiché la mutazione gli impedisce essenzialmente di legare i substrati, abrogando così la sua attività chaperone9.
Protocol
1. Trasformazione
NOTA: Utilizzare vetreria sterile per coltura, puntali per pipette e terreni appena preparati e sterilizzati in autoclave. Preparare colture di cellule di E. coli in 2x triptone di lievito (YT) [1,6% triptone (p/v), 1% estratto di lievito (p/v), 0,5% NaCl (p/v), 1,5% agar (p/v)] agar. I reagenti generali utilizzati nel protocollo e le loro fonti sono forniti nella Tabella dei materiali.
- Etichettare le provette per microcentrifuga da 2,0 mL e aliquotare 50 μL di cellule dnaK756 di E. colicompetenti, mantenendo le cellule in ghiaccio.
- Alle provette per microcentrifuga da 2,0 mL con cellule competenti, aliquotare 10-50 ng di pQE60/DnaK, pQE60/KPf e pQE60/KPf-V436F DNAplasmidico 9 in provette separate.
- Tenere le provette per microcentrifuga da 2,0 mL contenenti le cellule competenti e il DNA plasmidico su ghiaccio per 30 minuti.
- Eseguire uno shock termico della miscela cellule-DNA competente per 60 secondi a 42 °C e riportare le provette della microcentrifuga sul ghiaccio per 10 minuti.
- Aggiungere 950 μL di brodo fresco 2x YT (pre-incubato a 37 °C) e incubare a 37 °C agitando a 150 giri/min per 1 h. Lascia crescere le cellule molto più a lungo per favorire il loro recupero, se necessario.
NOTA: Evitare di agitare vigorosamente le cellule. - Pipettare 100 μL di cellule e distribuirle su 2 piastre di agar YT contenenti 50 μg/mL di kanamicina, 10 μg/mL di tetraciclina per il rispettivo ceppo e 100 μg/mL di ampicillina (vedere Tabella dei materiali) per la selezione dei plasmidi.
- Centrifugare il resto delle cellule (il cui volume è ora di circa 900 μL) per 1 minuto a 5000 x g (a 4 °C) utilizzando una microcentrifuga da banco.
- Decantare circa 800 μL di brodo e utilizzare il terreno rimanente per risospendere le cellule pellettate.
- Placcare le cellule recuperate sulla piastra di agar YT 2x.
- Incubare entrambe le piastre di agar per una notte (o circa 17 ore) a 37 °C.
NOTA: Queste cellule crescono molto lentamente e potrebbero aver bisogno di essere incubate molto più a lungo. Fate attenzione ad avvistare le colonie che possono iniziare molto piccole. La piastra contenente le cellule risospese dopo la centrifugazione (fase 1.7) funge da back-up nel caso in cui l'efficienza di trasformazione delle cellule sia scarsa, nel qual caso le cellule pellettate possono migliorare il recupero di eventuali cellule trasformate. Tuttavia, se l'efficienza di trasformazione è eccellente, la piastra di agar su cui sono state piastrate le cellule concentrate può essere caratterizzata da una coltura troppo cresciuta durante l'incubazione, rendendo difficile l'identificazione delle singole colonie. In tal caso, l'altra piastra di agar può essere quella su cui crescono colonie ben distanziate.
2. Placcatura cellulare
- Prelevare una singola colonia dai trasformanti e inocularla in 10 mL di brodo YT 2x integrato con 50 μg/mL di kanamicina, 10 μg/mL di tetraciclina per la selezione delle cellule dnaK756 di E. coli e 100 μg/mL di ampicillina per la selezione del plasmide.
NOTA: Utilizzare matracci (≥50 ml) per garantire l'aerazione durante l'agitazione della coltura. Incubare l'inoculo per una notte (17 h) a 37 °C agitando a 150 giri/min. - Effettuare una lettura dell'assorbanza a OD600 la mattina seguente.
- Pulire la superficie del banco di lavoro utilizzando etanolo al 75% per tamponare la superficie in preparazione allo spotting cellulare.
- Utilizzando una provetta per microcentrifuga da 2 mL, standardizzare la coltura a una lettura OD600 di 2,0 utilizzando 2 brodi YT.
NOTA: Assicurarsi che le letture OD siano effettuate correttamente poiché questo passaggio è importante per standardizzare la densità cellulare tra i vari campioni. - Utilizzando provette per microcentrifuga da 2 mL, preparare diluizioni seriali delle cellule da 100 a 10-5.
- Incubare le piastre di agar da utilizzare per individuare le cellule in un forno impostato a 40 °C per consentire alle piastre di asciugarsi con i coperchi parzialmente aperti per garantire la fuoriuscita del vapore acqueo.
NOTA: Per assicurarsi che le cellule siano individuate a distanze uniformemente separate, tracciare linee su un foglio di carta su cui è stampato un modello di siti di individuazione. - Individuare 2 μL delle cellule diluite in serie sulle piastre di agar integrate con 50 μg/mL di kanamicina, 10 μg/mL di tetraciclina, 100 μg/mL di ampicillina e 0,5 mM di IPTG (per l'induzione dell'espressione delle proteine ricombinanti) (vedi Tabella dei materiali).
- Posizionare ciascun campione su due piastre separate (una da incubare a 37 °C e l'altra a 43,5 °C).
NOTA: Evitare di forare la piastra di agar. - Posiziona i campioni di controllo sulla stessa piastra dei campioni sperimentali per ridurre al minimo gli effetti ambientali.
- Eseguire rapidamente lo spotting per assicurarsi che il processo sia completato prima che le cellule inizino a crescere, poiché ciò potrebbe generare modelli di crescita obliqui.
NOTA: È importante evitare gli aerosol durante l'avvistamento, poiché contaminerebbero le piastre. È anche importante tenere le piastre chiuse tra una macchia e l'altra per evitare contaminazioni. - Incubare una piastra a 37 °C (temperatura di crescita permissiva) e l'altra alla temperatura di crescita non permissiva di 43,5 °C.
NOTA: Incubare le piastre rivolte verso il basso per evitare che il vapore si accumuli sul coperchio, poiché l'acqua di condensa laverebbe le colonie maculate dalle loro posizioni. - Mettere tutte le piastre nelle incubatrici contemporaneamente ed evitare di aprire l'incubatrice fino al mattino seguente.
NOTA: Si sconsiglia di aprire più volte lo sportello dell'incubatrice durante l'incubazione delle piastre. Questo perché l'accesso dell'aria nell'incubatore può provocare fluttuazioni di temperatura che hanno un impatto negativo sulla crescita cellulare.
3. Confermare l'espressione di proteine ricombinanti
- Utilizzando un'ansa sterile, prelevare parte delle cellule rimanenti dalla stessa colonia di cellule dnaK756 di E. coli trasformate.
- Inoculare le cellule in brodo YT da 10 mL integrato con 50 μg/mL di kanamicina, 10 μg/mL di tetraciclina e 100 μg/mL di ampicillina. Incubare per una notte (17 h) a 37 °C agitando a 150 giri/min.
- Trasferire la coltura in 90 ml di brodo sterile 2x YT contenente gli antibiotici necessari come indicato al punto 3.2. Lasciare che le cellule crescano fino alla fase logaritmica intermedia (OD600 = 0,4-0,6).
- Prelevare 2 mL del campione di coltura prima dell'induzione (0 h di induzione).
- Aggiungere IPTG a una concentrazione finale di 1 mM per indurre la produzione di proteine e reincubare le cellule a 37 °C.
- Prelevare un secondo campione da 2 ml 6 ore dopo l'induzione.
- Raccogliere le cellule centrifugandole a 5000 x g per 10 min. Mantenere la temperatura della centrifuga a 4 °C.
- Scartare il surnatante.
- Risospendere il pellet nel tampone PBS (137 mM NaCl, 27 mM KCl, 4,3 mM Na2HPO4, 1,4 mM KH2PO4) e conservare a -20 °C.
4. SDS-PAGE e analisi western blot
- Preparare 2 gel SDS al 10% come descritto in precedenza19.
- Conservare uno dei gel SDS-PAGE per la successiva colorazione utilizzando il colorante di Coomassie per visualizzare le bande proteiche. Utilizzare il secondo gel SDS-PAGE per eseguire l'analisi western blot.
- Aliquotare 80 μL dei campioni risospesi e miscelarli con 20 μL di tampone di carico SDS Laemmli 4x.
- Far bollire la sospensione a 100 °C per 10 min. Quindi caricare 10 μL di ciascun campione sul gel SDS prefabbricato (vedere la tabella dei materiali).
- Eseguire l'elettroforesi a temperatura ambiente per 1 ora utilizzando una tensione di 120 V in una soluzione 1x di tampone di funzionamento SDS (25 mm Tris, 250 mm di glicina, 0,1% (p/v) SDS).
- Colorare il gel con colorante di Coomassie (vedi Tabella dei materiali) per 1 ora, quindi decolorare con tampone decolorante (50% (v/v) metanolo, 10% (v/v) acido acetico in acqua distillata) per 2 ore.
- Visualizzare le bande proteiche presenti nel gel utilizzando un sistema di imaging su gel (vedere la tabella dei materiali). Ripetere l'esecuzione di un altro gel SDS-PAGE con gli stessi campioni seguendo il protocollo sopra menzionato.
- Al termine del ciclo elettroforetico, prelevare gel SDS-PAGE per eseguire l'analisi western blot come descrittoin precedenza 19.
- Lavare tre volte la membrana di nitrocellulosa su cui sono state trasferite le proteine nel tampone di lavaggio (TBS-Tween, pH 7,4 [50 mM Tris, 150 mM NaCl, 1% (v/v) Tween]).
- Utilizzare α-DnaK (vedere la tabella dei materiali) per rilevare rispettivamente DnaK e α-PfHsp70-17 per rilevare KPf e il suo mutante, KPf-V436F.
- Utilizzare gli anticorpi a diluizione 1:2000 in latte scremato al 5%. Incubare a 4 °C agitando a 60 giri/min per 1 h.
- Rimuovere l'anticorpo non legato in modo specifico lavando la membrana di nitrocellulosa in TBS-Tween 3 volte in 15 minuti.
- Incubare la membrana nell'anticorpo secondario (α-coniglio, vedere Tabella dei materiali) nelle stesse condizioni della fase precedente. Segue un successivo lavaggio nelle stesse condizioni dell'anticorpo primario.
- Risolvere le bande utilizzando il reagente di rilevamento della chemiluminescenza avanzata (ECL).
- Visualizza le bande utilizzando un gel imager.
Results
La Figura 2 presenta un'immagine dell'agar scansionato contenente cellule che sono state individuate e coltivate alla temperatura di crescita permissiva di 37 °C e 43,5 °C, rispettivamente. Sul lato destro della Figura 2, i componenti western blot asportati rappresentano l'espressione di DnaK, KPf e KPf-V436F nelle cellule dnaK756 di E. coli. Come previsto, tutte le cellule di E. coli dnaK756 coltivate alla temperatura di crescita permissiva di 37 °C sono riuscite a crescere. Tuttavia, in condizioni di crescita non permissiva di 43,5 °C, solo le cellule che esprimono eterologamente DnaK e KPf sono riuscite a crescere, come precedentemente riportato 6,9,20 (Figura 2). D'altra parte, le cellule che esprimono KPf-V436F sono cresciute solo a 37 °C ma non sono riuscite a crescere a 43,5 °C. Ciò dimostra che DnaK e KPf sono stati in grado di ripristinare il difetto di crescita delle cellule dnaK756 di E. coli in condizioni di stress termico. L'incapacità delle cellule che esprimono eterologamente KPf-V436F di supportare la crescita delle cellule a 43,5 °C dimostra la mancanza della funzione chaperone di questa proteina. A questo proposito, KPf-V436F funge da proteina ideale per il controllo negativo.
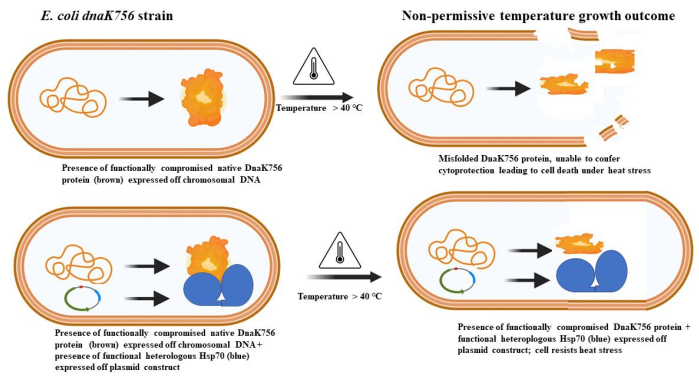
Figura 1: Principio del saggio di complementazione utilizzando cellule dnaK756 di E. coli per studiare la funzione chaperone di proteine espresse eterologamente. E. coli dnaK756 esprime una proteina nativa DnaK756 che non è in grado di proteggere le cellule dallo stress termico. L'introduzione di Hsp70 eterologa funzionale salva le cellule dalla morte in seguito all'esposizione a stress termico. Fare clic qui per visualizzare una versione più grande di questa figura.
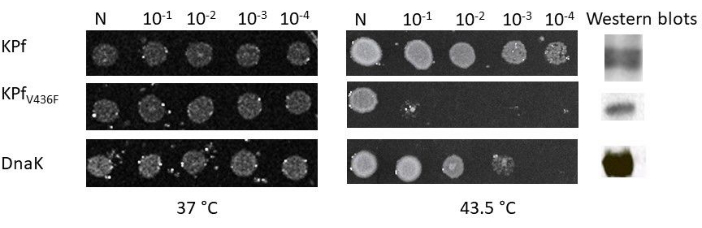
Figura 2: Saggio su piastra di complementazione che dimostra le capacità di DnaK e KPf di proteggere le cellule dnaK756 di E. coli dallo stress termico. Le cellule trasformate sono state coltivate a 37 °C (temperatura di crescita permissiva) e 43,5 °C (temperatura di crescita non permissiva). Le celle sono state standardizzate e placcate come diluizioni seriali. 'N' simboleggia 'Neat', che rappresenta il primo punto composto da cellule non diluite. All'estrema destra si trovano le escissioni western blot che rappresentano l'espressione delle tre proteine. Fare clic qui per visualizzare una versione più grande di questa figura.
Discussion
Il protocollo dimostra l'utilità delle cellule dnaK756 di E. colinell'esplorare la funzione chaperone di Hsp70 espressa eterologamente. Questo test potrebbe essere adottato per lo screening di inibitori che mirano alla funzione di Hsp70 nella cellulo. Tuttavia, una limitazione di questo metodo è che gli Hsp70 che non sono in grado di sostituire il DnaK in E. coli non sono compatibili con questo test. La mancanza di modificazione post-traduzionale21 di alcuni Hsp70 non nativi può spiegare la loro mancanza di funzione all'interno del sistema di E. coli . Un saggio di complementazione a base di lievito22 può risolvere alcune delle carenze del saggio a base di E. coli.
Diversi passaggi chiave sono fondamentali per garantire risultati riproducibili. Questi includono la garanzia che durante la placcatura vengano utilizzate solo le cellule trasformate dal rispettivo costrutto plasmidico. Inoltre, è importante evitare la contaminazione della coltura durante le fasi. Inoltre, poiché le cellule DnaK di E. coli stressate sono suscettibili a un'eccessiva filamentazione10, è importante evitare scuotimenti vigorosi durante la coltura, poiché questo sforzo fisico favorisce un'ampia filamentazione. Le cellule eccessivamente filamentate forniscono letture di crescita apparente false più elevate a OD600, portando a una sovrastima della crescita della coltura e influenzando negativamente la standardizzazione delle cellule prima della placcatura. Sebbene Hsp70 non sia essenziale per la crescita di E. coli in condizioni normali, le cellule prive di questa proteina sono suscettibili allo stress10. Per questo motivo, le cellule dnaK756 di E. coli crescono molto più lentamente dopo essere state trasformate o durante il loro recupero dalle scorte di glicerolo. Inoltre, sono estremamente sensibili alle fluttuazioni di temperatura. Pertanto, è importante evitare di aprire la porta dell'incubatrice una volta che le piastre di agar placcate sono state posizionate all'interno fino al momento di view le piastre.
I dati di western blot sono importanti per confermare l'espressione delle rispettive proteine ricombinanti Hsp70 nelle cellule dnaK756 di E. coli. La mancata espressione della rispettiva proteina porta a un risultato falso negativo per le cellule che crescono a una temperatura di crescita non permissiva.
Disclosures
Gli autori non hanno interessi finanziari concorrenti o altri conflitti di interesse.
Acknowledgements
Il lavoro è stato sostenuto con sovvenzioni ottenute dal Centro Internazionale per l'Ingegneria Genetica e la Biotecnologia (ICGEB) numero di sovvenzione, HDI/CRP/012, Direzione della Ricerca dell'Università di Venda, sovvenzione I595, Dipartimento di Scienza e Innovazione (DSI) e dalla National Research Foundation (NRF) del Sud Africa (numeri di sovvenzione, 75464 e 92598) assegnati ad AS.
Materials
| Name | Company | Catalog Number | Comments |
|---|---|---|---|
| 2-β-Mercaptoetanolo | Sigma-Aldrich | 8,05,740 | Costituente per il caricamento del campione |
| colorante Acido acetico | Labchem | 101005125 | Costituente del decoloratore |
| Acrilammide | Sigma-Aldrich | 8008300100 | Componente di SDS |
| Agar | Merck | HG000BX1.500 | Costituente del saggio di crescita medio e liquido |
| Agarosio | Clever Scientific | 14131031 | Biologia molecolare certificata agarosio |
| Persolfato di ammonio | Sigma-Aldrich | 101875295 | Costituente per gel SDS-PAGE |
| Ampicillina | VWR International | 0339—EU— 25G | Antibiotico selettivo |
| Bis | Sigma-aldrich | 1015460100 | Componente di SDS |
| Bromophenol | Sigma-Aldrich | 0449-25G | Costituente per il colorante di caricamento dei campioni |
| CaCl2 | Sigma-Aldrich | 10043-52-4 | Per una preparazione competente delle cellule |
| Coomassie blu brillante | VWR International | 443293X | Colorante SDS-PAGE |
| Fosfato di sodio bibasico | Sigma-Aldrich | RB10368 | Costituente del tampone PBS |
| ECL | Thermofischer Scientific | 32109 | Reagente per la rilevazione di Western blot |
| Bromuro di etidio | Thermofischer Scientific | 17898 | Colorante intercalante del DNA |
| Glicerolo | Merck | SAAR2676520L | Costituente per il caricamento del campione |
| Colorante Glicina | VWR International | 10119CU | Componente di SDS |
| IPTG | Glentham scienze della vita | 162IL | induttore |
| Kanamicina | Melford | K0126 | Antibiotico selettivo |
| Cloruro di magnesio | Merck | SAAR4123000EM | Costituente del test di crescita medio e liquido |
| Metanolo | Labchem | 113140129 | Costituente del decoloratore |
| Fosfato di potassio monobasico | Merck | 1,04,87,30,250 | Costituente del tampone PBS |
| Peptone | Merck | HG000BX4.250 | Costituente del saggio di crescita medio e liquido |
| Cloruro di potassio | Merck | SAAR5042020EM | Costituente del tampone PBS |
| Membrana PVDF | Thermofischer scientific | PB7320 | Membrana Western blot |
| Cloruro di sodio | Merck | SAAR5822320EM | Costituente del saggio di crescita medio e liquido |
| Dodecil solfato di sodio | VWR International | 108073 | Per risolvere le proteine espresse |
| Spectramax iD3 | Separazioni | 373705019 | Lettore automatico di piastre |
| TEMED | VWR international | ACRO420580500 | Componente del gel SDS |
| Tetraciclina | Duchefa Biochemies | T0150.0025 | Antibiotico selettivo |
| Tris | VWR International | 19A094101 | Componente del gel SDS |
| Tween20 | Merck | SAAR3164500XF | Costituente per il tampone di lavaggio occidentale |
| Camera di trasferimento occidentale | Thermofisher Scientific | PB0112 | Trasferimento di proteine alla membrana di nitrocellulosa |
| Estratto di lievito | Merck | HG000BX6.500 | Costituente del saggio di crescita medio e liquido |
| &alfa;-DnaK anticorpo | Inqaba | BK CAC09317 | Anticorpo primario |
| &alfa;-coniglio | Thermofischer scientific | 31460 | Anticorpo secondario |
References
- Bukau, B., Deuerling, E., Pfund, C., Craig, E. A. Getting newly synthesized proteins into shape. Cell. 101 (2), 119-122 (2000).
- Shonhai, A. Plasmodial heat shock proteins: targets for chemotherapy. FEMS Microbiol. Immunol. 58 (1), 61-74 (2010).
- Mogk, A., et al. Identification of thermolabile Escherichia coli proteins: prevention and reversion of aggregation by DnaK and ClpB. EMBO J. 18 (24), 6934-6949 (1999).
- Edkins, A. L., Boshoff, A. General structural and functional features of molecular chaperones. Heat shock proteins of malaria. Adv Exp Med Biol. Shonhai, A., Picard, D., Blatch, G. L. , Springer. (2021).
- Bertelsen, E. B., Chang, L., Gestwicki, J. E., Zuiderweg, E. R. Solution conformation of wild-type E. coli. Hsp70 (DnaK) chaperone complexed with ADP and substrate. PNAS. 106 (21), 8471-8476 (2009).
- Shonhai, A., Boshoff, A., Blatch, G. L. Plasmodium falciparum heat shock protein 70 is able to suppress the thermosensitivity of an Escherichia coli DnaK mutant strain. Mol Genet Genomics. 274, 70-78 (2005).
- Shonhai, A., Botha, M., de Beer, T. A., Boshoff, A., Blatch, G. L. Structure-function study of a Plasmodium falciparum Hsp70 using three-dimensional modelling and in vitro analyses. Protein Pept Lett. 15 (10), 1117-1125 (2008).
- Cockburn, I. L., Boshoff, A., Pesce, E. -R., Blatch, G. L. Selective modulation of plasmodial Hsp70s by small molecules with antimalarial activity. Biol Chem. 395 (11), 1353-1362 (2014).
- Makhoba, X. H., et al. Use of a chimeric Hsp70 to enhance the quality of recombinant Plasmodium falciparum s-adenosylmethionine decarboxylase protein produced in Escherichia coli. PLoS One. 11 (3), 0152626(2016).
- Bukau, B., Walker, G. C. Cellular defects caused by deletion of the Escherichia coli dnaK gene indicate roles for heat shock protein in normal metabolism. J Bact. 171 (5), 2337-2346 (1989).
- Makumire, S., Revaprasadu, N., Shonhai, A. DnaK protein alleviates toxicity induced by citrate-coated gold nanoparticles in Escherichia coli. PLoS One. 10 (4), 0121243(2015).
- Spence, J., Cegielska, A., Georgopoulos, C. Role of Escherichia coli heat shock proteins DnaK and HtpG (C62. 5) in response to nutritional deprivation. J Bact. 172 (12), 7157-7166 (1990).
- Mayer, M. P., et al. Multistep mechanism of substrate binding determines chaperone activity of Hsp70. Nat Struct Biol. 7 (7), 586-593 (2000).
- Georgopoulos, C. A new bacterial gene (groP C) which affects λ DNA replication. Mol Genet Genomics. 151 (1), 35-39 (1977).
- Tilly, K., McKittrick, N., Zylicz, M., Georgopoulos, C. The dnaK protein modulates the heat-shock response of Escherichia coli. Cell. 34 (2), 641-646 (1983).
- Buchberger, A., Gassler, C. S., Buttner, M., McMacken, R., Bukau, B. Functional defects of the DnaK756 mutant chaperone of Escherichia coli indicate distinct roles for amino-and carboxyl-terminal residues in substrate and co-chaperone interaction and interdomain communication. J Biol Chem. 274 (53), 38017-38026 (1999).
- Taj, M. K., et al. Escherichia coli as a model organism. Int J Eng Res. 3 (2), 1-8 (2014).
- Sato, S., Wilson, R. I. Organelle-specific cochaperonins in apicomplexan parasites. Mol Biochem Parasitol. 141 (2), 133-143 (2005).
- Shonhai, A. Molecular characterisation of the chaperone properties of Plasmodium falciparum. heat shock protein 70. Rhodes University. , Available from: https://commons.ru.ac.za/vital/access/manager/Repository/vital:3977?site_name=Rhodes+University (2007).
- Makumire, S., et al. Mutation of GGMP repeat segments of Plasmodium falciparum Hsp70-1 compromises chaperone function and Hop co-chaperone binding. Int J Mol Sci. 22 (4), 2226(2021).
- Nitika, P. C. M., Truman, A. W., Truttmann, M. C. Post-translational modifications of Hsp70 family proteins: Expanding the chaperone code. J Biol Chem. 295 (31), 10689-10708 (2020).
- Knighton, L. E., Saa, L. P., Reitzel, A. M., Truman, A. W. Analyzing the functionality of non-native Hsp70 proteins in Saccharomyces cerevisiae. Bio Protoc. 9 (19), e3389(2019).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request Permission