Modellering Snabbsök cyklisk voltammetrydata från elektriskt stimulerade data om dopaminöverföring via QNsim1.0
Summary
Snabbscanning cyklisk voltammetri kan övervaka dopamin-neurotransmission in vivo i samband med droger, sjukdomar och andra experimentella manipuleringar. Detta arbete beskriver implementeringen av QNsim1.0, en mjukvara för att modellera elektriskt stimulerade dopaminreaktioner enligt den kvantitativa neurobiologiska modellen för att kvantifiera uppskattningar av dopaminfrisättning och återupptagningsdynamik.
Abstract
Centrala dopaminerga (DAergic) vägar har en viktig roll i ett brett spektrum av funktioner, såsom uppmärksamhet, motivation och rörelse. Dopamin (DA) är inblandad i sjukdomar och störningar, däribland uppmärksamhetsbrist hyperaktivitetsstörning, Parkinsons sjukdom och traumatisk hjärnskada. Sålunda är DA neurotransmission och metoderna för att studera den av intensivt vetenskapligt intresse. In vivo snabbscanning cyklisk voltammetri (FSCV) är en metod som möjliggör selektiv övervakning av DA-koncentrationsförändringar med fin temporal och rumslig upplösning. Denna teknik används vanligen i samband med elektriska stimuleringar av stigande DAerg-vägar för att styra impulsflödet av dopamin-neurotransmission. Även om det stimulerade DA-neurotransmissionsparadigmet kan producera robusta DA-svar med tydliga morfologier, vilket gör dem mottagliga för kinetisk analys, är det fortfarande mycket debatt om hur man tolkar svaren i fråga om deras DA-frisättning och clearanCe komponenter. För att ta itu med detta problem utvecklades en kvantitativ neurobiologisk (QN) ram för stimulerad DA-neurotransmission för att realistiskt modellera dynamiken för DA-frisättning och återupptagning under ett stimulerat DA-svar. Grunden för denna modell är baserad på experimentella data från stimulerad DA-neurotransmission och på principer för neurotransmission antagen från olika forskningslinjer. QN-modellen implementerar 12 parametrar relaterade till stimulerad DA-frisättning och återupptagningsdynamik för modell DA-svar. I det här arbetet beskrivs hur man simulerar DA-svar med QNsim1.0 och även detaljer om principer som har implementerats för att systematiskt urskilja förändringar i den stimulerade dopaminfrisättningen och återupptagningsdynamiken.
Introduction
Dopamin (DA) neurotransmission spelar en viktig roll i olika kognitiva och beteendemässiga funktioner, och dess dysfunktion är inblandad i flera vanliga sjukdomar och störningar. Som sådan är det kritiskt att utveckla exakta metoder för att kvantitativt studera DA-neurotransmission in vivo för att utvärdera hur DA-neurotransmission förändras i samband med sjukdomsmodeller och läkemedelsfarmakologi. Snabb-skanning cyklisk voltammetri (FSCV) möjliggör övervakning in vivo DA-neurotransmission med fin spatial och tidsmässig upplösning. Medan det är möjligt att övervaka fysiologisk DA-neurotransmission i vakna, fritt uppfostrade djur kan den elektriska stimuleringen av stigande dopaminerga vägar i bedövade djur producera robusta DA-svar som är mottagliga för den förbättrade kinetiska analysen av DA-neurotransmission.
Elektriskt stimulerade DA-svar speglar ett dynamiskt samspel av DA-frisläppande och återupptagning och tolkningarAv dessa svar har främst använt en enkel modell av stimulerad DA-neurotransmission, kallad Michaelis-Menten (MM) -modellen 12 . MM-modellen består av 3 variabler för att beskriva DA-responser i form av en konstant DA-frisättningshastighet och en konstant återupptagningseffektivitet ( dvs. förhållandet mellan DA-upptagningshastigheten och extracellulära DA-koncentrationer), såsom beskrivs av ekvation 1 : 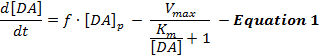
(DA release) (DA återupptagning)
I ekvation 1 är f frekvensen för stimulering; [DA] p är den uppskattade DA-koncentrationens ökning per stimuleringsimpuls; V max representerar den uppskattade maximal återupptagningshastigheten; Och Km är den uppskattade MM-konstanten, som är teoretiskt ekvivalent med den extracellulära DA-koncentrationen som mättar 50% av DAT, vilket leder till en halv maximal återupptagningshastighet. Denna differentiAl ekvation kan integreras för att simulera experimentella DA-svar genom att uppskatta [DA] p , V max och K m parametrar.
Även om MM-modellen har underlättat betydande framsteg i förståelsen av DA-neurotransmissionskinetik i olika experimentella sammanhang, gör MM-modellen enkla grundläggande antaganden som begränsar dess tillämplighet vid modellering DA-svar som framkallas av suprafysiologiska stimulanser 2 , 13 . Exempelvis kan MM-modellen bara approximera DA-responsformer om de stiger på ett konvex sätt, men det kan inte ta hänsyn till de gradvisa (konkava) stigande svaren som finns i dorsala striatala regioner 12 . Således tar MM-modellen antaganden inte exakt upp de dynamiska frisättnings- och återupptagsprocesserna för stimulerad DA-neurotransmission.
Att modellera stimulerade DA-svar enligt en realistisk kvantItative ramverk, den kvantitativa neurobiologiska (QN) ramen utvecklades baserat på principer för stimulerad neurotransmissionskinetik härrörande från komplementär forskning och experiment 2 . Olika linjer av neurotransmissionsforskning visar att (1) stimulerad frigörande av neurotransmitter är en dynamisk process som minskar i takt under stimulans 14 , (2) frisättning fortsätter i post-stimuleringsfasen med bifasisk sönderfallskinetik 15 och (3) DA Reuptake-effektiviteten hämmas progressivt under själva stimulansperioden 2 , 16 . Dessa tre begrepp fungerar som grunden för QN-ramen, och de tre ekvationerna består av 12 parametrar som beskriver dynamiken för DA-frisättning och återupptagning ( Tabell 1 ). QN-ramen kan noggrant simulera heterogena experimentella DA-svarstyper, såväl som pReducerade effekter av experimentella manipuleringar av stimuleringsparametrar och läkemedelsadministration 2 , 6 . Även om ytterligare forskning är nödvändig för att fördjupa datamodelleringsmetoden, kan framtida experiment i stor utsträckning dra nytta av detta neurobiologiskt grundade modellerings-tillvägagångssätt, vilket väsentligt bidrar till de härledda resultaten från det stimulerade DA-neurotransmissionsparadigmet.

Tabell 1: Modelleringsekvationer och parametrar . Vänligen klicka här för att se en större version av denna figur.
Denna handledning beskriver hur man modellerar stimulerad DA-responsdata för att uppskatta DA-frisättning och återupptagskinetik med QNsim 1.0. Den faktiska experimentella datainsamlingen och prUppgift är inte beskrivet här och kräver endast tidsmässig DA-koncentrationsdata. Det teoretiska stödet och grunden för QN-ramen har beskrivits utförligt tidigare 2 , men ett praktiskt perspektiv på att tillämpa QN-ramverket för modell DA-svardata beskrivs nedan.
QN-ramen modellerar det dynamiska samspelet mellan: 1) dynamisk DA-frisättning, 2) DA-återupptagning, och 3) effekterna av suprafysiologiska stimulanser på dessa processer för att extrahera meningsfull kinetisk information från DA-svardata. QN-ramverket passar bäst för modellering av FSCV-data som erhållits med högt suprafysiologiska stimulanser med lång varaktighet ( t.ex. 60 Hz, 10 s stimulanser), vilket ger robusta DA-svar som är mottagliga för kinetisk analys. Efter noggrann modellering av de underliggande frisättnings- och återupptagsprocesserna kan modellparametrarna användas för att simulera ett DA-svar som skulle approximera formen på exPerimental DA svar.
Ekvationerna i QN-ramen beskriver hastigheterna för DA-frisättning och återupptagning under de stimulerade DA-svarenas lopp. QN-ramen beskriver den stimulerade DA-frisättningsgraden som en funktion av tiden från stimulansstart (t-st), när DA-frisättningsgraden exponentiellt minskar under stimulansförloppet. Detta överensstämmer med uttömningen av en lätt frigörbar pool, med en tillsatt stabiliserad DA-frisättningshastighet (DARss) för redovisning av vesikelpåfyllning, som liknar andra rapporter ( ekvation 2 ) 14 , 17 .
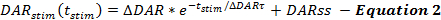
Manipuleringar som ökar DA-frisättningsfrekvensen, såsom ökande ΔDAR, ΔDAR τ eller DARss, leder till ökade responsförstärkningar på DA-versus tidstimer. Varje parameTer bidrar olika till DA-responsformer. Ökande DARss och ΔDAR τ gör båda stigande faser av svar mer linjära (mindre konvexa). Att minska Δ DAR τ främjar konvexitet, som styrs av storleken av Δ DAR. Baserat på modelleringserfarenhet är DARss generellt mindre än 1/5 av Δ DAR; Sålunda är Δ DAR frisättningsparametern som primärt bestämmer den totala responsamplituden för ett DA-svar.
DA-frisättningshastigheten efter stimulering modelleras av ekvation 3 som en fortsättning på den stimulerade DA-frisättningshastigheten från slutet av stimulering (DAR ES ) som en funktion av tiden efter stimulering (t- post ). Post-stimulering DA-frisättningshastigheten följer ett bifasiskt sönderfallsmönster, som tidigare beskrivits 15 , med en snabb exponentiell sönderfallsfas och en förlängd linjär sönderfallsfas till modell två caLciumberoende neurotransmittor-frisättningsförfaranden.
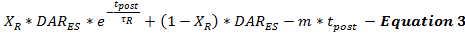
(Snabb exponentiell sönderfall) (långvarigt linjärt förfall)
Det är för närvarande inte möjligt att bestämma hur mycket poststimulering DA-frisättning uppstår. Denna begränsning kan åtgärdas genom att systematiskt minimera uppskattningar av poststimulering DA-frisättning och validering av modellparametrar över en uppsättning experimentella DA-svar som samlas in från samma inspelningsplats med användning av varierande stimuleringstider. Denna minimering tillåter användare att göra konservativa uppskattningar av frisättning och återupptagning. Eftersom elektriska stimuleringar leder till kalciumackumulering som främjar frisättning av neurostransmitter efter stimulering påverkar stimuleringstiden poststimulationsneurotransMitterfrigöringsparametrar 18 , 19 . Baserat på modelleringserfarenhet visade sig att när stimulansvaraktigheten ökar ökar τ R och X R minskar, vilket överensstämmer med de förväntade effekterna av en större kalciumackumulering 20 .
Ekvation 4 beskriver DA-återupptagningsgraden som en förlängning av MM-ramen och införlivar en dynamisk Km-term som ökar under stimulering för att modellera en gradvis minskande återupptagningseffektivitet orsakad av de suprafysiologiska stimulanserna 2 , 16 . Km efter stimulering hålls konstant vid Km-värdet vid slutet av stimuleringen (K mES ).
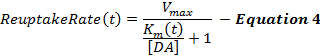
var,
<img alT = "ekvation 6" src = "/ files / ftp_upload / 55595 / 55595eq6.jpg" />
(Under stimulering) (Efter stimulering)
Stimulerade DA-svar, särskilt från ventralstriatala regioner, är ofta okänsliga för förändringar i det ursprungliga Km-värdet (K mi ), vilket gör att ett K mi- värde problematiskt definieras. Således är, som den ursprungliga MM-ramen, K mi approximerad vid 0,1-0,4 μM för DA-svar uppsamlade från kontrollbehandlade djur 12 . Termen Δ K m bestämmer omfattningen av upptagningseffektivitetsförändringen under stimulering, vilket från vår erfarenhet är cirka 2081; M under loppet av en 60 Hz, 10 s stimulering. K- och K- minf- värdena bestämmer hur Km ändras över tiden, och ökning av någon av dessa termer främjar uppgången i stigningsfasen. V max är den maximala återupptagningsgraden som delvis hänför sig till lokal DA-transportörens densitet, vilken uppvisar en ventromedial till dorsolateral gradient 21 . Följaktligen är Vmax- värden i dorsalstriatumet (D-Str) i allmänhet större än 30 ^ M / s men i allmänhet mindre än 30 ^ M / s i de ventrala regionerna, som kärnan accumbens (NAc) 6 .
De allmänna riktlinjerna ovan kan hjälpa till med modellering av experimentella DA-svardata, men generering av en simulering som approximerar det experimentella DA-svaret kräver iterativt att justera modellparametrar. Noggrannheten hos modellparametrarna kan förbättras genom att erhålla DA-svar på suprafysiologiska stimuleringar som tillhandahållerEa robust substrat för simulering, samt genom att erhålla och modellera flera DA-svar på stimuleringar av varierande varaktighet på samma inspelningsplats ( t.ex. stimulering av 60 Hz, 5 s och 10 s) för att validera parameterns noggrannhet ( Se provdata). För att visa att en dataset ingår i mjukvarupaketet som innehåller regiospecifika stimulerade DA-svar som samlats in i kärnans accumbens och dorsalstriatum före och efter en farmakologisk utmaning som redan modellerades med hjälp av QN-ramverket. Utvidgningen kommer användarna att finna att denna metodik kan användas för att karakterisera kinetiken för DA-neurotransmission i olika sjukdomskontext och farmakologiska manipuleringar.
Protocol
Representative Results
Discussion
Användningen av FSCV för att studera in vivo- stimulerad DA-neurotransmission härstammar från 1980-talet 30 och fortsätter fortfarande att vara en rik källa till in vivo- neurotransmissionsdata med oöverträffad rumslig och tidsmässig upplösning. Stimulerade DA-svar speglar en komplex balans av DA-frisättning och återupptagning som moduleras av de elektriska stimulansema själva. QN-modellen innehåller principer från modern neurotransmissionsforskning för att model…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi erkänner UPMC Rehabilitation Institute för att stödja detta arbete.
Materials
| MATLAB R2016a for Mac | Mathworks | ||
| QNsim1.0 | In house software package | Software to model FSCV data using the QN framework |
References
- Taylor, I. M., et al. Kinetic diversity of dopamine transmission in the dorsal striatum. J Neurochem. 133 (4), 522-531 (2015).
- Harun, R., Grassi, C. M., Munoz, M. J., Torres, G. E., Wagner, A. K. Neurobiological model of stimulated dopamine neurotransmission to interpret fast-scan cyclic voltammetry data. Brain Res. 1599, 67-84 (2015).
- Taylor, I. M., Jaquins-Gerstl, A., Sesack, S. R., Michael, A. C. Domain-dependent effects of DAT inhibition in the rat dorsal striatum. Journal of neurochemistry. 122 (2), 283-294 (2012).
- Garris, P. A., Ciolkowski, E. L., Wightman, R. M. Heterogeneity of evoked dopamine overflow within the striatal and striatoamygdaloid regions. Neuroscience. 59 (2), 417-427 (1994).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain Res. 487 (2), 311-320 (1989).
- Harun, R., et al. Fast-scan cyclic voltammetry demonstrates that L-DOPA produces dose-dependent regionally selective, bimodal effects on striatal dopamine kinetics in vivo. J Neurochem. , (2015).
- Jones, S. R., Garris, P. A., Wightman, R. M. Different effects of cocaine and nomifensine on dopamine uptake in the caudate-putamen and nucleus accumbens. The Journal of pharmacology and experimental therapeutics. 274 (1), 396-403 (1995).
- Budygin, E. A., John, C. E., Mateo, Y., Jones, S. R. Lack of cocaine effect on dopamine clearance in the core and shell of the nucleus accumbens of dopamine transporter knock-out mice. J Neurosci. 22 (10), RC222 (2002).
- Jones, S. R., et al. Loss of autoreceptor functions in mice lacking the dopamine transporter. Nat Neurosci. 2 (7), 649-655 (1999).
- Wagner, A. K., et al. Chronic methylphenidate treatment enhances striatal dopamine neurotransmission after experimental traumatic brain injury. J Neurochem. 108 (4), 986-997 (2009).
- Wagner, A. K., et al. Controlled cortical impact injury influences methylphenidate-induced changes in striatal dopamine neurotransmission. J Neurochem. 110 (3), 801-810 (2009).
- Wightman, R. M., et al. Real-time characterization of dopamine overflow and uptake in the rat striatum. Neuroscience. 25 (2), 513-523 (1988).
- Moquin, K. F., Michael, A. C. Tonic autoinhibition contributes to the heterogeneity of evoked dopamine release in the rat striatum. J Neurochem. 110 (5), 1491-1501 (2009).
- Pyott, S. J., Rosenmund, C. The effects of temperature on vesicular supply and release in autaptic cultures of rat and mouse hippocampal neurons. J Physiol. 539 (Pt 2), 523-535 (2002).
- Atluri, P. P., Regehr, W. G. Delayed release of neurotransmitter from cerebellar granule cells. J Neurosci. 18 (20), 8214-8227 (1998).
- Wang, S. R., et al. Role of vesicle pools in action potential pattern-dependent dopamine overflow in rat striatum in vivo. J Neurochem. 119 (2), 342-353 (2011).
- Taschenberger, H., von Gersdorff, H. Fine-tuning an auditory synapse for speed and fidelity: developmental changes in presynaptic waveform, EPSC kinetics, and synaptic plasticity. J Neurosci. 20 (24), 9162-9173 (2000).
- Goda, Y., Stevens, C. F. Two components of transmitter release at a central synapse. Proc Nat Acad of Sci U S A. 91 (26), 12942-12946 (1994).
- Yao, J., Gaffaney, J. D., Kwon, S. E., Chapman, E. R. Doc2 is a Ca2+ sensor required for asynchronous neurotransmitter release. Cell. 147 (3), 666-677 (2011).
- Hagler, D. J., Goda, Y. Properties of synchronous and asynchronous release during pulse train depression in cultured hippocampal neurons. J Neurophysiol. 85 (6), 2324-2334 (2001).
- Ciliax, B. J., et al. The dopamine transporter: immunochemical characterization and localization in brain. J Neurosci. 15 (3 Pt 1), 1714-1723 (1995).
- Volz, T. J., Farnsworth, S. J., Rowley, S. D., Hanson, G. R., Fleckenstein, A. E. Methylphenidate-induced increases in vesicular dopamine sequestration and dopamine release in the striatum: the role of muscarinic and dopamine D2 receptors. J Pharm Exp Ther. 327 (1), 161-167 (2008).
- Dresel, S. H., Kung, M. P., Plossl, K., Meegalla, S. K., Kung, H. F. Pharmacological effects of dopaminergic drugs on in vivo binding of [99mTc]TRODAT-1 to the central dopamine transporters in rats. Eur J Nucl Med. 25 (1), 31-39 (1998).
- Near, J. A., Bigelow, J. C., Wightman, R. M. Comparison of uptake of dopamine in rat striatal chopped tissue and synaptosomes. J Pharm Exp Ther. 245 (3), 921-927 (1988).
- Michael, A. C., Ikeda, M., Justice, J. B. Dynamics of the recovery of releasable dopamine following electrical stimulation of the medial forebrain bundle. Neurosci Lett. 76 (1), 81-86 (1987).
- Fierro, L., DiPolo, R., Llano, I. Intracellular calcium clearance in Purkinje cell somata from rat cerebellar slices. The Journal of physiology. 510 (Pt 2), 499-512 (1998).
- Sandoval, V., Riddle, E. L., Hanson, G. R., Fleckenstein, A. E. Methylphenidate redistributes vesicular monoamine transporter-2: role of dopamine receptors. J Neurosci. 22 (19), 8705-8710 (2002).
- Daws, L. C., et al. Cocaine increases dopamine uptake and cell surface expression of dopamine transporters. Biochem Biophys Res Commun. 290 (5), 1545-1550 (2002).
- Little, K. Y., Kirkman, J. A., Carroll, F. I., Clark, T. B., Duncan, G. E. Cocaine use increases [3H]WIN 35428 binding sites in human striatum. Brain Res. 628 (1-2), 17-25 (1993).
- Ewing, A. G., Bigelow, J. C., Wightman, R. M. Direct in vivo monitoring of dopamine released from two striatal compartments in the rat. Science. 221 (4606), 169-171 (1983).
- Janezic, S., et al. Deficits in dopaminergic transmission precede neuron loss and dysfunction in a new Parkinson model. Proc Natl Acad Sci U S A. 110 (42), E4016-E4025 (2013).
- Macdonald, P. A., Monchi, O. Differential effects of dopaminergic therapies on dorsal and ventral striatum in Parkinson’s disease: implications for cognitive function. Parkinsons Dis. 2011, 572743 (2011).
- Kile, B. M., et al. Optimizing the Temporal Resolution of Fast-Scan Cyclic Voltammetry. ACS Chem Neurosci. 3 (4), 285-292 (2012).
- Venton, B. J., Troyer, K. P., Wightman, R. M. Response times of carbon fiber microelectrodes to dynamic changes in catecholamine concentration. Anal Chem. 74 (3), 539-546 (2002).
- May, L. J., Wightman, R. M. Heterogeneity of stimulated dopamine overflow within rat striatum as observed with in vivo voltammetry. Brain research. 487 (2), 311-320 (1989).
- Wu, Q., Reith, M. E., Wightman, R. M., Kawagoe, K. T., Garris, P. A. Determination of release and uptake parameters from electrically evoked dopamine dynamics measured by real-time voltammetry. J Neurosci Methods. 112 (2), 119-133 (2001).

