Protocolo fácil para la síntesis de uno mismo-montaje base poliamina péptido Anfífilos (PPAs) y relacionados con biomateriales
Summary
La síntesis del péptido base poliamina Anfífilos (PPA) es un reto importante debido a la presencia de múltiples nitrógenos de Amina, que requiere un uso juicioso de la protección de los grupos para enmascarar estas funcionalidades reactivas. En este papel, describimos un método fácil para la preparación de estas nueva clase de moléculas de uno mismo-montaje.
Abstract
Base poliamina péptido Anfífilos (PPA) son una nueva clase de uno mismo-montaje anfifílicas biomateriales relacionadas con el péptido Anfífilos (PAs). Tradicionales PAs poseen aminoácidos cargados como grupos (lisina, arginina), que están conectados directamente a un segmento de lípidos o pueden contener una región vinculador de los aminoácidos neutros de solubilización. Ajuste de la secuencia del péptido de PAs puede producir diversas morfologías. Asimismo, los PPA poseen un segmento hidrofóbico y aminoácidos neutros, pero también contienen poliamina moléculas como el agua (hidrofílicos) grupos de solubilización. Como es el caso de PAs, PPA también pueden uno mismo-montar en diversas morfologías, incluyendo barras pequeñas, trenzados cintas de nano y fundidas hojas de nano, cuando está disuelto en agua. Sin embargo, la presencia de aminas primarias y secundarias en una molécula de poliamina solo plantea un desafío significativo al sintetizar los PPA. En este documento, se muestra un protocolo simple, basado en precedentes de la literatura, para lograr una síntesis fácil de PPA usando síntesis peptídica en fase sólida (SPPS). Este protocolo puede ampliarse a la síntesis de PAs y otros sistemas similares. También ilustran los pasos que son necesarios para el escote de la resina, la identificación y la purificación.
Introduction
Anfífilos peptide uno mismo-montaje (PAs) son una clase de biomateriales, normalmente conformada de los siguientes segmentos: jefe (a) hidrofílico, (b) vinculador región y cola (c) hidrofóbica. PAs la mayoría descritos en la literatura poseen una cabeza hidrofílica compuesta por aminoácidos cargados o polares residuos1,2,3,4. PAs han encontrado una amplia gama de aplicaciones en biomedicina, incluyendo el suministro de medicamentos, diagnóstico de la enfermedad, medicina regenerativa, etc.5. De acuerdo con su secuencia de aminoácidos, PAs puede formar una variedad amplia de nanoestructuras como micelas esféricas, nano-filamentos. Recientemente hemos reportado una clase de híbrido péptido base poliamina Anfífilos, denominado PPA6. Las morfologías, cinética de la uno mismo-montaje y degradación metabólica, de estos biomateriales, fueron encontrados para ser relacionado con su grupo de cabeza solubilización. Por otra parte, las nanoestructuras de PPA no mostraron toxicidad hacia células de mamífero (líneas MiaPaCa2 y HeLa de la célula) en las concentraciones probadas. Nanocarriers basados en PPA son vehículos de fármaco atractivo porque: poliaminas (1) absorción y metabolismo se ha demostrado para ser aumentada en las células cancerosas, nanoestructuras (2) catiónico pueden lograr endosomal escape7,8, que conduce a mayor circulación y residencia dentro de una célula y (3) deben tener un perfil metabólico distinto en comparación con PA; por ejemplo, será más estables a las proteasas que se encuentran en el cuerpo humano (aunque ellos tal vez sensibles a otras enzimas, como oxidasas amina)9,10. Además, los PPA se han encontrado diversas morfologías, propiedades fisicoquímicas, rigidez de nanopartículas y cinética de montaje dependiendo de la longitud y la carga de cada molécula de PPA6. Adjunto, describimos un protocolo detallado de síntesis, identificación y purificación de los PPA que puede aplicarse también a la preparación de PAs o moléculas de péptidos híbridos similares.
Porque poliaminas no están comúnmente disponibles en el mercado en sus formas protegidas y porque proteger las aminas primarias y secundarias de poliaminas es de suma importancia para conjugar con los aminoácidos y otras moléculas, hemos descrito el medidas sintéticas para lograr su protección. El objetivo general de este protocolo es proporcionar un método simple para conjugar poliaminas a aminoácidos. Poliaminas carecen de un grupo carboxílico; por lo tanto, no puede acoplarse a pista de amida o resinas de Wang. En cambio, resinas como el cloruro de 2-chlorotrityl se recomiendan el protocolo sintético. El desafío principal para la síntesis de la PPA es la presencia de grupos funcionales de aminas primarias y secundarias. Para nuestros propósitos, hemos protegido todas las aminas secundarias de la poliamina manteniendo el grupo amino primario de la poliamina libre permitir la reacción de acoplamiento. La reacción se realizó sobre un soporte sólido siguiendo los principios de síntesis de péptidos de fase sólida (SPPS) para facilitar el trabajo después de cada etapa de acoplamiento y desprotección. El protocolo siguiente es para la síntesis manual y automatizada de PPAs (aunque la verificación de algunos pasos será difícil en un sistema automatizado). La síntesis de estas moléculas puede también ser realizada en un sintetizador automático o con la ayuda de un reactor de microondas (automático o semiautomático). El esquema de la reacción ha sido resumido en la figura 1.
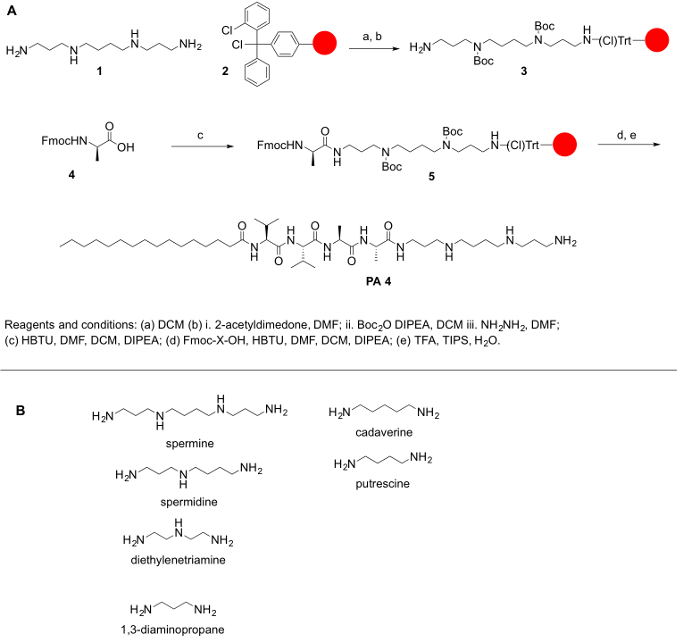
Figura 1: (A) A esquema general de la reacción para la síntesis de los PPA. Poliaminas representante (B) que pueden utilizarse para sintetizan PPAs se describe aquí. Haga clic aquí para ver una versión más grande de esta figura.
Protocol
Representative Results
Discussion
Los protocolos descritos aquí pueden utilizarse para sintetizar los PPA como pozos como PAs y relacionados con moléculas basadas en péptidos (como híbrido peptoides PA). Aunque la síntesis de péptidos mediante SPPS es un procedimiento sencillo, la síntesis de péptidos que contiene moléculas biológicas autoguiados hacia el blanco puede ser particularmente difícil. Poliaminas como espermina, espermidina, diethyelenetriamine, etc., pueden funcionar como moléculas autoguiados hacia el blanco para apuntar…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Este proyecto fue financiado por la Universidad de Nebraska Medical Center (fondos de arranque, MC-S); NIH-COBRE, 5P20GM103480 (T. Bronich) y la American Chemical Society, PRF # 57434-DNI7(MC-S).
Materials
| 2-Chlorotrityl chloride resin | AappTec | RTZ001 | |
| SynthwareTM synthesis vessel | Aldrich | SYNP120050M | |
| Dichloromethane | Acros | AC406920250 | Fisher Sci. Catalogue # |
| Wrist Shaker | Boekel Scientific | 401000-2 | |
| Kaiser test kit | Sigma-Aldrich | 60017 | |
| 2-[(4,4-dimethyl-2,6-dioxocyclohex-1-ylidene)ethyl-amino]-ethanol | Sigma-Aldrich | CDS004772 | |
| Anhydrous Methanol | Acros | AC610981000 | Fisher Sci. Catalogue # |
| Chloranil test kit | TCI | TCC1771-KIT | VWR Catalogue # |
| Di-tert butyl di-carbonate | Acros | AC194670250 | Fisher Sci. Catalogue # |
| Dimethylformamide | Fisher Scientific | BP1160-4 | |
| Hydrazine | Acros | AC296815000 | FIsher Sci. Catalogue # |
| (2-(1H-benzotriazol-1-yl)-1,1,3,3-tetramethyluronium hexafluorophosphate) | p3biosystems | 31001 | |
| 4-methyl piperidine | Acros | AC127515000 | FIsher Sci. Catalogue # |
| Trifluoroacetic Acid | AappTec | CXZ035 | |
| Triisopropyl Silane | Sigma-Aldrich | 233781 | |
| Ether | Fisher Scientific | E138-1 | |
| α-Cyano-4-hydroxycinnamic acid | Sigma-Aldrich | C8982 | |
| 9-Aminoacridine | Sigma-Aldrich | 92817 | |
| Fisherbrand Syringe Filters: PTFE Membrane | Fisher Scientific | 09-730-21 |
References
- Cui, H., Pashuck, E. T., Velichko, Y. S., Weigand, S. J., Cheetham, A. G., Newcomb, C. J., Stupp, S. I. Spontaneous and x-ray-triggered crystallization at long range in self-assembling filament networks. Science. 327, 555-559 (2010).
- Pashuck, E. T., Cui, H., Stupp, S. I. Tuning supramolecular rigidity of peptide fibers through molecular structure. Journal of the American Chemical Society. 132, 6041-6046 (2010).
- Stupp, S. I., Zha, R. H., Palmer, L. C., Cui, H., Bitton, R. Self-assembly of biomolecular soft matter. Faraday Discussions. 166, 9-30 (2013).
- Conda-Sheridan, M., Lee, S. S., Preslar, A. T., Stupp, S. I. Esterase-activated release of naproxen from supramolecular nanofibres. Chemical Communications. 50, 13757-13760 (2014).
- Mata, A., Palmer, L., Tejeda-Montes, E., Stupp, S. I. Design of biomolecules for nanoengineered biomaterials for regenerative medicine. Nanotechnology in Regenerative Medicine. , 39-49 (2012).
- Samad, M. B., Chhonker, Y. S., Contreras, J. I., McCarthy, A., McClanahan, M. M., Murry, D. J., Conda-Sheridan, M. Developing Polyamine-Based Peptide Amphiphiles with Tunable Morphology and Physicochemical Properties. Macromolecular bioscience. 17, (2017).
- Nel, A. E., Mädler, L., Velegol, D., Xia, T., Hoek, E. M., Somasundaran, P., Klaessig, F., Castranova, V., Thompson, M. Understanding biophysicochemical interactions at the nano-bio interface. Nature Materials. 8, 543 (2009).
- Gujrati, M., Malamas, A., Shin, T., Jin, E., Sun, Y., Lu, Z. -. R. Multifunctional cationic lipid-based nanoparticles facilitate endosomal escape and reduction-triggered cytosolic siRNA release. Molecular Pharmaceutics. 11, 2734-2744 (2014).
- Zhu, Y., Li, J., Kanvinde, S., Lin, Z., Hazeldine, S., Singh, R. K., Oupický, D. Self-immolative polycations as gene delivery vectors and prodrugs targeting polyamine metabolism in cancer. Molecular Pharmaceutics. 12, 332-341 (2014).
- Planas-Portell, J., Gallart, M., Tiburcio, A. F., Altabella, T. Copper-containing amine oxidases contribute to terminal polyamine oxidation in peroxisomes and apoplast of Arabidopsis thaliana. BMC Plant Biology. 13, 109 (2013).
- Nash, I. A., Bycroft, B. W., Chan, W. C. Dde – A selective primary amine protecting group: A facile solid phase synthetic approach to polyamine conjugates. Tetrahedron Letters. 37, 2625-2628 (1996).
- Ralhan, K., KrishnaKumar, V. G., Gupta, S. Piperazine and DBU: a safer alternative for rapid and efficient Fmoc deprotection in solid phase peptide synthesis. RSC Advances. 5, 104417-104425 (2015).
- Casero, R. A., Marton, L. J. Targeting polyamine metabolism and function in cancer and other hyperproliferative diseases. Nature Reviews Drug Discovery. 6, 373 (2007).
- Wuts, P. G. M., Greene, T. W. . Protection for the Amino Group. In Greene’s Protective Groups in Organic Synthesis. , 696-926 (2006).
- Palasek, S. A., Cox, Z. J., Collins, J. M. Limiting racemization and aspartimide formation in microwave-enhanced Fmoc solid phase peptide synthesis. Journal of Peptide Science. 13, 143-148 (2007).

