Facile protokoll för syntesen av självmonterande Polyamine-baserade peptid Amphiphiles (energiköpsavtalen) och relaterade biomaterial
Summary
Syntesen av polyaminen-baserade peptid amphiphiles (energiköpsavtalen) är en betydande utmaning på grund av närvaron av flera amine kväveatomer, som kräver förnuftig användning av skydda grupper för att maskera dessa reaktiva funktioner. I den här artikeln beskriver vi en lättköpt metod för beredning av dessa nya klass av egen montering molekyler.
Abstract
Polyamine-baserade peptid Amphiphiles (energiköpsavtalen) är en ny klass av egen montering amfifila biomaterial-relaterade till den peptid amphiphiles (PAs). Traditionella PAs äger laddade aminosyror som solubilizing grupper (lysin, arginin), som är direkt anslutna till ett lipid-segment eller kan innehålla en länkare region av neutrala aminosyror. Tuning peptid sekvensen av PAs kan ge olika morfologier. Likaså energiköpsavtalen besitter ett hydrofoba segment och neutrala aminosyror, men också innehålla polyamine molekyler som vatten solubilizing (hydrofil) grupper. Som är fallet med PAs, energiköpsavtalen kan även själv sätta ihop till olika morfologier, inklusive små stavar, vridna nano-band och smält nano-ark, när upplöst i vatten. Men utgör förekomsten av både primära och sekundära aminer på en enda polyamine molekyl en betydande utmaning när syntetisera energiköpsavtalen. I detta papper visar vi ett enkelt protokoll, baserade på litteratur prejudikat, att uppnå en lättköpt syntes av energiköpsavtalen använder fasta fasen peptidsyntesen (SPPS). Detta protokoll kan utvidgas till syntesen av PAs och andra liknande system. Vi illustrerar också de steg som behövs för klyvning från harts, identifiering och rening.
Introduction
Egen montering peptid amphiphiles (PAs) är en klass av biomaterial som vanligtvis består av följande segment: a hydrofil huvud, (b) linker region och (c) hydrofoba svans. De flesta PAs beskrivs i litteraturen äger en hydrofil huvud består av laddade eller polar aminosyra rester1,2,3,4. PAs har hittat ett brett spektrum av applikationer i biomedicin inklusive sjukdom diagnostik, regenerativ medicin, läkemedel, etc.5. Baserat på deras aminosyrasekvens, kan PAs bilda ett brett utbud av nanostrukturer inklusive sfäriska miceller och nano-filament. Vi har nyligen rapporterat en klass av hybrid polyamine-baserade peptid amphiphiles, kallas energiköpsavtalen6. Den morfologier, egen montering kinetik och metabola nedbrytning, av dessa biomaterial, befanns vara relaterade till deras solubilizing huvud grupp. PPA nanostrukturerna visade dessutom inte toxicitet mot däggdjursceller (MiaPaCa2 och HeLa cell linjer) vid de testa koncentrationerna. PPA-baserade nanocarriers är attraktiva drog-leverans fordon eftersom: (1) polyamine upptag och metabolism har visats ökas i cancerceller, (2) katjoniska nanostrukturer kan uppnå endosomal fly7,8, vilket leder till högre omsättning och bosättning inom en cell, och (3) de ska ha en tydlig metaboliska profil jämfört med PA; till exempel, de blir stabilare mot proteaser som finns i den mänskliga kroppen (även om de kanske känslig för andra enzymer, såsom amine oxidases)9,10. Inköpsavtalen har också befunnits har olika morfologier, fysikalisk-kemiska egenskaper, nanopartiklar stelhet och församlingen kinetik beroende på längd och kostnad av enskilda PPA molekyl6. Häri, beskriver vi ett detaljerat protokoll för syntes, identifiering och rening av energiköpsavtalen som kan också tillämpas på beredning av PAs eller liknande hybrid peptid molekyler.
Eftersom polyaminer vanligen inte är kommersiellt tillgängliga i sina skyddade formulär, och skydda de primära och sekundära aminesna av polyaminer är av yttersta vikt för konjugera dem med aminosyror och andra molekyler, har vi sammanställt den syntetiska steg för att uppnå deras skydd. Det övergripande målet med detta protokoll är att tillhandahålla en enkel metod för att konjugera polyaminer till aminosyror. Polyaminer saknar en karboxylsyror grupp; Således, de kan inte kopplas till rinken Amide eller Wang hartser. Istället rekommenderas protokollet syntetiska hartser såsom 2-chlorotrityl klorid. Den största utmaningen för PPA syntes är förekomsten av primära och sekundära aminen funktionella grupper. För våra syften skyddade vi alla de sekundära aminesna i polyaminen samtidigt den primära aminogruppen på polyaminen ledig för att tillåta koppling reaktionen. Reaktionen var gjort på ett massivt stöd för en fast fas peptidsyntesen (SPPS) att underlätta arbete-upp efter varje koppling och deprotection steg. Följande protokoll är för både manuell och automatiserad syntes av energiköpsavtalen (även om kontrollen av några steg kommer utmanande i ett automatiserat system). Syntesen av dessa molekyler kan också utföras på en automatiserad synthesizer eller med hjälp av en mikrovågsugn reaktor (automatiskt eller halvautomatiskt). Reaktionsformel har sammanfattas i figur 1.
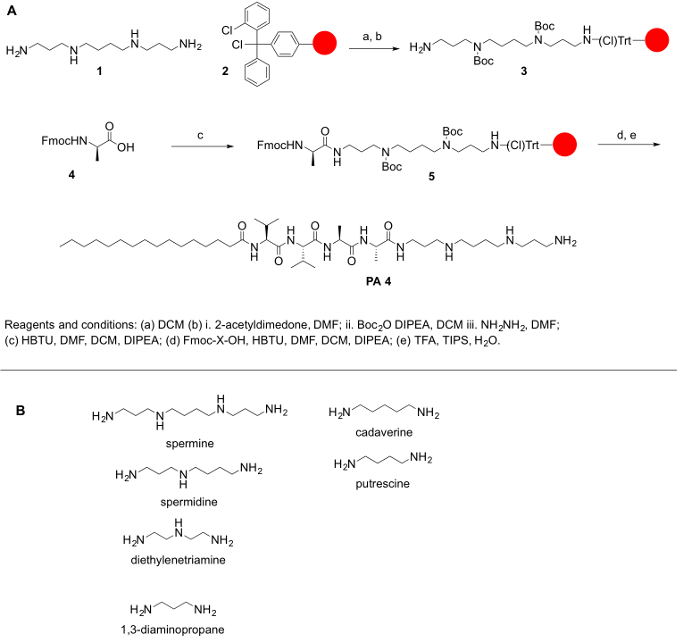
Figur 1: (A) A allmänna reaktionsformel för syntesen av energiköpsavtalen. (B) representativa polyaminer som kan användas till syntetiseras energiköpsavtalen beskrivs här. Klicka här för att se en större version av denna siffra.
Protocol
Representative Results
Discussion
De protokoll som beskrivs här kan användas för att syntetisera energiköpsavtalen brunnar som PAs och relaterad peptid-baserad molekyler (såsom hybrid PA-peptoids). Även om syntesen av peptider med SPPS är en enkel procedur, kan syntesen av peptider som innehåller biologiska målsökande molekyler vara särskilt utmanande. Polyaminer som spermine, spermidine, diethyelenetriamine, etc., kan fungera som målsökande molekyler för inriktning cancer celler13. Energiköpsavtalen kan sj…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Projektet finansierades av University of Nebraska Medical Center (nystartade fonder, MC-S); NIH-COBRE, 5P20GM103480 (T. Bronich) och American Chemical Society, PRF # 57434-DNI7(MC-S).
Materials
| 2-Chlorotrityl chloride resin | AappTec | RTZ001 | |
| SynthwareTM synthesis vessel | Aldrich | SYNP120050M | |
| Dichloromethane | Acros | AC406920250 | Fisher Sci. Catalogue # |
| Wrist Shaker | Boekel Scientific | 401000-2 | |
| Kaiser test kit | Sigma-Aldrich | 60017 | |
| 2-[(4,4-dimethyl-2,6-dioxocyclohex-1-ylidene)ethyl-amino]-ethanol | Sigma-Aldrich | CDS004772 | |
| Anhydrous Methanol | Acros | AC610981000 | Fisher Sci. Catalogue # |
| Chloranil test kit | TCI | TCC1771-KIT | VWR Catalogue # |
| Di-tert butyl di-carbonate | Acros | AC194670250 | Fisher Sci. Catalogue # |
| Dimethylformamide | Fisher Scientific | BP1160-4 | |
| Hydrazine | Acros | AC296815000 | FIsher Sci. Catalogue # |
| (2-(1H-benzotriazol-1-yl)-1,1,3,3-tetramethyluronium hexafluorophosphate) | p3biosystems | 31001 | |
| 4-methyl piperidine | Acros | AC127515000 | FIsher Sci. Catalogue # |
| Trifluoroacetic Acid | AappTec | CXZ035 | |
| Triisopropyl Silane | Sigma-Aldrich | 233781 | |
| Ether | Fisher Scientific | E138-1 | |
| α-Cyano-4-hydroxycinnamic acid | Sigma-Aldrich | C8982 | |
| 9-Aminoacridine | Sigma-Aldrich | 92817 | |
| Fisherbrand Syringe Filters: PTFE Membrane | Fisher Scientific | 09-730-21 |
References
- Cui, H., Pashuck, E. T., Velichko, Y. S., Weigand, S. J., Cheetham, A. G., Newcomb, C. J., Stupp, S. I. Spontaneous and x-ray-triggered crystallization at long range in self-assembling filament networks. Science. 327, 555-559 (2010).
- Pashuck, E. T., Cui, H., Stupp, S. I. Tuning supramolecular rigidity of peptide fibers through molecular structure. Journal of the American Chemical Society. 132, 6041-6046 (2010).
- Stupp, S. I., Zha, R. H., Palmer, L. C., Cui, H., Bitton, R. Self-assembly of biomolecular soft matter. Faraday Discussions. 166, 9-30 (2013).
- Conda-Sheridan, M., Lee, S. S., Preslar, A. T., Stupp, S. I. Esterase-activated release of naproxen from supramolecular nanofibres. Chemical Communications. 50, 13757-13760 (2014).
- Mata, A., Palmer, L., Tejeda-Montes, E., Stupp, S. I. Design of biomolecules for nanoengineered biomaterials for regenerative medicine. Nanotechnology in Regenerative Medicine. , 39-49 (2012).
- Samad, M. B., Chhonker, Y. S., Contreras, J. I., McCarthy, A., McClanahan, M. M., Murry, D. J., Conda-Sheridan, M. Developing Polyamine-Based Peptide Amphiphiles with Tunable Morphology and Physicochemical Properties. Macromolecular bioscience. 17, (2017).
- Nel, A. E., Mädler, L., Velegol, D., Xia, T., Hoek, E. M., Somasundaran, P., Klaessig, F., Castranova, V., Thompson, M. Understanding biophysicochemical interactions at the nano-bio interface. Nature Materials. 8, 543 (2009).
- Gujrati, M., Malamas, A., Shin, T., Jin, E., Sun, Y., Lu, Z. -. R. Multifunctional cationic lipid-based nanoparticles facilitate endosomal escape and reduction-triggered cytosolic siRNA release. Molecular Pharmaceutics. 11, 2734-2744 (2014).
- Zhu, Y., Li, J., Kanvinde, S., Lin, Z., Hazeldine, S., Singh, R. K., Oupický, D. Self-immolative polycations as gene delivery vectors and prodrugs targeting polyamine metabolism in cancer. Molecular Pharmaceutics. 12, 332-341 (2014).
- Planas-Portell, J., Gallart, M., Tiburcio, A. F., Altabella, T. Copper-containing amine oxidases contribute to terminal polyamine oxidation in peroxisomes and apoplast of Arabidopsis thaliana. BMC Plant Biology. 13, 109 (2013).
- Nash, I. A., Bycroft, B. W., Chan, W. C. Dde – A selective primary amine protecting group: A facile solid phase synthetic approach to polyamine conjugates. Tetrahedron Letters. 37, 2625-2628 (1996).
- Ralhan, K., KrishnaKumar, V. G., Gupta, S. Piperazine and DBU: a safer alternative for rapid and efficient Fmoc deprotection in solid phase peptide synthesis. RSC Advances. 5, 104417-104425 (2015).
- Casero, R. A., Marton, L. J. Targeting polyamine metabolism and function in cancer and other hyperproliferative diseases. Nature Reviews Drug Discovery. 6, 373 (2007).
- Wuts, P. G. M., Greene, T. W. . Protection for the Amino Group. In Greene’s Protective Groups in Organic Synthesis. , 696-926 (2006).
- Palasek, S. A., Cox, Z. J., Collins, J. M. Limiting racemization and aspartimide formation in microwave-enhanced Fmoc solid phase peptide synthesis. Journal of Peptide Science. 13, 143-148 (2007).

