Легкий управляемый Ферментативный Декарбоксилирование
Summary
Мы опишем протокол для легкой катализируемой генерации перекиси водорода – кофактор для окислительных превращений.
Abstract
Оксидоредуктазы принадлежат к наиболее применяемых промышленных ферментов. Тем не менее, они нуждаются во внешних электронов, поставка которых часто дорогостоящим и сложным. Рециркуляция NADH доноров электронов или NADPH требует использования дополнительных ферментов и жертвенные субстратов. Интересно отметить, что несколько оксидоредуктаз принимают перекись водорода в качестве донора электронов. Будучи недорогими, этот реагент часто снижает стабильность ферментов. Решение этой проблемы заключается непосредственно в космическом пространстве поколение кофактора. Непрерывная подача кофактора при низкой концентрации приводит в действие реакцию без ухудшения стабильности фермента. Эта статья демонстрирует способ свет катализируемых в месте генерации перекиси водорода на примере гема-зависимого декарбоксилазы жирных кислот Olet JE. Декарбоксилазы жирных кислот Olet JE была обнаружена благодаря своей уникальной способности производить с длинной цепью 1-алкенов из жирных кислот, ранее неизвестному ферментативныхреакция. 1-алкенов широко используются добавки для пластификаторов и смазочных материалов. OLET Ю.Е. было показано , принимать электроны из перекиси водорода для окислительного декарбоксилирования. В то время как добавление перекиси водорода повреждает фермента и приводит к низкой урожайности, в месте генерации кофактора обходит эту проблему. Photobiocatalytic система показывает очевидные преимущества в отношении ферментативной активности и урожайности, что приводит к простой и эффективной системы декарбоксилирования жирных кислот.
Introduction
Изменение климата и предсказуемым истощение возобновляемых ресурсов представляет собой серьезную угрозу для нашего общества. В этом контексте, катализ фермент представляет собой до сих пор не использованы в полной мере потенциал для развития устойчивых и "зеленому" химии 1. Оксидоредуктазы обладают способностью катализировать введение и модификацию функциональных групп в мягких условиях реакции и относятся к наиболее важных биокатализаторов 2. Большинство окислительно-восстановительных преобразований требуют питания внешних кофакторов, таких как NAD (P) H. Методы регенерации кофактора были применены в промышленных масштабах. Тем не менее, они по-прежнему приводит к высокой стоимости процесса, что ограничивает их применение в основном для продуктов с высокой добавленной стоимостью. Интересно отметить , что несколько пероксидазы 3,4 и P450 монооксигеназ 5 принимает электроны из перекиси водорода с помощью так называемого перекисного шунта. В то время как H 2 O 2 является дешевым совместно реагент, он , как сообщается , harmfуль для многих ферментов. Устойчивый к образованию на месте низких концентраций перекиси водорода является жизнеспособным подходом для проведения реакции без ухудшения операционной стабильности фермента.
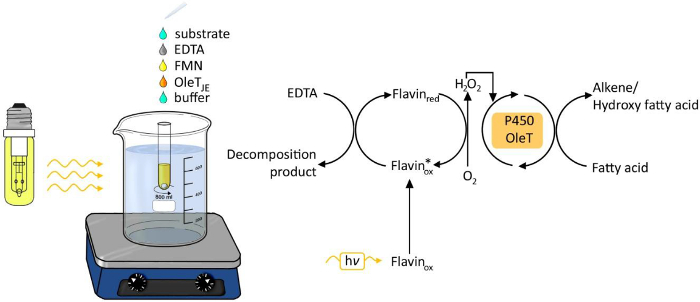
Рисунок 1. Экспериментальная установка из photobiocatalytic декарбоксилирования жирных кислот путем Olet JE. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
Использование света в качестве источника энергии для химических и биологических процессов получает все большее внимание в последние годы 6. Свет управляемой генерации перекиси водорода стала простой и надежный метод для подачи пероксида водорода для окислительно – восстановительных преобразований (рисунок 1). Фотокатализатор такие как флавин аденин пнonucleotide (ФМН) позволяет уменьшить молекулярного кислорода до пероксида водорода, который затем используют в качестве кофактора для ферментативной реакции oxyfunctionalization. Возможные доноры электронов являются этилендиаминтетрауксусная кислота (ЭДТА), аскорбат или недорогой формиат. Метод , как правило , применяется для H 2 O 2 -зависимые ферменты, включая пероксидаз 3,4 и P450 монооксигеназ 5.
Недавно мы исследовали применение нового бактериального декарбоксилазы 7 для превращения природных жиров в олефины 8. Это было бы устойчивым маршрутом для синтеза широко используемых химических веществ платформы из биооснове источника. Декарбоксилазы Olet JE из грамположительной бактерии Jeotgalicoccus зр. катализирует окислительное декарбоксилирование жирных кислот и образует 1-алкенов в качестве продуктов. Olet JE тесно связана с бактериальной P450 монооксигеназ и потребности электронов ером перекиси водорода для реакции.
К сожалению, добавление H 2 O 2 к раствору субстрата и фермента приводит к низкой конверсии и плохой воспроизводимости результатов, по- видимому из – за вредного воздействия перекиси водорода на стабильность OLET JE. Генерация гибридного белка с НАДФН-редуктазы RhFred сделал NADPH-зависимой декарбоксилирование возможно. 9 Тем не менее, высокие цены на NADPH и нынешние ограниченные возможности для экономически эффективного восстановления побудило нас исследовать более дешевые доноров электронов. Воодушевленные сходство Olet JE с P450 монооксигеназ, мы использовали свет катализируемой поколение H 2 O 2. Мы были рады получить высокие конверсии (до> 95%) с использованием бесклеточных экстрактов или очищенные растворы фермента.
На примере декарбоксилирования жирных кислот, мы приводим общий протокол для легкой управляемой ЭнзимАИКТ окислительно-восстановительные преобразования с использованием ФМН в качестве фотокатализатора и перекиси водорода в качестве кофактора. Представленные способы включают в себя получение фермента в рекомбинантной клетке Е. палочка, очистка фермента, применение для синтеза 1-алкенов и анализ продуктов реакции.
Protocol
Representative Results
Discussion
Свет управляемой генерации перекиси водорода может быть применен для целого ряда окислительно – восстановительных преобразований, в том числе peroxygenases 3, chloroperoxidases 10 и P450 Монооксигеназы 5. Это простой и практически подход. В долгосрочной перспективе, использование видимого света открывает перспективу, чтобы использовать солнечный свет для химических превращений, которая является устойчивой альтернативой для богатых энергией реакций.
Метод применим очищенным ферментом или с экстрактом бесклеточной. В то время как последний требует меньше затрат и работы, следует отметить, что малые молекулы, в неочищенном экстракте может помешать световом катализируемой конверсии. Стать реальный подход заключается в удалении этих мелких компонентов , с micromembrane (т.е., с помощью центрифугирования в центробежном блоке фильтров или с помощью диализа). Концентрация молекулы светособирающего ФМН определяет концентрацию перекиси водорода. В зависимости от AFFINIти оксидоредуктазы, эта концентрация имеет решающее значение для ферментативной активности. Еще одним важным фактором является концентрация жертвенного донора электронов ЭДТА. Наиболее важным параметром, однако, является операционная стабильность и активность фермента.
Olefinization жирных кислот является элегантный реакция для превращения биологической основе жирных кислот в олефины, которые принадлежат к основным товарам для химической промышленности. Свет приводом биокаталитическая декарбоксилирование можно проводить при комнатной температуре и при нейтральном значении рН, который предлагает явные преимущества с точки зрения устойчивости.
Наши результаты показывают , что на месте образование перекиси водорода представляет собой стратегию для питания кофактора без ухудшения стабильности фермента, что приводит к высокой конверсии. Современные методы регенерации кофактора используют сельскохозяйственные продукты или бензиновые на основе химических веществ. Легкие реакции, вызванные появляются как возобновляемые альтернативы. БудущееИсследование будет посвящено способам замещения жертвенного ЭДТА реагента дешевыми молекул и уменьшить количество молекул ФМН светособирающего.
Disclosures
The authors have nothing to disclose.
Acknowledgements
R.K. and F.H. are grateful for the EU-commision for financial support within the Marie-Sklodowska ITN Biocascades (Nr. 634200).
Materials
| Chemicals | |||
| Ampicillin | Sigma Aldrich | 69-52-3 | |
| Bradford reagent | Roth | K015.1 | |
| BSA | Sigma Aldrich | 90604-29-8 | |
| DMSO | Sigma Aldrich | 67-68-5 | |
| Ethyl acetate | Fisher Chemical | 141-78-6 | |
| Ethylenediaminetetraacetic acid (EDTA) | Roth | 8043.1 | |
| Riboflavin 5-monophosphate sodium salt hydrate | Sigma Aldrich | 130-40-5 | |
| Hydrochlorid acid 37% | Sigma Aldrich | 7647-01-0 | |
| Hydrogen peroxide 30% | Sigma Aldrich | 7722-84-1 | |
| δ-Amino levulinic acid | Sigma Aldrich | 5451-09-2 | |
| N-Methyl-N-(Trimethylsilyl)trifluoro acetamide (MSTFA) | Sigma Aldrich | 24589-78-4 | |
| Myristic acid >99% | Sigma Aldrich | 208-875-2 | |
| Imidazole | Sigma Aldrich | 288-32-4 | |
| Sodium chloride | Fisher Chemical | 7647-14-5 | |
| Stearic acid >99% | Sigma Aldrich | 57-11-4 | |
| Tetracycline | Sigma Aldrich | 60-54-8 | |
| Tergitol | Sigma Aldrich | MFCD01779855 | |
| Tris(hydroxymethyl)-aminomethan | Sigma Aldrich | 77-86-1 | |
| Name | Company | Catalog Number | Comments |
| Device | |||
| Incubator shaker | G-25CK | New Brunswick Scientific | |
| Ecotron | Infors HT | ||
| Centrifugation | Labofuge 400R | Heraeus | |
| RC 5B Plus | Sorvall | ||
| Fresco 17 | Thermo Scientific | ||
| Centrifugation rotors | SS34 | Sorvall | |
| SLA | Sorvall | ||
| Clean bench | Envirco | Ceag Schirp Reinraum technik | |
| Column GC-FID | CP-Sil 5CB (30 m x 0.25 mmx 0.25 µm) | Agilent Technologies | |
| Column GC-MS | FactorFour Capillary Coloumn (VF-5 ms + 5 m EZ Guard) | Varian | |
| GC-FID | GC-2010 plus | Shimadzu | |
| GC-MS | IST-40 | Varian | |
| Magnetic stirrer | RCT classic | IKA | |
| pH meter | SevenEasy | Mettler toledo | |
| Sonicator | Branson Sonifier 250 | Branson | |
| Spectral photometer | FLUOstar Omega | BMG Labtech | |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Affinity chromatography column | His Pur Ni-NTA spin column | Thermo Scientific | |
| Centricon | Vivaspin turbo 15 | VWR International | |
| Microtiter plates | 96 Well Multiply®PCR Plates | Sarstedt |
References
- Kourist, R., Domìnguez de Marìa, P., Miyamoto, K. Biocatalytic strategies for the asymmetric synthesis of profens – recent trends and developments. Green Chem. , 2607-2618 (2011).
- Holtmann, D., Fraaije, M. W., Arends, I. W., Opperman, D. J., Hollmann, F. The taming of oxygen: biocatalytic oxyfunctionalisations. Chemical Comm. 50, 13180-13200 (2014).
- Churakova, E., et al. Specific photobiocatalytic oxyfunctionalization reactions. Ang. Chem. In. Ed. 123, 10904-10907 (2011).
- Hollmann, F., Arends, I., Buehler, K. Biocatalytic Redox Reactions for Organic Synthesis: Nonconventional Regeneration Methods. ChemCatChem. 2, 762-782 (2010).
- Girhard, M., Kunigk, E., Tihovsky, S., Shumyantseva, V. V., Urlacher, V. B. Light-driven biocatalysis with cytochrome P450 peroxygenases. Biotechnol. Appl. Biochem. 60, 111-118 (2013).
- Bartsch, M., et al. Photosynthetic production of enantioselective biocatalysts. Microb. Cell. Fact. 14, 53 (2015).
- Rude, M. A., et al. Terminal olefin (1-alkene) biosynthesis by a novel P450 fatty acid decarboxylase from Jeotgalicoccus species. Appl. Environ. Microbiol. 77, 1718-1727 (2011).
- Zachos, I., et al. Photobiocatalytic decarboxylation for olefin synthesis. Chem. Comm. 51, 1918-1921 (2015).
- Liu, Y., et al. Hydrogen peroxide-independent production of α-alkenes by OleTJE P450 fatty acid decarboxylase. Biotechnol. Biofuels. 7, 28 (2014).
- Perez, D. I., Grau, M. M., Arends, I. W., Hollmann, F. Visible light-driven and chloroperoxidase-catalyzed oxygenation reactions. Chem. Comm. 40 (44), 6848-6850 (2009).

