Разработка Backbone циклический пептид библиотека как потенциал Противопаразитарные терапии Использование микроволнового облучения
Summary
A simple and general method for the synthesis of cyclic peptides using microwave irradiation is outlined. This procedure enables the synthesis of backbone cyclic peptides with a collection of different conformations while retaining the side chains and the pharmacophoric moieties., and therefore, allows to screen for the bioactive conformation.
Abstract
Белок-белковые взаимодействия (ИПП) принимают непосредственное участие почти во всех биологических процессов и связан со многими заболеваниями человека. Таким образом, есть серьезные усилия, чтобы цель ИЦП в области фундаментальных исследований, так и в фармацевтической промышленности. Белок-белковые интерфейсы, как правило, большие, плоские, и часто не хватает карманов, усложняя открытие малых молекул, которые нацелены на такие сайты. Альтернативные подходы в отношении использованием антител имеют ограничения из-за плохого пероральной биодоступности, низкая клеток проницаемости и неэффективности производства.
Использование пептидов целевой PPI интерфейсы имеет несколько преимуществ. Пептиды имеют более высокую гибкость, конформационные повышенной селективности и, как правило, недороги. Тем не менее, пептиды имеют свои собственные ограничения в том числе плохой стабильности и неэффективность пересечения клеточных мембран. Чтобы преодолеть эти ограничения, пептид циклизации может быть выполнена. Циклизация было продемонстрировано, чтобы улучшить селективность пептид, Метаболическую стабильность, и биодоступность. Тем не менее, предсказания биологически активный конформацию циклического пептида не является тривиальной. Чтобы преодолеть эту проблему, одна подход привлекательным оно для скрининга библиотеки сфокусированный на экране, в котором все магистральные циклические пептиды имеют одинаковую первичную последовательность, но отличаются параметров, влияющих свою конформацию, таких как размер кольца и положении.
Мы описываем подробный протокол для синтеза библиотеку магистральных циклических пептидов, ориентированные на конкретные паразитов ИЦП. Использование рационального подхода к проектированию, мы разработали пептидов, полученных из леса белка L eishmania рецептора активированной киназы С-(отсутствие). Мы предположили, что последовательности в отсутствии, что сохраняющиеся в паразитов, но не в хозяина млекопитающего гомолога, может представлять сайты взаимодействия для белков, которые имеют решающее значение для жизнеспособности паразитов. Циклические пептиды были синтезированы с использованием микроволнового излучения, чтобы уменьшить время реакции и повыситьЭффективность. Разработка библиотеки системообразующих циклических пептидов с различными размерами кольца облегчает систематическое экран для наиболее биологически активной конформации. Этот метод обеспечивает общий, быстрый и легкий путь к синтезу циклических пептидов.
Introduction
Белок-белковые взаимодействия (ИПП) играют ключевую роль в большинстве биологических процессов, от внутриклеточного передачи сигнала к гибели клеток 1. Следовательно, ориентации ИЦП имеет фундаментальное значение для фундаментальных исследований и терапевтического применения. ИПП может регулироваться конкретных и стабильных антител, но антитела дорого и сложно в изготовлении и имеют низкую биодоступность. Кроме того, ИПП может быть мишенью малых молекул. Малые молекулы легче синтезировать и недороги по сравнению с антителами; Однако, они относительно менее гибким и подходит лучше небольших полостей, чем крупные белок-белковых интерфейсов 2,3. Различные исследования показали, что пептиды, которые проще и дешевле, чем антитела и более гибким, чем малые молекулы, могут связываться белковые интерфейсы ИПП и регулировать 4,5. Глобальный рынок терапевтический пептид был оценен примерно пятнадцать миллиардов долларов в 2013 году и растет на 10,5% однолетнийLLY 6. Кроме того, есть более чем 50 продаются пептиды, около 270 пептидов в различных фазах клинических испытаний, и около 400 пептидов в передовых доклинических стадиях 7. Несмотря на многочисленные пептиды используются в качестве лекарственных средств, пептиды по-прежнему представляют несколько проблем, которые ограничивают их широкое применение в том числе плохой биодоступности и стабильности, неэффективности пересечения клеточных мембран, и конформационной гибкости 8,9. Один из вариантов для преодоления этих недостатков является применение различных модификаций, таких как местные (D-аминокислоты и N-алкилирования) и глобальных (циклизации) ограничений 8,10-12. Эти модификации также происходят естественно. Например, циклоспорин А, иммунодепрессант циклический пептид естественно, содержит один D-аминокислоты и подвергается N-алкилирования модификации 13,14.
Модификация природных аминокислот, чтобы вызвать локальные ограничения, такие как D- и N-алкилированием, часто влияет на пептид9, S биологической активности. Тем не менее, циклизация, в котором последовательность интерес может оставаться таким же, скорее всего, чтобы сохранить биологическую активность. Циклизация является весьма привлекательным способом ограничить пептид конформационные пространство за счет уменьшения равновесие между различных конформаций. Это увеличивает биологическую, как правило, активность и селективность путем ограничения пептид в активной конформации, который опосредует только одну функцию. Циклизация также улучшает стабильность пептида, сохраняя пептид в конформации, которая меньше признанной ферменты, разрушающие. Действительно, циклические пептиды были показаны улучшились метаболическую стабильность, биодоступность, и селективность по сравнению с их аналогами линейных 15-17.
Тем не менее, циклизация может быть обоюдоострым мечом, так как в некоторых случаях ограничение может предотвратить пептидов от достижения биологически активный конформацию. Чтобы преодолеть это препятствие, сфокусированный библиотеку, в которой все пептиды в ту же основную sequencе и, следовательно, постоянные фармакофоров могут быть синтезированы. Пептиды в библиотеке отличаются параметрами, которые влияют на их структуру, таких как размер и положение кольца, для того, чтобы впоследствии скрининга наиболее биоактивного конформации 9,18.
Пептиды могут быть синтезированы как в растворе и пептидного синтеза в твердой фазе (SPPS) подхода, который в настоящее время является более распространенным подходом синтез пептидов и будет обсуждаться дальше. SPPS представляет собой процесс, посредством которого химические превращения выполняются на твердой подложке через линкер подготовить широкий спектр синтетических соединений 19. SPPS позволяет их установку пептиды путем последовательного сцепления аминокислот ступенчатым образом от С-конца, который прикреплен к твердой подложке, на N-конце. N-альфа-аминокислот, боковые цепи должен быть экранирован защитных групп, которые стабильны в условиях реакции, используемых при удлинении пептида, чтобы обеспечить добавление одной аминокислоты на стер. На заключительном этапе, пептид высвобождается из смолы и боковой цепью защитные группы удалены одновременно. В то время как пептид синтезируют, все растворимые реагенты могут быть удалены из пептида-твердой подложке матрицы путем фильтрации и смыл в конце каждой стадии связывания. При такой системе, большой избыток реагентов при высокой концентрации может управлять реакции сочетания к завершению, и все стадии синтеза могут быть выполнены в том же сосуде без переноса материала 20.
Хотя SPPS имеет некоторые ограничения, такие как производство неполных реакций, побочных реакций, нечистых реагентов, а также трудности мониторинга реакции 21, преимущества SPPS сделали его "золотым стандартом" для синтеза пептидов. Эти преимущества включают в себя опцию, чтобы включить ненатуральных аминокислот, автоматизация, простое очищение, свернутые физические потери, и использование избытка реагентов, в результате чеговысокие урожаи. SPPS было показано быть чрезвычайно полезным в синтезе сложных последовательностей 21,22, флуоресцентные модификаций 23 и пептидных библиотек 24,25. SPPS также очень полезно для других узлов поли-цепи, такие как олигонуклеотиды, олигосахариды 26,27 28,29, и пептидных нуклеиновых кислот 30,31. Интересно, что в некоторых случаях, SPPS было показано, что выгодно для синтеза малых молекул, которые традиционно изготавливают в растворе 32,33. SPPS используется как в небольших масштабах для научных исследований и преподавания 34,35, а также больших масштабах в промышленности 36-38.
Две стратегии синтеза, которые используются главным образом в методологии SPPS для синтеза пептидов бутилоксикарбонил (Вос) и 9-флуоренилметоксикарбонил (Fmoc). Оригинальный стратегия введена SPPS был Вос, что требует условий сильной кислотой, чтобы удалить боковые защитные группы и отщепления пептида с RЕсин. Fmoc-пептид на основе синтеза, однако, использует умеренные базовых условий и является более мягким альтернативой кислотно-лабильных Boc протокола 39. Стратегия Fmoc использует мультиплексирование с ортогональным трет-бутил (TBU) защиту боковой цепи, который удаляется на последней стадии синтеза, а отщепление пептида от смолы в кислых условиях.
Общий принцип синтеза пептидов на твердом носителе представлена на Рисунке 1. Исходное аминокислоты, маскируется временной защитной группы на N-альфа-конце, загружают на смоле от С-конца. Полупостоянная защитную группу, чтобы замаскировать боковую цепь также используется, если необходимо (Рисунок 1, Шаг 1). Синтез целевого пептида собран из С-конца к N-концу с помощью повторяющихся циклов снятия защиты с N-α-временного защитной группы (рисунок 1, шаг 2) и соединительных следующего защищенной аминокислоты (рис 1 </str Онг> Шаг 3). После последнего аминокислота загружен (Рисунок 1, Шаг 4), пептид отщепл ют от полимерной подложки и полупостоянных защитные группы удаляют (рис 1, Шаг 5).
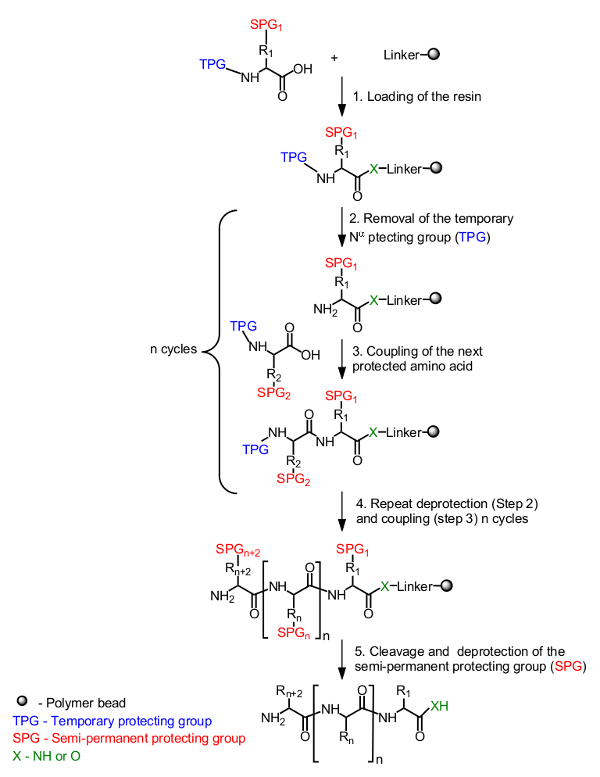
Рисунок 1. Общая схема твердофазного пептидного синтеза. N-α-защищенной аминокислоты закреплена с помощью карбоксильной группы с помощью линкера к смоле (стадия 1). Желаемый пептид, собраны в линейном виде с С-конца к N-концу повторяющихся циклов снятия защиты с временной защищающей группой (ТПГ) из N-альфа (шаг 2) и соединением аминокислот (шаг 3). После выполнения синтез (шаг 4), то полу-постоянные защитные группы (SPG) снимают защиту во время расщепление пептида (шаг 5).получить = "_blank"> Нажмите здесь, чтобы посмотреть большую версию этой фигуры.
После сборки полного пептидной цепи, циклизация может быть достигнуто путем нескольких альтернатив: (А) с головы до хвоста циклизации – это удобный способ, но ограничена, поскольку она обеспечивает только один вариант для циклизации (рис 2А), (б) циклизация с использованием аминокислот из последовательности интерес, которые содержат биологически активные функциональные группы – однако, использование этих аминокислот могут влиять на биологическую активность (Фигура 2В), и (с) циклизацию добавлением аминокислот (или другие строительные блоки), не нарушая биоактивный последовательность. Введение этих молекул широко, как это позволяет производить ориентированных библиотек, не изменяя последовательность интерес (фиг.2с).
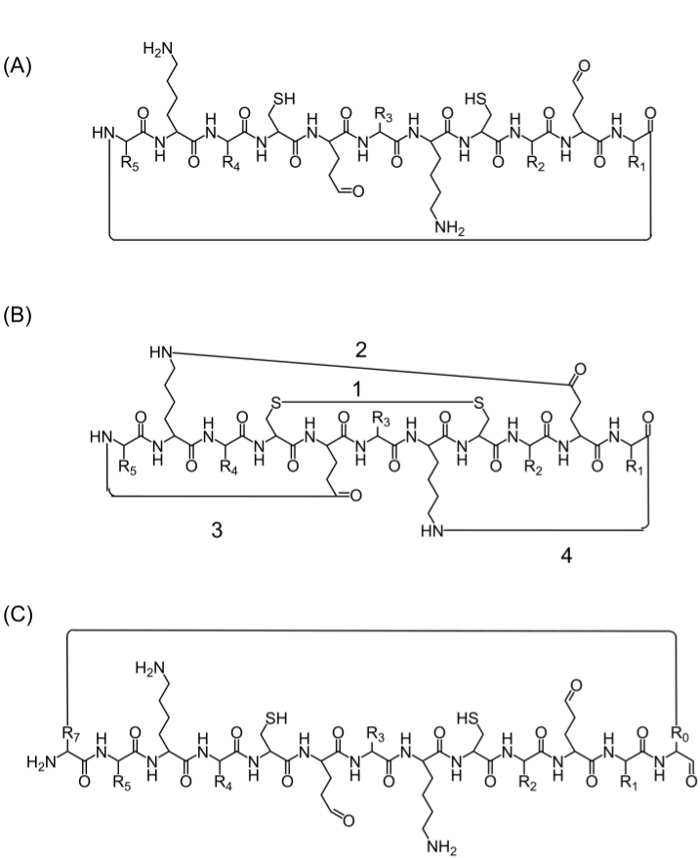
F2. Альтернативный igure пептид циклизации стратегии (А) голова к хвосту циклизации, через пептидную связь между С-концом и N-концом. (Б) циклизации между функциональными группами, такими как дисульфидной связи между остатками цистеина (1) или амидной связи между боковыми цепями лизина к аспарагиновой кислоты / глутаминовой (2), или боковой цепи, чтобы N- или С-конца (3 -4); (С) циклизация путем добавления дополнительных аминокислот или производных аминокислот или небольших молекул, например, перед (R0) и после (R7) биологически активное последовательности. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Микроволновая печь-помощь синтеза использует микроволнового излучения для нагрева реакции, тем самым ускоряя органических химических превращений 40,41. Микроволновая химия основана на способности реагента / растворитель, чтобы поглотитьмикроволновая энергия и конвертировать ее в тепло 42. Перед технология получила широкое распространение, основные недостатки пришлось преодолеть, в том числе управляемости и воспроизводимости протоколов синтеза и отсутствие доступных систем для адекватных температуры и давления управления 43,44. Первый доклад СВЧ-помощь синтеза пептидов проводили с использованием кухня микроволновая синтезировать несколько коротких пептидов (7-10 аминокислот) со значительным улучшением эффективности связи и чистоты 45. Кроме того, микроволновая энергия была показана для уменьшения агрегации цепи, уменьшить побочные реакции, ограничить рацемизацию, и улучшить сцепные ставки, которые все решающее значение для сложных и длинных последовательностей 46-53.
В настоящее время применение микроволнового облучения для синтеза пептидов или родственных соединений на твердой подложке, весьма обширен, в том числе (а) синтеза в воду вместо органического растворителя 54; (В) Синтез пептидов собщие пост-трансляционной модификации, такие как гликопептиды 55-58 или 59-61 фосфопептиды, синтез, как правило, затруднено из-за низкой эффективности связывания стерически затрудненных производных аминокислот; (С) Синтез пептидов с модификацией в основной цепи, например, azapeptides, которые могут быть образованы путем замены C (A) от аминокислотного остатка с атомом азота, 62 или пептоиды, чей боковой цепи соединен с Амид азота, чем атома Cα 63,64; (D), синтез циклических пептидов 65-71; и (Е) Синтез комбинаторных библиотек 51,72. Во многих случаях, авторы сообщили более высокую эффективность и сокращение времени синтеза с использованием микроволнового излучения, по сравнению с обычным протоколом.
Использование рациональную конструкцию 73-75, мы разработали анти-паразитарные пептиды, которые были получены от рецептора эшафот L eishmania в FOг активированного C-киназы (отсутствие). ОТСУТСТВИЕ играет важную роль в ранней фазе инфекции Leishmania 76. Паразиты, выражающие более низкие уровни отсутствия не паразитируют даже ослабленным иммунитетом мышам 77, как отсутствие участвует в основных паразитов сигнализации процессов и синтеза белка 78. Таким образом, не хватает ключевой белок эшафот 79 и ценным объектом наркотиков. Сосредоточение внимания на последовательностях в отсутствии которые сохраняются в паразитов, но не в принимающей млекопитающих гомологов RACK, мы определили пептид 8 аминокислот (RNGQCQRK), что снижение Leishmania зр. Жизнеспособность в культуре.
Здесь мы описываем протокол для синтеза циклических пептидов магистральных, полученных из последовательности белка ОТСУТСТВИЕ описанной выше. Пептиды были синтезированы на твердой подложке с использованием микроволнового нагрева с помощью методологии SPPS с протоколом Fmoc / Tbu. Пептиды, конъюгированный с ТАТ пептид 47-57 (YGRKKRRQRRR) несущей посредством амидной связи, какчасть SPPS. ТАТ на основе транспорт различных грузов в клетки был использован для более чем 15 лет и доставка груза в субклеточных органелл была подтверждена 80. Четыре различных линкеров, янтарная и глутаровый ангидрид, а также адипиновой кислоты и пимелиновой, были использованы для выполнения циклизации генерировать линкеров карбоновых кислот от двух до пяти атомов углерода. Циклизация было сделано с использованием микроволновой энергии и окончательные расщепления и боковой цепи шаги снятия защиты проводили вручную без микроволновой энергии. Применение автоматизированной микроволновой синтезатора улучшило чистоту продукта, увеличение выхода продукта и снижение продолжительности синтеза. Этот общий протокол может быть применен к другим исследований, которые используют пептиды, чтобы понять важную молекулярный механизм в пробирке и в естественных и дальнейшее развитие потенциальных лекарственных препаратов для человека заболеваний.
Protocol
Representative Results
Discussion
Синтез сфокусированного библиотеки магистральных циклических пептидов, полученных из-за отсутствия белка паразита Leishmania использованием полностью автоматизированной микроволновой синтезатор описано. Сосредоточенный библиотека циклических пептидов был разработан с консерват…
Divulgations
The authors have nothing to disclose.
Acknowledgements
Мы благодарим Лорен Ван Wassenhove, Sunhee Хван, и Дарья Mochly-Розен за полезные обсуждения. Работа выполнена при поддержке Национального института здоровья Грант NIH RC4 TW008781-01 C-IDEA (СПАРК) для NQ Доноры не было никакой роли в дизайн исследования, сбора и анализа данных, решение о публикации или подготовки рукописи.
Materials
| REAGENTS | |||
| Solid support, Rink Amide AM resin ML | CBL | BR-1330 | loading: 0.49 mmol/g |
| Fmoc-Ala-OH | Advanced Chemtech | FA2100 | |
| Fmoc-Arg(Pbf)-OH | Advanced Chemtech | FR2136 | |
| Fmoc-Asn(Trt)-OH | Advanced Chemtech | FN2152 | |
| Fmoc-Asp(OBut)-OH | Advanced Chemtech | FD2192 | |
| Fmoc-Cys(Trt)-OH | Advanced Chemtech | FC2214 | |
| Fmoc-Gln(Trt)-OH | Advanced Chemtech | FQ2251 | |
| Fmoc-Glu(OtBu)-OH | Advanced Chemtech | FE2237 | |
| Fmoc-Gly-OH | Advanced Chemtech | FG2275 | |
| Fmoc-His(Trt)-OH | Advanced Chemtech | FH2316 | |
| Fmoc-Ile-OH | Advanced Chemtech | FI2326 | |
| Fmoc-Leu-OH | Advanced Chemtech | FL2350 | |
| Fmoc-Lys(Boc)-OH | Advanced Chemtech | FK2390 | |
| Fmoc-Met-OH | Advanced Chemtech | FM2400 | |
| Fmoc-Phe-OH | Advanced Chemtech | FF2425 | |
| Fmoc-Pro-OH | Advanced Chemtech | FP2450 | |
| Fmoc-Ser-(tBu)-OH | Advanced Chemtech | FS2476 | |
| Fmoc-Thr(tBu)-OH | Advanced Chemtech | FT2518 | |
| Fmoc-Trp(Boc)-OH | Advanced Chemtech | FW2527 | |
| Fmoc-Tyr(But)-OH | Advanced Chemtech | FY2563 | |
| Fmoc-Val-OH | Advanced Chemtech | FV2575 | |
| 1-Methyl-2-pyrrolidinone (NMP) | Sigma | 328634 | Caution Toxic/Highly flammable/Irritant. |
| N,N-Dimethylformamide (DMF) | Alfa Aesar | 43465 | Caution Toxic |
| Use high quality DMF to eliminate side reactions such as Fmoc removal as a result of the dimethylamine traces from DMF decomposition. | |||
| Dichloromethane (DCM) | Sigma | D65100 | Caution Harmful |
| Dibromomethane (DBM) | Sigma | D41868 | Caution Harmful |
| Trifluoroacetic acid (TFA) | Sigma | T62200 | Caution Corrosive/Toxic |
| Trifluoroacetic acid, HPLC grade (TFA) | Sigma | 91707 | Caution Corrosive/Toxic |
| Diethylether | Sigma | 31690 | Caution Highly flammable/Harmful |
| Triisopropylsilane (TIS) | Sigma | 233781 | Caution Irritant/Flammable |
| Water, HPLC grade | Sigma | 270733 | |
| Acetonitroile, HPLC grade (ACN) | Fisher Scientific | A998-4 | Caution Flammable/Irritant/Harmful |
| N,N-Diisopropylethylamine (DIEA) | Sigma | 3440 | Caution Corrosive/Highly flammable |
| Piperidine | Sigma | W290807 | Caution Toxic/Highly flammable |
| Pyridine | Sigma | 270970 | Caution Highly flammable/Harmful |
| Ethanol (EtOH) | Sigma | 459844 | Caution Highly flammable/Irritant |
| 1-Hydroxybenzotriazole hydrate (HOBt) | Sigma | 157260 | Caution Highly flammable/Irritant/Harmful |
| O-(Benzotriazol-1-yl)-N,N,N′,N′-tetramethyluronium hexafluorophosphate (HBTU) | Sigma | 12804 | Caution Irritant/Harmful |
| Benzotriazole-1-ly-oxy-tris-pyrrolidinophosphonium hexafluorphosphate (PyBOP) | Advanced Chemtech | RC8602 | Caution Irritant |
| Ninhydrin | Sigma | 454044 | Caution Harmful |
| Phenol | Sigma | P3653 | Caution Corrosive/Toxic |
| Potassium cyanide (KCN) | Sigma | 11813 | Caution Very Toxic |
| Potassium hydroxide (KOH) | Sigma | 221473 | Caution Toxic |
| N,N’- | Sigma | 38370 | Caution Flammable/ Toxic |
| Diisopropylcarbodiimide (DIC) | |||
| 4-Dimethylaminopyridine (DMAP) | Sigma | 522805 | Caution Toxic/Irritant |
| Glutaric anhydride | Sigma | G3806 | Caution Flammable/Irritant/Harmful |
| Succinic anhydride | Sigma | 239690 | Caution Irritant/Harmful |
| Adipic acid | Sigma | A26357 | Caution Toxic/Irritant |
| Pimelic acid | Sigma | P45001 | Caution Toxic/Irritant |
| Chloranil | Sigma | 23290 | Caution Toxic/Irritant |
| Acetaldehyde | Sigma | 402788 | Caution Flammable/ Toxic |
| EQUIPMENT | |||
| Name | Company | Catalog Number | Comments |
| Centrifuge | Beckman Coulter | Allegra 6R centrifuge | |
| Lyophilizer | Labconco | freezone 4.5 | |
| Vacuum pump | Franklin Electric | model 1101101416 with 3/4 HP | Alcatel pump with Franklin Motor |
| Polypropylene cartridge 12 ml | Applied Separation | 2419 | |
| Cap plug for 12 ml polypropylene cartridge | Applied Separation | 8157 | |
| Polypropylene cartridge 3 ml | Applied Separation | 2413 | |
| Cap plug for 3 ml polypropylene cartridge | Applied Separation | 8054 | |
| Stop cocks PTFE | Applied Separation | 2406 | |
| Tubes flat, 50 ml | VWR | 21008-240 | |
| Extraction manifold, 20 pos, 16 x 100 mm tubes | Waters | WAT200609 | |
| Shaker, BD adams™ nutator mixer | Fisher scientific | 22363152 | |
| Nalgene HDPE narrow mouth IP2 bottles, 125 ml | Fisher scientific | 03-312-8 | |
| Erlenmeyer flask | Fisher Scientific | FB-501, 500 ml | |
| Heating block | Thermolyne | 1760 dri bath | |
| Disposable borosilicate glass tubes with plain end | Fisher Scientific | 14-961-25 | |
| Micropipettes and tips Finnpipette | Thermo | 20–200 and 100–1,000 μl | |
| HPLC vials – micro vl pp 400 µl PK100 | VWR | 69400-124 | |
| HPLC vial- Blue Snap-It Cap | VWR | 66030-600 | |
| Analytical HPLC column | Peeke Scientific | U1-5C18Q-JJ | ultro 120 5 µm C18Q, 4.6 mm ID 150 mm |
| Prep HPLC column, XBridge | Waters | OBD C18 5 µm column | 19 mm × 150 mm |
| Mass spectrometer | Applied Biosystems | Voyager DE-RP |
References
- Wells, J. A., McClendon, C. L. Reaching for high-hanging fruit in drug discovery at protein-protein interfaces. Nature. 450 (7172), 1001-1009 (2007).
- Arkin, M. R., Wells, J. A. Small-molecule inhibitors of protein-protein interactions: progressing towards the dream. Nat Rev Drug Discov. (4), 301-317 (2004).
- Mandell, D. J., Kortemme, T. Computer-aided design of functional protein interactions. Nat. Chem. Biol. 5 (11), 797-807 (2009).
- Friedler, A., et al. Backbone cyclic peptide, which mimics the nuclear localization signal of human immunodeficiency virus type 1 matrix protein, inhibits nuclear import and virus production in nondividing cells. Biochimie. 37 (16), 5616-5622 (1998).
- Brandman, R., Disatnik, M. H., Churchill, E., Mochly-Rosen, D. Peptides derived from the C2 domain of protein kinase C epsilon (epsilon PKC) modulate epsilon PKC activity and identify potential protein-protein interaction surfaces. J. Biol. Chem. 282 (6), 4113-4123 (2007).
- Vlieghe, P., Lisowski, V., Martinez, J., Khrestchatisky, M. Synthetic therapeutic peptides: science and market. Drug discov today. 15 (1-2), 40-56 (2010).
- Marx, V. Watching Peptide Drugs Grow Up. Chemical & Engineering News. 83, 17-24 (2005).
- Denicourt, C., Dowdy, S. F. Medicine. Targeting apoptotic pathways in cancer cells. Science. 305 (5689), 1411-1413 (2004).
- Qvit, N., et al. Synthesis of a novel macrocyclic library: discovery of an IGF-1R inhibitor. J Comb Chem. 10 (2), 256-266 (2008).
- Patch, J. A., Barron, A. E. Mimicry of bioactive peptides via non-natural, sequence-specific peptidomimetic oligomers. Curr. Opin. Chem. Biol. 6 (6), 872-877 (2002).
- Kessler, H. Peptide Conformations .19. Conformation and Biological-Activity of Cyclic-Peptides. Angew. Chem. Int. Ed. Engl. 21 (7), 512-523 (1982).
- Gazal, S., Gelerman, G., Gilon, C. Novel Gly building units for backbone cyclization: synthesis and incorporation into model peptides. Peptides. 24 (12), 1847-1852 (2003).
- Fesik, S. W., et al. NMR studies of [U-13C]cyclosporin A bound to cyclophilin: bound conformation and portions of cyclosporin involved in binding. Biochimie. 30 (26), 6574-6583 (1991).
- Kornfeld, O. S., et al. Mitochondrial Reactive Oxygen Species at the Heart of the Matter: New Therapeutic Approaches for Cardiovascular Diseases. Circ. Res. 116 (11), 1783-1799 (2015).
- Boguslavsky, V., Hruby, V. J., O’Brien, D. F., Misicka, A., Lipkowski, A. W. Effect of peptide conformation on membrane permeability. J. Pept. Res. 61 (6), 287-297 (2003).
- Eguchi, M., et al. Solid-phase synthesis and structural analysis of bicyclic beta-turn mimetics incorporating functionality at the i to i+3 positions. J. Am. Chem. Soc. 121 (51), 12204-12205 (1999).
- Altstein, M., et al. Backbone cyclic peptide antagonists, derived from the insect pheromone biosynthesis activating neuropeptide, inhibit sex pheromone biosynthesis in moths. J. Biol. Chem. 274 (25), 17573-17579 (1999).
- Cheng, M. F., Fang, J. M. Liquid-phase combinatorial synthesis of 1,4-benzodiazepine-2,5-diones as the candidates of endothelin receptor antagonism. J. Comb. Chem. 6 (1), 99-104 (2004).
- Merrifield, R. B. Solid Phase Peptide Synthesis I. the Synthesis of a Tetrapeptide. J. Am. Chem. Soc. 85, 2149-2154 (1963).
- Pfeiffer, C. T., Schafmeister, C. E. Solid phase synthesis of a functionalized bis-peptide using ‘safety catch’ methodology. J Vis Exp. (63), e4112 (2012).
- Coin, I., Beyermann, M., Bienert, M. Solid-phase peptide synthesis: from standard procedures to the synthesis of difficult sequences. Nat. Protoc. 2 (12), 3247-3256 (2007).
- Qvit, N., et al. Design and synthesis of backbone cyclic phosphorylated peptides: the IκB model. Biopolymers. 91 (2), 157-168 (2009).
- Sainlos, M., Imperiali, B. Tools for investigating peptide-protein interactions: peptide incorporation of environment-sensitive fluorophores through SPPS-based ‘building block’ approach. Nat. Protoc. 2 (12), 3210-3218 (2007).
- Hilpert, K., Winkler, D. F., Hancock, R. E. Peptide arrays on cellulose support: SPOT synthesis, a time and cost efficient method for synthesis of large numbers of peptides in a parallel and addressable fashion. Nat. Protoc. 2 (6), 1333-1349 (2007).
- Qi, X., Qvit, N., Su, Y. C., Mochly-Rosen, D. A novel Drp1 inhibitor diminishes aberrant mitochondrial fission and neurotoxicity. J. Cell Sci. 126 (Pt 3), 789-802 (2013).
- Beaucage, S. L. Solid-phase synthesis of siRNA oligonucleotides. Curr. Opin. Drug Discovery Dev. 11 (2), 203-216 (2008).
- Dhanawat, M., Shrivastava, S. K. Solid-Phase Synthesis of Oligosaccharide Drugs: A Review. Mini Rev Med Chem. 9 (2), 169-185 (2009).
- Seeberger, P. H., Werz, D. B. Synthesis and medical applications of oligosaccharides. Nature. 446 (7139), 1046-1051 (2007).
- Plante, O. J., Palmacci, E. R., Seeberger, P. H. Automated solid-phase synthesis of oligosaccharides. Science. 291 (5508), 1523-1527 (2001).
- Komiyama, M., Aiba, Y., Ishizuka, T., Sumaoka, J. Solid-phase synthesis of pseudo-complementary peptide nucleic acids. Nat. Protoc. 3 (4), 646-654 (2008).
- Christensen, L., et al. Solid-Phase synthesis of peptide nucleic acids. J. Pept. Sci. 1 (3), 175-183 (1995).
- Qvit, N., et al. Development of bifunctional photoactivatable benzophenone probes and their application to glycoside substrates. Biopolymers. 90 (4), 526-536 (2008).
- O’Neill, J. C., Blackwell, H. E. Solid-phase and microwave-assisted syntheses of 2,5-diketopiperazines: small molecules with great potential. Comb Chem High Throughput Screen. 10 (10), 857-876 (2007).
- Qvit, N., Barda, Y., Shalev, D., Gilon, C. A Laboratory Preparation of Aspartame Analogs Using Simultaneous Multiple Parallel Synthesis Methodology. J. Chem. Educ. 84 (12), 1988-1991 (2007).
- Truran, G. A., Aiken, K. S., Fleming, T. R., Webb, P. J., Markgraf, J. H. Solid phase organic synthesis and combinatorial chemistry: A laboratory preparation of oligopeptides. J. Chem. Educ. 79 (1), 85-86 (2002).
- Verlander, M. Industrial applications of solid-phase peptide synthesis – A status report. Int. J. Pept. Res. Ther. 13 (1-2), 75-82 (2007).
- Bray, B. L. Large-scale manufacture of peptide therapeutics by chemical synthesis. Nature reviews. Drug discovery. 2 (7), 587-593 (2003).
- Qvit, N. Development and therapeutic applications of oligonucleotides and peptides. chimica Oggi / CHEMISTRY today. 29 (2), 4-7 (2011).
- Carpino, L. A., Han, G. Y. 9-Fluorenylmethoxycarbonyl Amino-Protecting Group. J. Org. Chem. 37 (22), 3404-3409 (1972).
- Gedye, R., et al. The use of microwave ovens for rapid organic synthesis. Tetrahedron Lett. 27 (3), 279-282 (1986).
- Giguere, R. J., Bray, T. L., Duncan, S. M., Majetich, G. Application of commercial microwave ovens to organic synthesis. Tetrahedron Lett. 27 (41), 4945-4948 (1986).
- Kappe, C. O., Dallinger, D. The impact of microwave synthesis on drug discovery. Nature reviews. Drug discovery. 5 (1), 51-63 (2006).
- Kappe, C. O. Controlled microwave heating in modern organic synthesis. Angew. Chem. Int. Ed. Engl. 43 (46), 6250-6284 (2004).
- de la Hoz, A., Diaz-Ortiz, A., Moreno, A. Microwaves in organic synthesis. Thermal and non-thermal microwave effects. Chem. Soc. Rev. 34 (2), 164-178 (2005).
- Yu, H. M., Chen, S. T., Wang, K. T. Enhanced coupling efficiency in solid-phase peptide synthesis by microwave irradiation. J. Org. Chem. 57 (18), 4781-4784 (1992).
- Mingos, D. M. P., Baghurst, D. R. Tilden Lecture. Applications of microwave dielectric heating effects to synthetic problems in chemistry. Chem. Soc. Rev. 20 (1), 1-47 (1991).
- Gabriel, C., Gabriel, S., Grant, E. H., Halstead, B. S. J., Mingos, D. M. P. Dielectric parameters relevant to microwave dielectric heating. Chem. Soc. Rev. 27 (3), 213-224 (1998).
- Sabatino, G., Papini, A. M. Advances in automatic, manual and microwave-assisted solid-phase peptide synthesis. Curr. Opin. Drug Discovery Dev. 11 (6), 762-770 (2008).
- Banerjee, J., Hanson, A. J., Muhonen, W. W., Shabb, J. B., Mallik, S. Microwave-assisted synthesis of triple-helical, collagen-mimetic lipopeptides. Nat. Protoc. 5 (1), 39-50 (2010).
- Bacsa, B., Kappe, C. O. Rapid solid-phase synthesis of a calmodulin-binding peptide using controlled microwave irradiation. Nat. Protoc. 2 (9), 2222-2227 (2007).
- Murray, J. K., Gellman, S. H. Parallel synthesis of peptide libraries using microwave irradiation. Nat. Protoc. 2 (3), 624-631 (2007).
- Palasek, S. A., Cox, Z. J., Collins, J. M. Limiting racemization and aspartimide formation in microwave-enhanced Fmoc solid phase peptide synthesis. J Pept Sci. 13 (3), 143-148 (2007).
- Murray, J. K., Aral, J., Miranda, L. P. Solid-Phase Peptide Synthesis Using Microwave Irradiation. Methods Mol. Biol. 716, 73-88 (2011).
- Galanis, A. S., Albericio, F., Grotli, M. Solid-Phase Peptide Synthesis in Water Using Microwave-Assisted Heating. Organic Letters. 11 (20), 4488-4491 (2009).
- Rizzolo, F., Sabatino, G., Chelli, M., Rovero, P., Papini, A. M. A convenient microwave-enhanced solid-phase synthesis of difficult peptide sequences: Case study of Gramicidin A and CSF114(Glc). Int. J. Pept. Res. Ther. 13 (1-2), 203-208 (2007).
- Matsushita, T., Hinou, H., Kurogochi, M., Shimizu, H., Nishimura, S. Rapid microwave-assisted solid-phase glycopeptide synthesis. Org Lett. 7 (5), 877-880 (2005).
- Nagaike, F., et al. Efficient microwave-assisted tandem N- to S-acyl transfer and thioester exchange for the preparation of a glycosylated peptide thioester. Org Lett. 8 (20), 4465-4468 (2006).
- Naruchi, K., et al. Construction and structural characterization of versatile lactosaminoglycan-related compound library for the synthesis of complex glycopeptides and glycosphingolipids. J. Org. Chem. 71 (26), 9609-9621 (2006).
- Brandt, M., Gammeltoft, S., Jensen, K. J. Microwave heating for solid-phase peptide synthesis: General evaluation and application to 15-mer phosphopeptides. Int. J. Pept. Res. Ther. 12 (4), 349-357 (2006).
- Harris, P. W. R., Williams, G. M., Shepherd, P., Brimble, M. A. The Synthesis of Phosphopeptides Using Microwave-assisted Solid Phase Peptide Synthesis. Int. J. Pept. Res. Ther. 14 (4), 387-392 (2008).
- Qvit, N. Microwave-assisted Synthesis of Cyclic Phosphopeptide on Solid Support. Chem. Biol. Drug Des. 85 (3), 300-305 (2014).
- Kato, D., Verhelst, S. H., Sexton, K. B., Bogyo, M. A general solid phase method for the preparation of diverse azapeptide probes directed against cysteine proteases. Org Lett. 7 (25), 5649-5652 (2005).
- Olivos, H. J., Alluri, P. G., Reddy, M. M., Salony, D., Kodadek, T. Microwave-assisted solid-phase synthesis of peptoids. Org Lett. 4 (23), 4057-4059 (2002).
- Gorske, B. C., Jewell, S. A., Guerard, E. J., Blackwell, H. E. Expedient synthesis and design strategies for new peptoid construction. Org Lett. 7 (8), 1521-1524 (2005).
- Grieco, P., et al. Design and microwave-assisted synthesis of novel macrocyclic peptides active at melanocortin receptors: discovery of potent and selective hMC5R receptor antagonists. J. Med. Chem. 51 (9), 2701-2707 (2008).
- Boutard, N., Jamieson, A. G., Ong, H., Lubell, W. D. Structure-Activity Analysis of the Growth Hormone Secretagogue GHRP-6 by alpha- and beta-Amino gamma-Lactam Positional Scanning. Chem. Biol. Drug Des. 75 (1), 40-50 (2010).
- Jamieson, A. G., et al. Positional scanning for peptide secondary structure by systematic solid-phase synthesis of amino lactam peptides. J. Am. Chem. Soc. 131 (22), 7917-7927 (2009).
- Hossain, M. A., Bathgate, R. A. D., Tregear, G., Wade, J. D. De Novo Design and Synthesis of Cyclic and Linear Peptides to Mimic the Binding Cassette of Human Relaxin. Annals of the New York Academy of Sciences. 1160, 16-19 (2009).
- Fowler, S. A., Stacy, D. M., Blackwell, H. E. Design and synthesis of macrocyclic peptomers as mimics of a quorum sensing signal from Staphylococcus aureus. Org Lett. 10 (12), 2329-2332 (2008).
- Cemazar, M., Craik, D. J. Microwave-assisted Boc-solid phase peptide synthesis of cyclic cysteine-rich peptides. J Pept Sci. 14 (6), 683-689 (2008).
- Miles, S. M., Leatherbarrow, R. J., Marsden, S. P., Coates, W. J. Synthesis and bio-assay of RCM-derived Bowman-Birk inhibitor analogues. Org Biomol Chem. 2 (3), 281-283 (2004).
- Murray, J. K., et al. Efficient synthesis of a beta-peptide combinatorial library with microwave irradiation. J. Am. Chem. Soc. 127 (38), 13271-13280 (2005).
- Churchill, E. N., Qvit, N., Mochly-Rosen, D. Rationally designed peptide regulators of protein kinase. C. Trends Endocrinol. Metab. 20 (1), 25-33 (2009).
- Mochly-Rosen, D., Qvit, N. Peptide inhibitors of protein-protein interactions. chimica Oggi / CHEMISTRY today. 28 (1), 14-16 (2010).
- Qvit, N., Mochly-Rosen, D. Highly specific modulators of protein kinase C localization: applications to heart failure. Drug Discov. Today Dis. Mech. 7 (2), e87-e93 (2010).
- Mougneau, E., et al. Expression cloning of a protective Leishmania antigen. Science. 268 (5210), 563-566 (1995).
- Kelly, B. L., Stetson, D. B., Locksley, R. M. Leishmania major LACK antigen is required for efficient vertebrate parasitization. J. Exp. Med. 198 (11), 1689-1698 (2003).
- Choudhury, K., et al. Trypanosomatid RACK1 orthologs show functional differences associated with translation despite similar roles in Leishmania pathogenesis. PLoS One. 6 (6), e20710 (2011).
- Gonzalez-Aseguinolaza, G., Taladriz, S., Marquet, A., Larraga, V. Molecular cloning, cell localization and binding affinity to DNA replication proteins of the p36/LACK protective antigen from Leishmania infantum. Eur. J. Biochem. 259 (3), 909-916 (1999).
- Gump, J. M., Dowdy, S. F. TAT transduction: the molecular mechanism and therapeutic prospects. Trends Mol. Med. 13 (10), 443-448 (2007).
- Aletras, A., Barlos, K., Gatos, D., Koutsogianni, S., Mamos, P. Preparation of the very acid-sensitive Fmoc-Lys(Mtt)-OH. Application in the synthesis of side-chain to side-chain cyclic peptides and oligolysine cores suitable for the solid-phase assembly of MAPs and TASPs. Int. J. Pept. Protein Res. 45 (5), 488-496 (1995).
- Li, D., Elbert, D. L. The kinetics of the removal of the N-methyltrityl (Mtt) group during the synthesis of branched peptides. J. Pept. Res. 60 (5), 300-303 (2002).
- Bourel, L., Carion, O., Gras-Masse, H., Melnyk, O. The deprotection of Lys(Mtt) revisited. J Pept Sci. 6 (6), 264-270 (2000).
- Tran, H., Gael, S. L., Connolly, M. D., Zuckermann, R. N. Solid-phase submonomer synthesis of peptoid polymers and their self-assembly into highly-ordered nanosheets. J Vis Exp. (57), e3373 (2011).
- Kaiser, E., Colescot, R. L., Bossinge, C. D., Cook, P. I. Color Test for Detection of Free Terminal Amino Groups in Solid-Phase Synthesis of Peptides. Anal. Biochem. 34 (2), 595-598 (1970).
- Christensen, T. Qualitative Test for Monitoring Coupling Completeness in Solid-Phase Peptide-Synthesis Using Chloranil. Acta Chem. Scand. Ser.B-Org. Chem. Biochem. 33 (10), 763-766 (1979).
- Qvit, N., Crapster, J. A. Peptides that Target Protein-Protein Interactions as an Anti-Parasite Strategy. chimica Oggi / CHEMISTRY today. 32 (6), 62-66 (2014).
- Byk, G., et al. Synthesis and biological activity of NK-1 selective, N-backbone cyclic analogs of the C-terminal hexapeptide of substance P. J. Med. Chem. 39 (16), 3174-3178 (1996).
- King, D. S., Fields, C. G., Fields, G. B. A cleavage method which minimizes side reactions following Fmoc solid phase peptide synthesis. Int. J. Pept. Protein Res. 36 (3), 255-266 (1990).
- Pedersen, S. L., Tofteng, A. P., Malik, L., Jensen, K. J. Microwave heating in solid-phase peptide synthesis. Chemical Society Reviews. 41 (5), 1826-1844 (2012).
- Colangelo, A. M., et al. A new nerve growth factor-mimetic peptide active on neuropathic pain in rats. J. Neurosci. 28 (11), 2698-2709 (2008).
- Mesfin, F. B., Andersen, T. T., Jacobson, H. I., Zhu, S., Bennett, J. A. Development of a synthetic cyclized peptide derived from alpha-fetoprotein that prevents the growth of human breast cancer. J. Pept. Res. 58 (3), 246-256 (2001).
- Mizejewski, G. J., Muehlemann, M., Dauphinee, M. Update of alpha fetoprotein growth-inhibitory peptides as biotherapeutic agents for tumor growth and metastasis. Chemotherapy. 52 (2), 83-90 (2006).

