Tynnsjiktskromatografiske (TLC) separasjoner og biologiske tester av planteekstrakter for å identifisere antimikrobielle forbindelser
Summary
Fremgangsmåter er beskrevet for tynn-sjikt kromatografi (TLC) separering av planteekstrakter og kontakt bioautography for å identifisere anti-bakterielle metabolitter. Metodene brukes på screening av rød kløver fenoliske forbindelser som hemmer hyper ammoniakk-produserende bakterier (HAB) innfødt til storfe vomma.
Abstract
En felles skjerm for plante antimikrobielle forbindelser består av separering av plante-ekstrakter med papir-eller tynnsjikt-kromatografi (PC eller TLC), utsette kromatogrammene til mikrobielle suspensjoner (for eksempel sopp eller bakterier i buljong eller agar), slik at tiden for mikrobene til å vokse i et fuktig miljø, og visualisere soner uten mikrobiell vekst. Effektiviteten av denne screening-metoden, kjent som bioautography, avhenger både av kvaliteten av kromatografisk separasjon og av nøyaktigheten med mikrobiell kultur forhold. Dette notatet beskriver standardprotokoller for TLC og kontakt bioautography med en roman søknad til aminosyre-fermen bakterier. Ekstraktet separeres på fleksible (aluminium-støttet) silica TLC-plater og bånd blir visualisert under ultrafiolett (UV) lys. Sonene er skåret ut og inkubert med forsiden ned på agar podet med forsøksmikroorganisme. Hemmende band er visualisert ved farging på agarplates med tetrazolium rødt. Metoden brukes til separasjon av rødkløver (Trifolium pratense cv. Kenland) fenoliske forbindelser og deres screening for aktivitet mot Clostridium sticklandii, en hyper ammoniakk-produserende bakterie (HAB) som er innfødt til storfe vomma. TLC fremgangsmåter gjelder for mange typer av plante-ekstrakter og andre bakteriearter (aerobe eller anaerobe), så vel som sopp, kan anvendes som testorganismer dersom dyrkningsbetingelser er modifisert for å passe til de vekstbetingelser av arten.
Introduction
Analysering med hensyn antimikrobielle forbindelser i planter trenger å skille komponentene av et planteekstrakt, utsette et testmikroorganisme til disse komponentene, og å bestemme om mikroorganismene er veksten hemmes av en hvilken som helst av forbindelsene. Separasjoner av papir eller tynn-sjiktskromatografi (PC eller TLC) er fordelaktig fordi mange forbindelser kan separeres på en plan overflate. Separasjon er basert på polaritet, med enkelte forbindelser binding tett til adsorpsjonsmidlet (cellulose i tilfelle av PC, og en rekke av adsorbenter i tilfelle av TLC) og migrering mindre enn andre en. Figur 1 gir et eksempel på de relative posisjonene polare og ikke-polare fenoliske forbindelser etter separasjon på en silika-TLC-plate.
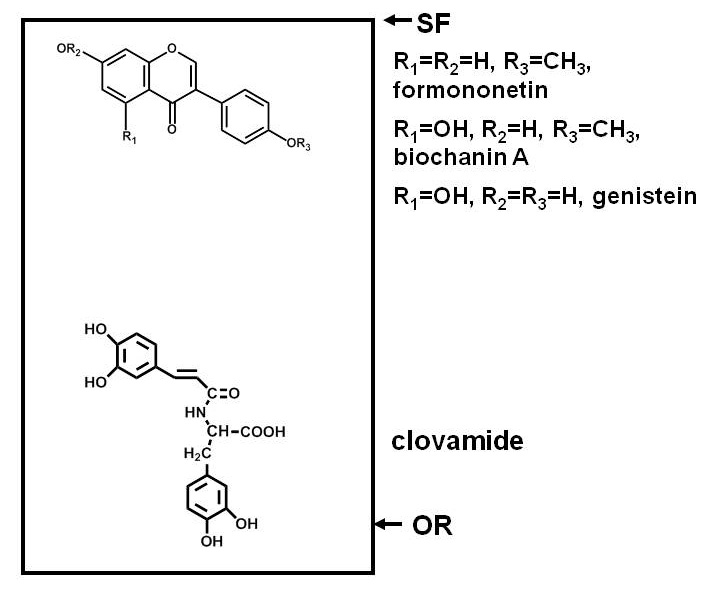
Figur 1. Diagram som illustrerer fordelinger av forbindelser med forskjellige polariteter etter separasjon på en silika-tynnsjikt kromatografi (TLC)-plate. Fenoliske forbindelser av rødkløver (Trifolium pratense L.) brukes som eksempel. Polare forbindelser, for eksempel clovamide, har en sterk affinitet for et polart adsorpsjonsmiddel som silika, og forblir i nærheten av origo (OR), mens mindre polare forbindelser, slik som de tre isoflavoner nær løsningsmiddelfronten (SF), partisjon lettere i løsningsmidlene (som er mindre polar enn silica med mindre vann, syrer eller baser er inkludert) og vandrer lenger opp tallerkenen.
Etter separasjon av en ekstrakt på en TLC-plate, kan test mikroorganismer utsatt for alle forbindelser på platen, og dermed påskynde identifikasjon av de aktive komponentene av en ekstrakt 2.. Hvis en sopp-eller bakteriekultur blir utsatt for kromatogrammet, oppstår mikrobiell vekst overalt unntatt over områder med vekst-inhibitory forbindelser. Soner av inhibering deretter kan visualiseres ved å observere kontrasten mellom mycelial vekst og vekstfrie områder hvis sopper har blitt anvendt 3, eller ved sprøyting med forbindelser som endrer farge når det reduseres eller hydrolyseres ved hjelp av levende celler 4.. Selv om bruken av papir eller tynnsjiktskromatogrammer for antimikrobielle analyser først ble brukt på antibiotika 5 og soppmidler 3,6, er planteekstrakter nå ofte skjermet for antimikrobielle forbindelser med denne metoden, ofte referert til som bioautography. De protokoller som her er beskrevet gjelder bioautography av tynnsjiktskromatogrammer. TLC er mye brukt fordi den er relativt rask og kan utføres på forskjellige adsorbenter (f.eks silika, stivelse, alumina), i tillegg til å gi god oppløsning og sensitivitet 1..
Planteekstrakter kan være forberedt på TLC på mange måter. Vanlige metoder inkluderer utdrager plantemateriale i alcohol-vann-blandinger som for eksempel 80% etanol 7,8, eventuelt med tilsetning av syre eller base 9. Etter en ekstraksjon i slike løsningsmidler, som inneholder litt vann, og er eventuelt sur eller basisk, må ekstrakter konsentreres, slik at de kan brukes på TLC-plater i et minimalt volum. Konsentrasjonen av alkohol-vann-ekstrakter kan oppnås ved oppdeling av med vann blandbare organiske oppløsningsmidler 8 eller med en blanding av slike oppløsningsmidler, slik som etyl-acetat-etyleter (01:01, v / v) 10,11. Forskjellige plante metabolitter blir ekstrahert inn i forskjellige organiske løsningsmidler, avhengig av deres polaritet. For å sikre at plante organiske syrer eller baser er ekstrahert i organiske oppløsningsmidler på dette stadiet, kan pH i en alkohol-vann-ekstrakt heves eller senkes med en vann-oppløselig syre eller base for å konvertere dissosiert analytter i sine nondissociated former, som deretter løselig i nøytrale organiske løsemidler ni. Den organiske fase kan deretter einndampet under redusert trykk og under nitrogen og ble justert til ønsket volum for TLC. PH i ekstraktet er lite sannsynlig å være dødelig for bioassay mikroorganismer på grunn av oppdeling av analytter i nøytrale oppløsningsmidler, små sluttvolum, og fordampning av ekstraktet på TLC-platen før separasjon.
Både sopp og bakterier er ansatt som testmikroorganismer i bioautography av planteekstrakter to. Sporer av noen sopper, slik som Cladosporium cucumerinum, spire på TLC-plater (bortsett fra områder med inhiberende forbindelser) hvis sprøytet på plater i en næringsoppløsning, og inkubert i et fuktig miljø i flere dager 3. Den mørke mycelium av C. cucumerinum på noninhibitory soner gir en skarp kontrast til soner uten mycelial vekst. Selv om bakterier er blitt anvendt på tynnsjiktskromatografi (TLC) plater på samme måte 4,12, blir bakterier også helles over TLCplate overflater i agar overlegg 13,14. Gjær, slik som Candida albicans, kan anvendes i agar overlegg så vel 14. Alternativt kan TLC-plater legges med forsiden ned på agar inokulert med bakterier 10,15 eller gjær 8, en metode som kalles kontakt bioautography to.
Vi beskriver en metode for kontakt bioautography å screene for antimikrobielle fenoliske forbindelser fra rødkløver (Trifolium pratense cv. Kenland). Testen mikroorganisme er Clostridium sticklandii, en ruminalt hyper ammoniakk-produserende bakterie (HAB) og forplikte anaerobt. Selv om de separasjoner som brukes ikke løser alle komponentene i ekstrakten, er de lette å identifisere soner med antimikrobiell aktivitet, og dermed begrense utvalget av mulige antimikrobielle forbindelser. Protokollen benytter standardprosedyrer for TLC en. Protokollen beskriver også noen av de teknikker som kreves for dyrking forplikgate anaerober for en slik assay, en bruk av kontakt bioautography 15 og en visualisering metode med et tetrazoliumsalt, som flekker levende celler 2,4.
Protocol
Representative Results
Discussion
Denne protokollen beskriver en enkel metode for separering av en ekstrakt til undergrupper av forbindelser, og analysering av disse undergrupper av kontakt bioautography. Fremgangsmåten er ganske lik den som brukes av Chomnawang et al. 15. for å screene for plante metabolitter hemmende til gonoré-bakterier. Den type bioautography ansatt til skjermen for antimikrobielle plantesammensetninger avhenger av mange faktorer, blant annet testmikroorganisme, laboratorieoppsett, og preferansene til den pers…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker den avdøde Dr. Norm Taylor, Dept. Plant og Soil Science ved University of Kentucky, for å tillate oss å bruke samples fra hans røde kløver tomter for denne studien. Dette prosjektet ble finansiert av United States Department of Agriculture.
Materials
| Silica F254 TLC plates, aluminum-backed, 0.2 mm thickness, 20 × 20 cm | EMD Chemicals | 5554/7 | These plates are coated with silica that contains an indicator fluorescing at 254 nm. Compounds absorbing at that wavelength appear dark on a fluorescent green background. Alternative sources include Analtech, Selecto Scientific, Fluka. Adsorbents other than silica may be needed. Plastic-backed plates may be suitable, depending on the solvents to be used. |
| Sharp, heavy-duty scissors | any sewing supply company | similar to Fiskars 175800-1002 | For cutting TLC plates. A paper cutter with a sharp blade can be used as well. Do not inhale silica dust. |
| Drying oven at 100 °C (mechanical convection) | Thermo Scientific | PR305225M | Quincy Lab, Inc, Chicago, IL (www.quincylab.com); Cascade Technical Sciences, Hillsboro, OR (www.cascadetek.com) |
| TLC chamber | Kimble Chase | 416180-0000 | Alternative sources: Aldrich. Pyrex beakers or preserving jars can be used for small plates (i.e. 5 × 10 cm). Cover with aluminum foil (jar lids may contain material extractable by solvent vapors). |
| 50-µL syringe with flat needle tip | Hamilton | 80965 | For loading amounts of standard or sample exceeding 5-10 µL. Alternative sources are equivalent. |
| micropipets | Drummond | 2-000-001 | For loading small amounts of standards or samples. Alternative sources: VWR. Also, Pasteur pipets can be stretched to a thinner diameter with a butane torch. |
| Filter paper (#1 grade) | Whatman | 1001 917 | Serves as a chamber wick. Other grades of filter paper are OK. This size can be trimmed for the chambers holding 20 × 20 cm plates. |
| Beaker tongs | Fisher Scientific | 15-186 | For putting plates in and out of a large TLC chamber. Alternate sources: VWR |
| Flat-edge forceps | Fisher Scientific | 10-275 | For putting plates in and out of a small chamber. Alternate sources: VWR |
| Small portable UV lamp with 4-Watt or 6-Watt bulbs for short- and long-wave UV light illumination (254 and 365 nm, respectively) | Ultraviolet Products | 95-0271-01 | Alternate sources: Spectronics Corporation (www.spectroline.net) |
| Viewing cabinet for use with hand-held UV lamp | Ultraviolet Products | Chromato-Vue C-10E | UV-active bands are more easily circled if plates can be set in here. Alternate sources: Spectronics Corporation. |
| Photodocumentation system with overhead UV lamp and visible lamp | Kodak | Gel Logic 200 | Alternate sources: Ultraviolet Products (www.uvp.com). See protocol for homemade alternative. |
| Anaerobic Chamber, Type A, Vinyl | Coy | 7150000 | This chamber is appropriate for anaerobic bacteria, like Clostridium sticklandii, as described. However, growth conditions must be tailored to organism used in the assay. A biosafety cabinet and other precautions should be taken if pathogenic organisms are used. Alternate sources: Anaerobe Systems, BioRad, Plas Labs, others |
| Tetrazolium red | Sigma-Aldrich | T8877 | Alternate sources: MP Biomedicals, Santa Cruz Biotechnology, Alfa Aesar |
| Ingredients for HAB media | |||
| Pyridoxamine · 2 HCl | Sigma-Aldrich | P9380 | For this and for all the other reagents in this table, alternative sources are equivalent. |
| Riboflavin | Sigma-Aldrich | R4500 | |
| Thiamine HCl | Sigma-Aldrich | T3902 | |
| Nicotinamide | Sigma-Aldrich | N3376 | |
| Calcium D-Pantothenate | Sigma-Aldrich | C8731 | |
| Lipoic Acid | Sigma-Aldrich | T5625 | |
| p-Aminobenzoic acid | Sigma-Aldrich | A9878 | |
| Folic acid | Sigma-Aldrich | F8798 | |
| Biotin | Sigma-Aldrich | B4639 | |
| Cobalamine | Sigma-Aldrich | C3607 | |
| Pyridoxal HCl | Sigma-Aldrich | P9130 | |
| Pyridoxine | Sigma-Aldrich | P5669 | |
| EDTA | Sigma-Aldrich | E6758 | |
| Iron sulfate · 7 H2O | Sigma-Aldrich | F8263 | |
| Zinc sulfate · 7 H2O | Sigma-Aldrich | Z0251 | |
| Manganese chloride · 4 H2O | Sigma-Aldrich | M8054 | |
| Boric acid | Sigma-Aldrich | B6768 | |
| Cobalt chloride · 6 H2O | Sigma-Aldrich | C8661 | |
| Copper chloride · 2 H2O | Sigma-Aldrich | 459097 | |
| Nickel chloride · 6 H2O | Sigma-Aldrich | 203866 | |
| Sodium molybdate · 2 H2O | Sigma-Aldrich | 331058 | |
| Trypticase (Pancreatic digest of casein) | Thermo Fisher | B11921 | |
| Potassium phosphate monobasic anhydrous | Thermo Fisher | P284 | |
| sodium carbonate · H2O | Thermo Fisher | S636 | |
| Agar | Thermo Fisher | 50841063 | |
| Magnesium sulfate · 6 H2O | Thermo Fisher | 7791-18-6 | |
| Calcium chloride · 2 H2O | Thermo Fisher | BP510 | |
| Cysteine HCl | Thermo Fisher | 19464780 | |
| Potassium phosphate dibasic anhydrous | Thermo Fisher | P290 | |
| Sodium chloride | Thermo Fisher | BP358 |
References
- Stahl, E., Ashworth, M. R. F. . Thin-layer chromatography. , (1969).
- Marston, A. Thin-layer chromatography with biological detection in phytochemistry. J. Chromatogr. A. 1218 (19), 2676-2683 .
- Homans, A. L., Fuchs, A. Direct bioautography on thin-layer chromatograms as a method for detecting fungitoxic substances. J. Chromatogr. 51, 327-329 .
- Lund, B. M., Lyon, G. D. Detection of inhibitors of Erwinia carotovora and E. herbicola on thin-layer chromatograms. J. Chromatogr. 110, 193-196 (1975).
- Betina, V. Bioautography in paper and thin-layer chromatography and its scope in the antibiotic field. J. Chromatogr. A. 78, 41-51 (1973).
- Weltzien, H. C. Ein biologischer Test für fungizide Substanzen auf dem Papierchromatogramm. Naturwissenschaften. 45, 288-289 (1958).
- Khurram, M., Khan, A. M., Hameed, A., Abbas, N., Quayum, A., Inayat, H. Antibacterial activities of Dodonaea viscosa using contact bioautography technique. Molecules. 14 (3), 1332-1341 (2009).
- Khurram, M., et al. Evaluation of anticandidal potential of Quercus baloot Griff. using contact bioautography technique. Afr. J. Pharm. Pharmacol. 5 (12), 1538-1542 (2012).
- Robinson, T. . The Organic Constituents of Higher Plants. , (1963).
- Kagan, I. A., Flythe, M. D. Factors affecting the separation and bioactivity of red clover (Trifolium pratense) extracts assayed against Clostridium sticklandii, a ruminal hyper ammonia-producing bacterium. Nat. Prod. Commun. 7 (12), 1605-1608 (2012).
- Mattila, P., Kumpulainen, J. Determination of free and total phenolic acids in plant-derived foods by HPLC with diode-array detection. J. Agric. Food Chem. 50 (13), 3660-3667 (2002).
- Hamburger, M. O., Cordell, G. A. A direct bioautographic TLC assay for compounds possessing antibacterial activity. J. Nat. Prod. 50 (1), 19-22 (1987).
- Flythe, M., Kagan, I. Antimicrobial effect of red clover (Trifolium pratense) phenolic extract on the ruminal hyper ammonia-producing bacterium, Clostridium sticklandii. Curr. Microbiol. 61, 125-131 .
- Rahalison, L., Hamburger, M., Hostettmann, K., Monod, M., Frenk, E. A bioautographic agar overlay method for the detection of antifungal compounds from higher plants. Phytochem. Anal. 2 (5), 199-203 (1991).
- Chomnawang, M. T., Trinapakul, C., Gritsanapan, W. In vitro antigonococcal activity of Coscinium fenestratum stem extract. J. Ethnopharmacol. 122, 445-449 (2009).
- Stahl, E., Kaldewey, H. Spurenanalyse physiologisch aktiver, einfacher Indolderivate. Hoppe-Seyler’s Z. Physiol. Chem. 323, 182-191 .
- Kagan, I. A., Hammerschmidt, R. Arabidopsis ecotype variability in camalexin production and reaction to infection by Alternaria brassicicola. J. Chem. Ecol. 28 (11), 2121-2140 (2002).
- Kline, R. M., Golab, T. A simple technique in developing thin-layer bioautographs. J. Chromatogr. 18, 409-411 (1965).
- Wedge, D. E., Nagle, D. G. A new 2D-TLC bioautography method for the discovery of novel antifungal agents to control plant pathogens. J. Nat. Prod. 63 (8), 1050-1054 (2000).
- Beck, A. B., Knox, J. R. The acylated isoflavone glycosides from subterranean clover and red clover. Aust. J. Chem. 24 (7), 1509-1518 (1971).
- Kahn, R. A., Bak, S., Svendsen, I., Halkier, B. A., Møller, B. L. Isolation and reconstitution of cytochrome P450ox and in vitro reconstitution of the entire biosynthetic pathway of the cyanogenic glucoside dhurrin from sorghum. Plant Physiol. 115 (4), (1997).
- Peterson, C. A., Edgington, L. V. Quantitative estimation of the fungicide benomyl using a bioautograph technique. J. Agr. Food Chem. 17 (4), 898-899 (1969).

