base HPLC-Assay pour surveiller extracellulaires Nucleotide / nucléosidiques Métabolisme dans les chroniques cellules leucémie lymphocytaire humaines
Summary
The protocol described here represents an easy and reproducible method that employs reverse phase high-performance liquid chromatography (RP-HPLC) to measure purine metabolism on chronic lymphocytic leukemia (CLL) cells cultured under different conditions.
Abstract
Cette méthode décrit une chromatographie sensible, spécifique, fiable et reproductible en phase inverse liquide à haute performance (HPLC-RP) l'essai développé et validé pour la quantification des nucleotides extracellulaires puriques et les nucléosides produites par purifiée leucémie lymphoïde chronique (CLL), les cellules dans différentes conditions de culture . La séparation chromatographique de l'adénosine 5'-monophosphate (AMP), l'adénosine (ADO) et inosine (INO) est effectuée à la température ambiante sur une colonne en phase inverse à base de silice qui est utilisé pour la rétention du composé polaire. Le procédé comprend une phase mobile binaire, qui est constitué d'acétate d'ammonium à 7 mM et de l'acétonitrile à un débit de 1,00 ml / min de débit. Les éluats sont surveillés à l'aide d'un détecteur UV Photodiode Array fixé à 260 nm. Une courbe d'étalonnage est générée pour calculer l'équation analytique pour la quantification de chaque composé de purine. le contrôle du système, l'acquisition de données et l'analyse sont ensuite effectuées. L'application de ce protocole, AMP, INO et ADO éluent à 7, 11 et 11,9 min, respectivement, et le temps total de course pour chaque échantillon est de 20 min. Ce protocole peut être appliqué à différents types de cellules et de lignées cellulaires (à la fois en suspension et adhérents), en utilisant des milieux de culture comme matrice. Les avantages sont la préparation des échantillons faciles et rapides et que l'exigence d'une faible quantité de surnageant pour l'analyse. En outre, l'utilisation d'un milieu exempt de sérum permet de sauter l'étape de précipitation des protéines avec de l'acétonitrile qui influe sur la concentration finale des composés de purine. L'une des limites de la méthode est l'exigence de la colonne d'équilibration exécuter avant chaque exécution d'un seul échantillon, ce qui rend le temps total d'exécution de l'expérience plus longue et la prévention des applications de criblage à haut débit.
Introduction
Adenosine (ADO) est une purine nucléoside avec une molécule d'adénine attachée à un fragment de molécule de sucre ribose par une liaison glycosidique. Lorsqu'ils sont présents dans le milieu extracellulaire, elle protège les cellules contre les dommages excessifs par l'action du système immunitaire. Ce rôle a été mis en évidence en utilisant différents modèles de maladies, telles que la colite 1, 2 diabète, l' asthme 3, la septicémie 4 et 5 lésion ischémique. L' une des principales fonctions d'ADO est l'inhibition des réponses immunitaires dans le microenvironnement de la tumeur, ce qui contribue à la tumeur évasion immunitaire 6. Pour cette raison, les mécanismes impliqués dans la formation ADO et la signalisation sont d' un intérêt thérapeutique considérable 7.
ADO niveaux dans le microenvironnement des tissus sont relativement faibles dans des conditions physiologiques normales, et certainement inférieure au seuil de sensibilité des cellules immunitaires. Cependant, au cours de l'hypoxie, l'ischémie, l'inflammation, l'infection, métaboliquele stress et la transformation tumorale , ils augmentent rapidement 8. Les niveaux d'ADO extracellulaires élevées en réponse à des signaux de tissu perturbant ont une double fonction: signaler une lésion tissulaire de façon autocrine et paracrine et pour générer des réponses tissulaires qui peuvent être généralement considérés comme cytoprotecteur.
Extracellulaires ADO peut être formé par une variété de mécanismes, qui comprennent la libération des compartiments intracellulaires médiés par les transporteurs de nucléosides 9 ou accumulation en raison de la dégradation altérée exploité par l' adénosine désaminase. La voie principale menant à une augmentation des niveaux extracellulaires ADO implique l'action d'une cascade de ectonucléotidases, qui sont associées à la membrane ectoenzymes générant ADO par phosphohydrolysis de nucléotides libérés de cellules mortes ou mourantes. Cette voie passe par l'action séquentielle de CD39 (triphosphate ectonucleoside diphosphohydrolase-1) qui convertit l'adénosine extracellulaire 5'-triphosphate (ATP) ou l' adénosine 5'-diphosphate (ADP) en adénosine 5'-monophosphate (AMP) et de CD73 (5'-nucléotidase) qui transforme l' AMP à 10 ADO.
Extracellulaires ADO provoque ses réactions physiologiques en se liant à quatre transmembranaire ADO récepteurs, à savoir A1, A2A, A2B et A3. Chaque récepteur a des affinités différentes pour ADO et la distribution des tissus spécifiques. Tous les récepteurs ont sept domaines transmembranaires et sont couplés aux protéines G à des protéines de liaison au GTP intracellulaire (protéines G), qui peut induire (protéine Gs) ou à inhiber (Gi protéine) activité de l'adénylate cyclase et, par la suite, la production d'AMPc intracellulaire. Par conséquent, les changements de l' impact cytoplasmique des taux d'AMPc sur l' activité protéine kinase intracellulaire pendant 11 réponses physiologiques. Dans des conditions physiologiques ADO extracellulaire est inférieure à 1 uM, qui peut activer indifféremment A1, A2A et récepteurs A3. Cependant, l'activation du sous-type A2B nécessite considérablement plus élevésLes concentrations du nucleoside, tels que ceux produits dans des conditions physiopathologiques. En variante, OAD extracellulaire peut être dégradée à l'inosine (INO) par l'adénosine désaminase (ADA) et de CD26, une protéine ADA complexant localisant l'ADA sur la surface cellulaire. Une autre possibilité est que ADO est internalisé par la cellule par les transporteurs de nucléosides (ORL) et phosphorylée à AMP par ADO protéine kinase 12,13.
L'objectif de ce protocole est de décrire une méthode d'analyse de la chromatographie en phase liquide à haute performance en phase inverse (RP-HPLC) pour quantifier en un seul passage AMP du substrat et des produits ADO et INO, telle que générée par les lymphocytes humains. Notre expérience a été initialement obtenue en utilisant des cellules de patients chroniques leucémie lymphoïde (CLL), qui sont caractérisés par l'expansion d'une population mature de lymphocytes CD19 + / CD5 + B exprimant constitutivement CD39 14,15. Nous avons montré environ 30%des CLL patients expriment le ectoenzyme CD73 et que ce phénotype est corrélée à un mauvais pronostic 16. Cette sous-population de cellules leucémiques co-exprimant CD39 et CD73 peut activement produire ADO extracellulaire d'ADP et / ou AMP. La pré – incubation de cellules CD73 + leucémiques avec des α, la synthèse d'ADO extracellulaire β-méthylène-ADP (PCAP), un inhibiteur connu de l' activité enzymatique CD73, bloque complètement confirmant que l'enzyme CD73 représente un goulot d'étranglement de cette cascade 16.
les cellules CLL expriment également ADA et l'ADA protéine complexant CD26, qui sont responsables de la conversion de ADO dans INO. En utilisant des inhibiteurs de l'ADA spécifiques, tels que érythro-9- (2-hydroxy-3-nonyl) Je wiadenine (EHNA) et du chlorhydrate désoxycoformycine (FNC), il est possible de bloquer la dégradation ADO extracellulaire dans INO. En outre, le prétraitement avec un inhibiteur de l'ADA, en combinaison avec le dipyridamole, qui bloque les transporteurs de nucléosides, augmente l'accumulation dans la cellule ADOsurnageants.
Nous avons ensuite étendu ce protocole à des cellules dérivées d'autres lignées, y compris les lymphocytes T et les cellules myéloïdes, confirmant la production d'ADO CD73-dépendante. Ces résultats suggèrent que ce protocole HPLC est très polyvalent et qu'il peut être appliqué à différentes lignées cellulaires et à différentes conditions de culture (figure 1).
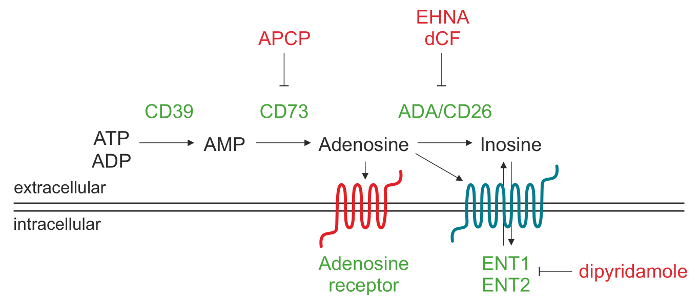
Figure 1. Représentation schématique de la machinerie enzymatique responsable de la production ADO extracellulaire. Adenosine 5'-triphosphate (ATP) et / ou l' adénosine 5'-diphosphate (ADP) peut être dégradé par CD39 à l' adénosine 5'-monophosphate (AMP), qui à son tour, est converti par CD73 dans l'adénosine nucléoside (ADO). Une fois que ADO est produite dans l'espace extracellulaire, elle peut rentrer dans la cellule par les transporteurs de nucléosides (ENT), être converti en l'inosine (INO) oulier à différents types de récepteurs P1 ADO. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Protocol
Representative Results
Discussion
Le protocole décrit ici permet d'évaluer l'activité du CD39 / CD73 machines adénosinergique dans des milieux de culture cellulaire à partir de cellules leucémiques humaines purifiées. Grâce à cette méthode HPLC, nous pouvons suivre et mesurer quantitativement la production enzymatique de ADO (CD73-dépendant) et sa dégradation subséquente à l'INO (CD26 / ADA dépendant). L'utilisation d'inhibiteurs de l'enzyme permet de contrôler le protocole et d'avoir des contrôles internes. …
Disclosures
The authors have nothing to disclose.
Acknowledgements
Ce travail est soutenu par l'Associazione Italiana Ricerca Cancro (IG # 12754).
Materials
| Human blood | |||
| Milli-Q water | Millipore | double deionised water | |
| Ficoll-Paque Plus | GE-Healthcare | 17-1440-03 | |
| purified anti-CD3, -CD14, -CD16 | made in-house | mouse monoclonal | |
| PE-labeled anti-CD19 | Miltenyi Biotec | 120-014-229 | |
| FITC-labeled anti-CD5 | Miltenyi Biotec | 130-096-574 | |
| Dynabeads sheep anti-mouse IgG | Invitrogen | 11031 | |
| Phosphate-buffered saline (PBS) | Amresco | E404-200TABS | tablets |
| bovine serum albumin (BSA) | ID bio | 1000-70 | standard grade |
| isolation buffer | PBS 0.1 % BSA 2 mM EDTA, pH 7.4 | ||
| AIM V serum free medium | GIBCO | 12055-091 | liquid (research grade) |
| adenosine 5’-diphosphate (ADP) | Sigma-Aldrich | A2754 | |
| adenosine 5’-monosphate (AMP) | Sigma-Aldrich | A1752 | |
| adenosine (ADO) | Sigma-Aldrich | A9251 | |
| inosine (INO) | Sigma-Aldrich | I4125 | |
| α,β-methylene-ADP (APCP) | Sigma-Aldrich | M8386 | CD73 inhibitor |
| EHNA hydrochloride | Sigma-Aldrich | E114 | adenosine deaminase inhibitor |
| Deoxycoformycin (dCF) | Tocris | 2033 | adenosine deaminase inhibitor |
| Dimethyl sulfoxide (DMSO) | Sigma-Aldrich | D2650 | |
| Dipyridamole | Sigma-Aldrich | D9766 | nucleoside transporter inhibitor |
| acetonitrile (CHROMASOLV Plus) | Sigma-Aldrich | 34998 | HPLC-grade |
| ammonium acetate | Sigma-Aldrich | 9688 | 7 mM, pH 3.0 |
| hydrochloric acid | Sigma-Aldrich | 30721-1L | min. 37 % |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Bürker cell counter | VWR | 631-0920 | hemocytometer |
| DynaMag-15 Magnet | Invitrogen | 12301D | Dynal magnetic bead separator |
| microcentrifuge safe-lock tubes | Eppendorf | 030-120-0086 | 1.5 ml |
| PET centrifuge tubes | Corning | 430053/430304 | 15 – 50 ml |
| Minisart RC4 syringe filters | Sartorius Stedim Biotech | 17821 | membrane 0.2 µm |
| short thread vials | VWR | 548-0029 | 1.5 ml/glass |
| micro-inserts | VWR | 548-0006 | 0.1 ml/glass |
| screw caps | VWR | 548-0085 | 9 mm/PP blue |
| Atlantis dC18 Column | Waters | 186001344 | 5 µm, 4.6 x 150 mm |
| Atlantis dC18 Guard Column | Waters | 186001323 | 5 µm, 4.6 x 20 mm |
| Waters Alliance 2965 Separations Module | Waters | HPLC separation module | |
| Waters 2998 Photodiode Array (PDA) Detector | Waters | UV detector | |
| Waters Empower2 software | Waters |
References
- Naganuma, M., Wiznerowicz, E. B., Lappas, C. M., Linden, J., Worthington, M. T., Ernst, P. B. Cutting edge: Critical role for A2A adenosine receptors in the T cell-mediated regulation of colitis. J Immunology. 177 (5), 2765-2769 (2006).
- Nemeth, Z. H., et al. Adenosine receptor activation ameliorates type 1 diabetes. FASEB J. 21 (10), 2379-2388 (2007).
- Fan, M., Jamal Mustafa, S. Role of adenosine in airway inflammation in an allergic mouse model of asthma. Int Immunopharmacol. 6 (1), 36-45 (2006).
- Csoka, B., et al. A2B adenosine receptors protect against sepsis-induced mortality by dampening excessive inflammation. J Immunol. 185 (1), 542-550 (2010).
- Peart, J. N., Headrick, J. P. Adenosinergic cardioprotection: multiple receptors, multiple pathways. Pharmacol Ther. 114 (2), 208-221 (2007).
- Ohta, A., et al. A2A adenosine receptor protects tumors from antitumor T cells. Proc Natl Acad Sci U S A. 103 (35), 13132-13137 (2006).
- Hasko, G., Linden, J., Cronstein, B., Pacher, P. Adenosine receptors: therapeutic aspects for inflammatory and immune diseases. Nat Rev Drug Discov. 7 (9), 759-770 (2008).
- Cronstein, B. N. Adenosine, an endogenous anti-inflammatory agent. J Appl Physiol (1985). 76 (1), 5-13 (1994).
- Molina-Arcas, M., Casado, F. J., Pastor-Anglada, M. Nucleoside transporter proteins. Curr Vasc Pharmacol. 7 (4), 426-434 (2009).
- Deaglio, S., et al. Adenosine generation catalyzed by CD39 and CD73 expressed on regulatory T cells mediates immune suppression. J Exp Med. 204 (6), 1257-1265 (2007).
- Linden, J. Regulation of leukocyte function by adenosine receptors. Adv Pharmacol. 61, 95-114 (2011).
- Antonioli, L., Blandizzi, C., Pacher, P., Hasko, G. Immunity, inflammation and cancer: a leading role for adenosine. Nat Rev Cancer. 13 (12), 842-857 (2013).
- Antonioli, L., Csoka, B., Fornai, M., et al. Adenosine and inflammation: what’s new on the horizon. Drug Discov Today. 19 (8), 1051-1068 (1051).
- Chiorazzi, N., Rai, K. R., Ferrarini, M. Chronic lymphocytic leukemia. N Engl J Med. 352 (8), 804-815 (2005).
- Abousamra, N. K., Salah El-Din, M., Hamza Elzahaf, E., Esmael, M. E. Ectonucleoside triphosphate diphosphohydrolase-1 (E-NTPDase1/CD39) as a new prognostic marker in chronic lymphocytic leukemia. Leuk Lymphoma. 56 (1), 113-119 (2015).
- Serra, S., et al. CD73-generated extracellular adenosine in chronic lymphocytic leukemia creates local conditions counteracting drug-induced cell death. Blood. 118 (23), 6141-6152 (2011).
- Chen, L. S., Keating, M. J., Gandhi, V. Blood collection methods affect cellular protein integrity: implications for clinical trial biomarkers and ZAP-70 inn CLL. Blood. 124 (7), 1192-1195 (2014).
- Kalina, T., et al. EuroFlow standardization of flow cytometer instrument settings and immunophenotyping protocols. Leukemia. 26 (9), 1986-2010 (2012).
- Deaglio, S., et al. CD38 and ZAP-70 are functionally linked and mark CLL cells with high migratory potential. Blood. 110 (12), 4012-4021 (2007).
- Sachsenmeier, K. F., et al. Development of a novel ectonucleotidase assay suitable for high-throughput screening. J Biomol Screen. 17 (7), 993-998 (2012).

