Sublimatie van DAN Matrix voor de detectie en Visualisatie van gangliosiden in Rat Brain Tissue voor MALDI Imaging Mass Spectrometry
Summary
A protocol for the sublimation of DAN matrix onto rat brain tissue for the detection of gangliosides using MALDI Imaging Mass Spectrometry is presented.
Abstract
Steekproef voorbereiding is essentieel voor een optimale detectie en visualisatie van analyten in matrix-geassisteerde laserdesorptie / ionisatie (MALDI) Imaging Mass Spectrometry (IMS) experimenten. Het bepalen van de juiste protocol te volgen door het monster bereidingswerkwijze kan moeilijk zijn omdat elke stap moet worden geoptimaliseerd om te voldoen aan de unieke eigenschappen van de analyten. Dit proces omvat niet alleen het vinden van een compatibele matrix die kunnen desorberen en efficiënt ioniseren van de moleculen van belang, maar ook het selecteren van de geschikte matrix depositietechniek. Bijvoorbeeld, een natte matrixafzetting techniek, die inhoudt het oplossen van een matrix oplosmiddel superieur voor desorptie van de meeste eiwitten en peptiden, terwijl droge matrixafzetting technieken zijn bijzonder effectief voor ionisatie van lipiden. Sublimatie is gerapporteerd als een zeer efficiënte droge matrixafzetting voor de detectie van lipiden in weefsel door MALDI IMS vanwege de homogeneity van matrix kristallen afzetting en minimale analyseren delokalisatie in vergelijking met veel natte depositie methoden 1, 2. Algemeen gaat het om een monster en gepoederde matrix in een vacuüm afgedichte kamer met gedrukt tegen een koud oppervlak monsters. De inrichting wordt vervolgens neergelaten in een verwarmd bad (zand of olie), waardoor sublimatie poedervormig matrix op het gekoelde oppervlak weefselmonster. Hier beschrijven we een sublimatie protocol via 1,5-diaminonaftaleen (DAN) matrix voor de detectie en visualisatie van gangliosiden in de rattenhersenen middels MALDI IMS.
Introduction
Matrix-geassisteerde laserdesorptie / ionisatie (MALDI) Imaging Mass Spectrometry (IMS) is steeds een zeer gewilde techniek voor visualisatie van de ruimtelijke verdeling van lipiden, peptiden en eiwitten over intact monster oppervlakken. MALDI IMS werd voorheen een analytische techniek voor pre-gezuiverde analyten, maar de laatste jaren, is de aandacht in vele disciplines vanwege de mogelijkheid om de nauwkeurigheid van massaspectrometrie in combinatie met hoge resolutie visuele / anatomische referentiepunten zonder behoefte aan externe labeling. De wetenschappelijke onderzoekerswereld gebruik van deze techniek blijft groeien, is er meer behoefte aan gestandaardiseerde, gemakkelijk te volgen protocollen om te helpen bij de ontwikkeling en optimalisatie van IMS experimenten. Gangliosiden, een groep van membraanlipiden veel voorkomt in het centrale zenuwstelsel, zijn geschikt voor MALDI IMS experimenten hun locatie, ingebed in het membraan zorgt ervoor species onmogelijk op te sporen met behulp van conventionele Immuno-labeling. Bovendien hebben we aangetoond, middels MALDI IMS, dat deze lipiden, die functioneren als modulatoren van celsignalering, onder andere, hebben unieke anatomische verspreidingspatroon in de gezonde knaagdierhersenen die gewijzigd na hersenletsel 3, 4, 5. Gangliosiden worden bij een hogere massabereik vergelijking met de meeste soorten lipiden, en dus best overeenstemt met de MALDI imaging platform.
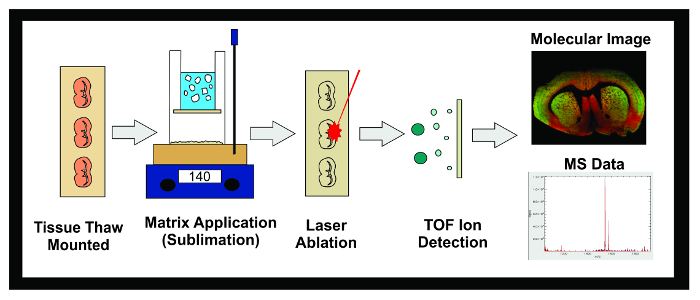
Figuur 1: Workflow van MALDI IMS Experiment. Diagram van de algemene workflow van een MALDI IMS experiment met behulp van sublimatie. Weefsel ingevroren bij -80 ° C is verdeeld in een cryostaat en 10 urn secties zijn ontdooien gemonteerd op geleidende ITO slides. Het objectglaasje wordt vervolgens in een exsiccator tot sublimatie. Slides worden in de sublimatie-inrichting en een gelijkmatige laag matrix wordt toegepast op het weefsel monsteroppervlak. De monsters worden gedurende de nacht ingevroren in een -20 ° C vriezer daarna in een exsiccator geplaatst gedurende 10 min. Zodra normen zijn toegepast, worden de monsters ingebracht in de MALDI instrument waarbij een laser is gericht aan de overkant van het weefsel veroorzaakt gedesorbeerde moleculen in de matrix te ioniseren. De ionen reizen naar beneden een vlucht buis en apart op basis van hun massa (time-of-flight / TOF) totdat ze de detector bereiken. De gegevens over de ionische overvloed van analyten binnen een vooraf bepaalde massa-tot-lading (m / z) bereik wordt als zowel een molecuulgewicht beeld en massaspectrum. Deze gegevens kunnen worden gebruikt om zowel visualiseren en kwantificeren van de ionische overvloed van de analyt van belang in het afgebeelde weefsel. Klik hier om een grotere versie van deze figuur te bekijken.
monstervoorbereidingvoor MALDI IMS is zeer variabel als elke stap van het proces moet worden aangepast aan de analyten. Het kenmerk van MALDI-gebaseerde experimenten is het gebruik van een matrix bekleding op het monsteroppervlak vóór de analyse afgezet. Naast de rol absorberen en overdragen stralingsenergie van de laser gedurende het ablatieproces, de matrix dient ook om diverse analyten te isoleren van het monster, waardoor de analyse van de van belang zijnde verbindingen 6, 7 vergemakkelijkt. Homogene toepassing van de matrix op het monsteroppervlak is de meest cruciale stap in het monster bereidingsproces. Onjuiste matrixafzetting kan leiden tot grote heterogene matrix kristalformaties en de ontwikkeling van artefacten, lage ion-signaal en slechte reproduceerbaarheid 7.
Door de affiniteit van bepaalde matrices specifieke analyten te isoleren, het type matrix gekozen voor een experiment kanaanzienlijke verandering van de uitkomst. De matrices voor beeldvorming van eiwitten en peptiden dikwijls verschillen van die welke voor de beeldvorming lipiden en het proces wordt verder bemoeilijkt door de behoefte aan aanvullende procedures zoals wassen en rehydratatie stappen om signalen uit weefsel succesvol detecteren. Hoewel wasstappen aanwezig voor de verhoging van lipide signalen 8, zij geen voorwaarde voor het detecteren van de meeste soorten lipiden. Bij het selecteren van een matrijs voor een lipide imagingexperiment, is het belangrijk om de polariteit van het lipide van belang, omdat dit gegeven moment het bereik van geschikte matrices beperken. Bijvoorbeeld gangliosiden bevatten siaalzuurresten waardoor ze een algemene negatieve polariteit geven. Er zijn een aantal matrices die effectief kan desorberen en ioniseren gangliosiden uit weefsel; evenwel moeten factoren als matrix afgeleide pieken in het spectrum en de stabiliteit van de matrix onder vacuüm behandeling genomen. 1,5-diaminonapthalene (DAN) matrix voldoende stabiel onder vacuüm instrument voor de meeste beeldvormende toepassingen en heeft een hoge mate van gevoeligheid voor lipide desorptie aangetoond en kan worden gebruikt voor de analyse van lipiden in zowel positieve als negatieve ion modus 2. DAN matrix, in vergelijking met andere negatieve lipide affiniteitsmatrices zoals dihydroxybenzoëzuur (DHB), 9-aminoacridine (9-AA) en 5-chloor-2-mercaptobenzothiazol (CMBT), kon gangliosiden uit rattenhersenen meest efficiënt desorberen weefsel in negatieve ionen-modus (manuscript in voorbereiding).
Het selecteren van de juiste methode van matrix afzetting is van even groot belang voor de keuze van de matrix zelf. Natte matrixafzetting methoden waarbij de vaste matrix wordt opgelost in een organisch oplosmiddel, en afgezet door pneumatische of geautomatiseerde sproeiers of spotters, zijn bijzonder effectief voor de desorptie van eiwitten en peptiden als de vloeistof doordringt het monster mogelijk te maken extractie van verbindingen en co-kristallisatie met de matrix. Hoewel deze technieken ook kunnen worden gebruikt voor lipide toepassingen analyt delocalisatie en onregelmatige matrix kristalformaties gemeenschappelijk gebeurtenissen vanwege de hoge dichtheid en oplosbaarheid van lipiden in oplosmiddelen, met name in weefsel 2, 9. Omdat lipiden gemakkelijk geïoniseerd uit weefsel, droge matrix depositietechnieken, zoals sublimatie, bieden een eenvoudige, kosteneffectief alternatief voor spuitmachines te omzeilen vele nadeel van deze technieken. Het succes van sublimatie in MALDI IMS experimenten wordt toegeschreven aan functies zoals microkristallijne matrix morfologie met een oppervlakte van matrix-bindende analyt verhoogt, verhoogde zuiverheid matrix en homogeen matrixafzetting leidt tot verhoogde reproduceerbaarheid in vergelijking met natte matrix technieken 1, 10.
sublimatie involves het verwarmen van een poedervormig matrix onder vacuüm onmiddellijk onder een gekoelde monster oppervlak resulteert in een vaste stof naar gas-fase-overgang van de gepoederde matrix gevolgd door afzetting op het weefselmonster oppervlak. Tijdens sublimatie kan matrixafzetting worden geregeld door factoren zoals tijd, temperatuur en druk zeer reproduceerbare resultaten opleveren. Eén sublimatie experiment kan variëren van 5 tot 20 minuten afhankelijk van het type matrix gekozen, die kan worden hergebruikt meerdere malen voor verwijdering. De inrichting kan commercieel worden gekocht bij een fractie van de prijs van automatische sproeiers en gemakkelijk uit elkaar gehaald voor reiniging en onderhoud. De lage kosten en relatieve eenvoud van deze matrix depositie techniek maakt het ideaal voor onderzoekers beginnen of uit te breiden op lipide imaging toepassingen in MALDI IMS. Hoewel de informatie detaillering protocollen voor sublimatie van weefsels voor IMS zijn gemeld 11, enkele gestandaardiseerde protocollen bestaan which focus op de basiswerkstroom betrokken bij het uitvoeren van een experiment voor het afbeelden sublimatie hoogmis lipiden in de negatieve ion modus, waardoor het moeilijk om de techniek te vestigen zonder uitgebreide trial and error. Het volgende is een experimentele protocol als doel om die kloof voor de sublimatie van DAN matrix op hersenen van de rat secties voor hoge resolutie beeldvorming en detectie van gangliosiden vullen.
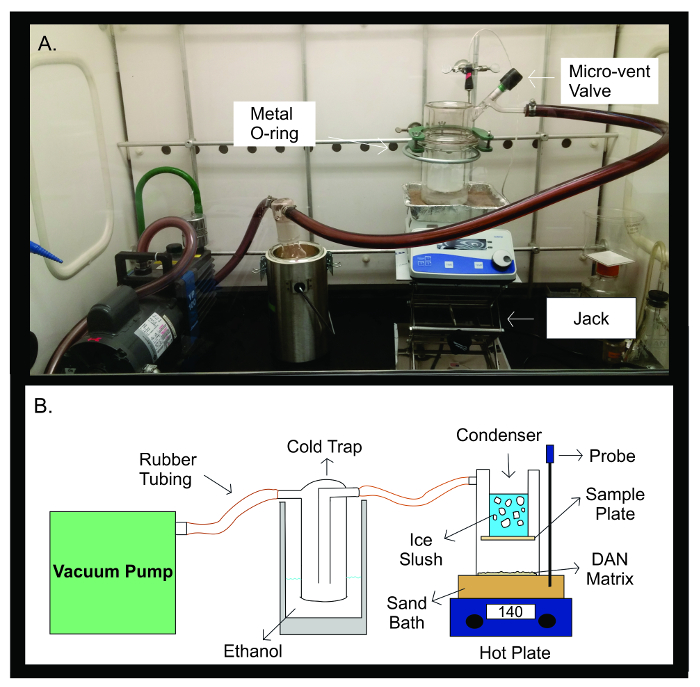
Figuur 2: de sublimatie Apparatuur. Foto (A) en schema (B) van de sublimatie-inrichting. De vacuümpomp is verbonden met rubberen slang aan een koude val gevuld met 300 ml ethanol. De koude val wordt dan verbonden met rubberen slang aan op de sublimatie apparaat. De inrichting bestaat uit twee afzonderlijke stukken glaswerk die aan elkaar afgedicht met een metalen U-joint. De bovenste helft van het sublimatorbevat de condensator die is gevuld met ijs slush. De monsterplaat wordt geplakt op de bodem van de condensor, in het afgesloten glazen inrichting. De onderste helft van de sublimatie apparaat bevat de DAN matrix, verspreid gelijkmatig tegenover het monster plaat. Tijdens sublimatie, wordt het glaswerk geplaatst op een zandbad verwarmd tot 140 ° C door een hete plaat eronder. De temperatuursensor helpt om een stabiele temperatuur in de sublimatie experiment door middel van feedback van de zand badtemperatuur vergeleken met de ingestelde temperatuur voor het experiment. Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
Dit werk Gegevens een gestandaardiseerd protocol matrix sublimatie op weefsel voor het detecteren van negatief geladen lipiden, zoals gangliosiden, in MALDI IMS experimenten. Monstervoorbereiding voor MALDI IMS is zeer variabel en worden aangepast aan de unieke eigenschappen van het analyt te passen. De toepassing van de matrix op weefselmonster oppervlak een cruciaal aspect van de monstervoorbereiding proces met betrekking tot de kwaliteit van de resultaten in IMS. Bijzondere aandacht dient te worden genomen bij het se…
Disclosures
The authors have nothing to disclose.
Acknowledgements
We would like to acknowledge the technical assistance of Kristina Jurcic in the University of Western Ontario MALDI MS facility, as well as the National Sciences and Engineering Council (NSERC) for funding this work. The authors would also like to acknowledge the Caprioli group (Vanderbilt University, TN) and Chaurand group (Université de Montreal, QC) for their advice in optimizing the sublimation technique presented in this manuscript.
Materials
| Sublimator | Chemglass Life Sciences | CG3038-01 | |
| 1,5- Diaminonapthalene (DAN) matrix | Sigma-Aldrich | D21200 | 100 G |
| Cryostat | Thermo-Fisher Scientific | CryoStar NX50 | |
| Hot plate with temperature feedback | Thermo-Fisher Scientific | HP88857290 | Isotemp ADVD 7×7 HP 100-120v |
| Stainless Steel Jack | Thermo-Fisher Scientific | 2216479 | 10×10 |
| Cold Trap | Custom built on site | ||
| Vacuum Pump | Franklin Electric | 1102180403 | Savant VP100 Two Stage |
| Indium-tin-oxide (ITO) Slides | Hudson Surface Technology | PSI 1111000 | type II, 1.1mm/25 each |
| MALDI TOF/TOF 5800 Instrument | AB Sciex | ||
| Desiccator | Sigma-Aldrich | D2797 | tabletop desiccator |
References
- Hankin, J. A., Barkley, R. M., Murphy, R. C. Sublimation as a method of matrix application for mass spectrometric imaging. J. Am. Soc. Mass Spectrom. 18, 1646-1652 (2007).
- Thomas, A., Charbonneau, J. L., Fournaise, E., Chaurand, P. Sublimation of new matrix candidates for high spatial resolution imaging mass spectrometry of lipids: enhanced information in both positive and negative polarities after 1,5-diaminonapthalene deposition. Anal. Chem. 84, 2048-2054 (2012).
- Caughlin, S., et al. Increased Expression of Simple Ganglioside Species GM2 and GM3 Detected by MALDI Imaging Mass Spectrometry in a Combined Rat Model of Aβ Toxicity and Stroke. PLoS ONE. 10, 0130364 (2015).
- Weishaupt, N., Caughlin, S., Yeung, K., Whitehead, S. Differential Anatomical Expression of Ganglioside GM1 Species Containing d18:1 or d20:1 Sphingosine Detected by MALDI Imaging Mass Spectrometry in Mature Rat Brain. Front Neuroanatomy. 9 (155), (2015).
- Whitehead, S., et al. Imaging Mass Spectrometry Detection of Gangliosides Species in the Mouse Brain following Transient Focal Cerebral Ischemia and Long-Term Recovery. PLoS ONE. 6 (6), 20808 (2011).
- Fuchs, B., Süß, R., Schiller, J. An update of MALDI-TOF mass spectrometry in lipid research. Progress in Lipid Research. 49, 450-475 (2010).
- Barceló-Coblijn, G., Fernández, J. A. Mass spectrometry coupled to imaging techniques: the better the view the greater the challenge. Front Physiol. 6 (3), 1-5 (2015).
- Angel, P. M., Spraggins, J. M., Baldwin, H. S., Caprioli, R. Enhanced sensitivity for high spatial resolution lipid analysis by negative ion mode matrix assisted laser desorption ionization imaging mass spectrometry. Anal. Chem. 84, 1557-1564 (2012).
- Murphy, R. C., Hankin, J. A., Barkley, R. M., Zemski Berry, K. A. MALDI imaging of lipids after matrix sublimation/deposition. Biochim. Biophys. Acta. 1811, 970-975 (2011).
- Jaskolla, T. W., Karas, M., Roth, U., Steinert, K. Comparison between vacuum sublimed matrices and conventional dried droplet preparation in MALDI-TOF mass spectrometry. J. Am. Soc. Mass Spectrom. 20, 1104-1115 (2009).
- O’Rourke, M. B., Raymond, B. B., Djordjevic, S. P., Padula, M. P. A versatile cost-effective method for the analysis of fresh frozen tissue sections via matrix-assisted laser desorption/ionisation imaging mass spectrometry. Rapid Commun. Mass Spectrom. 29, 637-644 (2015).
- Patterson, N. H., Thomas, A., Chaurand, P. Monitoring time-dependent degradation of phospholipids in sectioned tissues by MALDI imaging mass spectrometry. J Mass Spectrom. 49, 622-627 (2014).
- Cheng, H., Sun, G., Yang, K., Gross, R. W., Han, X. Selective desorption/ionization of sulfatides by MALDI-MS facilitated using 9-aminoacridine as matrix. J. Lipid Res. 51, 1599-1609 (2010).
- Puolitaival, S. M., Burnum, K. E., Cornett, D. S., Caprioli, R. M. Solvent-free matrix dry-coating for MALDI imaging of phospholipids. J. Am. Soc. Mass Spectrom. 19, 882-886 (2008).
- Chaurand, P., Cornett, D., Angel, P., Caprioli, R. From Whole-body Sections Down to Cellular Level, Multiscale Imaging of Phospholipids by MALDI Mass Spectrometry. Mol Cell Proteomics. 10, (2011).
- Grove, K. J., Frappier, S. L., Caprioli, R. M. Matrix pre-coated MALDI MS targets for small molecule imaging in tissues. J. Am. Soc. Mass Spectrom. 22, 192-195 (2011).
- Yang, J., Caprioli, R. M. Matrix precoated targets for direct lipid analysis and imaging of tissue. Anal. Chem. 85, 2907-2912 (2013).
- Gemperline, E., Rawson, S., Li, L. Optimization and comparison of multiple MALDI matrix application methods for small molecule mass spectrometric imaging. Anal. Chem. 86, 10030-10035 (2014).

