ライブの一次繊毛で高速超解像顕微鏡の応用
Summary
最近我々 は様々 なタンパク質の一次線毛による生細胞内透過輸送ルートの三次元 (3 D) 空間の場所を割り当てられます。ここで実験のセットアップ、生体試料のプロセスおよびアプローチを新しくイメージング 3 D 超解像蛍光のデータ解析の適用と課題については、一次繊毛を住んでいます。
Abstract
一次繊毛は、多くの真核細胞の表面に微小管の突出を細胞運動、シグナル伝達タンパク質のユニークな補体の関数を批判的に含みます。繊毛は自分のタンパク質を合成することができないので、ほぼ 200 のユニークな毛様体タンパク質は細胞質と一次繊毛の間取り引きされる必要があります。しかし、それはまだ既存の現在の制限のためライブの一次繊毛のこれらの蛋白質の輸送経路の三次元 (3 D) 場所をマップする技術的な課題のテクニック。挑戦を征服するには、最近開発して、輸送経路のための 3 D の空間的位置を決定するため、シングル ポイント エッジ励起サブ回折 (速度) 顕微鏡と呼ばれる高速仮想 3 D 超解像顕微鏡を採用ゾル性細胞質の両方の生きているセルの一次繊毛膜タンパク質。この記事で、顕微鏡、毛様体タンパク質の蛍光蛋白質標識、ライブの繊毛に個々 の蛋白質の実時間単一分子追跡および達成を発現する細胞の準備の詳細設定がデモンストレーションします。3 D 空間の確率密度に毛様体タンパク質の輸送ルートのマップします。
Introduction
以来、1873 年にエルンスト ・ アッベが述べたように、従来の光学顕微鏡の分解能は、客観的1,2から光の回折による限られた約 200 nm と考えられています。現在、超解像光学顕微鏡技術は、この制限を破るし、サブ回折 (< 200 nm) 解像度とダイナミックな画像を取得できます。技術は一般に 2 つの広範なカテゴリに分類: サンプル3で fluorophores の非線形光学応答のため、サブの回折照明ボリュームを生成、排出枯渇 (STED) 顕微鏡ベース アプローチを刺激センサーの光学顕微鏡観察 (パーム) と確率論的光再建顕微鏡 (嵐)-ベースの fluorophores の重心をローカライズし、この重心を再構成する数学的な関数を利用した超解像技術超解像画像4,5を形成。現在、比較的単純な光のセットアップのためパームと嵐が広く採用のみ生物学的製剤の長いビデオの各フレームでの同時の小さなサブセットをアクティブにします。これによりより正確な局在化のため 2次元ガウシアンフィッティング蛍光スポットの点拡がり関数 (PSF) と呼ばれる、ビデオの各フレームで蛍光標識したタンパク質の。蛍光標識した分子の 2次元位置は、生物学的準備1,2の超解像画像を生成する単一のイメージング平面上、重ね合わせることが。これらの分子の局在化しながら超解像顕微鏡方法確かに革命をどのように生体試料のイメージングを行った、まだ克服すべき課題があります。たとえば、嵐とパーム生体試料の固定後最高の分解能を達成できしたがって電子顕微鏡のような制限である蛍光標識したタンパク質の静的な表現を提示します。さらに、タンパク質のダイナミクスを捉えることである非常に長いフレーム レートで、生きた細胞の蛍光標識蛋白質ごとの高空間分解能を達成するためにサンプルをイメージする必要があります。したがって、これらの主要な技術的なハードルを克服するために必要です。
生細胞における高速移動蛋白質または Rna の検出に適しています高い時空間分解能を得るためには、私たち研究室 (図 1)6,7,の超解像顕微鏡を開発しました。8. 顕微鏡のいくつかの主要な技術の進歩は正常に小分子の核細胞質輸送を追跡する私たちを有効にしていた、ネイティブ核を介してウイルス mRNA、タンパク質孔複合体 (Npc)6,7,8. Npc など一次繊毛の生細胞におけるサブミクロン回転対称形構造の高分子の高速移動を追跡する簡単に、顕微鏡の次の機能が使用されます: (1) 傾斜または垂直照明 PSF により焦点面 (図 1); 小さな回折限界ボリューム内単一分子の励起(2) 傾斜の PSF は大きくアウト フォーカス蛍光を回避でき、信号対雑音比を向上させる。100-500 kW の光学濃度 (3)/cm2照明 PSF の高速検出速度 (> 500 Hz) で単一 fluorophores が付いてから収集する光子の数千をことができます。(4) 高速検出速度も大幅分子拡散は 1 つの主要な要因の生細胞における蛍光分子の移動の空間軌道を決定する単一分子空間定位エラー (< 10 nm) が減少します。分子の移動の単一分子の局在化の欠陥を引き起こします。(5) 老舗 2D 3d 変換アルゴリズムは、NPC または一次繊毛中分子の輸送ルートの 3 D 空間確率密度マップを提供するために私たちを有効にします。それはデカルトと円筒の調整システムの間の変換処理を使用して、3 D 空間の確率密度 3 D ではなくマップ単一分子追跡 (図 2) を生成することは注目に値する。以前は、電子顕微鏡データでは NPC9,10と一次繊毛11両方回転対称形の構造があることを明らかにしました。原則として、ランダムに拡散分子 NPC または一次繊毛を移動する必要があります回転対称形の分布。図 2に示すように、ランダムにシリンダーの中の分子の拡散の数が多いがおよそ均一の結果さらに NPC の回転対称形分布と断面生成空間2 つの隣接リング (図 2E) 間の非常に小さい各サブ領域内で配布します。この均一な分布を導く円筒における θ 次元空間分布は一定であります。その後、3 D 座標 (R, X, θ) は 2 D 座標 (R, X, 定数) であると簡略化できます。実際には、デカルトと円筒形のシステムの間の変換プロセスは (X, Y) は 2 D から 2 D (R, X, 定数) です。一定の θ図 2電子の空間密度pを指し、 Aの方程式を使用して計算されます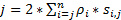 。
。
最終的には、単一分子追跡研究生物学の広範なアプリケーションには、したがって、特定の生物学的ニッチ12,13,14を入力するテクニックの茄多が開発することは当然です。顕微鏡の場合と同様であります。以前は、3 D 変換アルゴリズムと相まって、この手法が通過する Npc、diffraction サイズと回転対称の生物学的構造6による分子の 3 D 輸送ルートを解決する開発されました。本稿で一次繊毛がエクセレント モデル細胞小器官と同様に表示されます。一次繊毛は、プロジェクトのほとんどの哺乳類細胞15,16,17の表面からアンテナのように、円筒の器官 (~ 125 nm radius) です。外部信号を受信し、成長と代謝15,16に通常関連付けられている細胞内の応答を送信に責任があります。したがって、構造タンパク質のフラックス、膜貫通受容体と細胞内メッセンジャーの伝送のリサイクル一次繊毛の重要な責任です。一次繊毛、細胞体の間の連接は転移の地帯または11,18,19を発生する必要がありますこのすべてのタンパク質輸送、TZ と呼ばれる重要な選択性バリア 20。TZ のゲーティング機能に加えて少なくとも 2 つの輸送プロセス, 鞭毛内輸送と受動拡散この地域16,21,蛋白質の動きを担当すると考えられています。22. ヒトの健康の観点から主な毛損失と下流シグナルの後の規制緩和は多くの癌の特性。さらに、バルデ-ビードル症候群や多嚢胞性腎疾患など、多くの遺伝病は、欠陥のある蛋白質輸送23に関連付けられます。サブの回折限界サイズと TZ のたんぱく質の選択的輸送の複雑なプロセスの両方一次繊毛この技術のための主なターゲットを作る。この方法で毛様体膜貫通タンパク質、ソマトスタチン受容体 3 (SSTR3) の追跡を紹介24、Alexa Fluor 647 と IFT、IFT2025、溶かされた GFP の分子とラベルのコンポーネントで外部ラベルします。
Protocol
Representative Results
Discussion
このプロトコルでは、顕微鏡の一次繊毛、効率的なタンパク質輸送に大きく依存して細胞シグナリング オルガネラへの応用について説明します。顕微鏡に、TZ の中心一点照明を通過するときは、蛍光標識した分子 (< 10 nm) 場所高解像度を提供できます。以前それは NPC6,7,8を通じて人身売買蛋白質を調査に適用されています…
Disclosures
The authors have nothing to disclose.
Acknowledgements
いくつかのプラスミドの提供ありがとう博士クリステン四重奏団、他 (アナーバー、ミシガン州大学)、博士グレゴリー Pazour (マサチューセッツ大学医学部)。プロジェクトは、国立衛生研究所 (NIH の GM097037、GM116204、大学院に GM122552) からの助成金によって支えられました。
Materials
| 25 cm2 tissue culture dish | Corning | VV-01936-00 | |
| Penicillin/streptomycin | ThermoFisher | 15140122 | |
| Fetal bovine serum | ThermoFisher | 10438018 | |
| DMEM | ThermoFisher | 10566-016 | |
| OPTIMEM | ThermoFisher | 31985062 | |
| Trypsin | ThermoFisher | 25300054 | |
| Phosphate buffered saline | Sigma-Aldrich | P3813-1PAK | |
| Transit LT1 | Mirus | MIR 2300 | |
| 35 mm glass bottom dish | MatTek | P35GCOL-0-14-C | |
| AlexaFluor 647-conjugated streptavidin | ThermoFisher | S21374 | |
| Biotin | Sigma-Aldrich | B4501-100MG | |
| 633 nm He-Ne laser | Melles Griot | 25-LHP-928-249 | |
| 561 nm solid state laser | Coherent | OBIS 561-50 LS | |
| 488 nm solid state laser | Coherent | 1185053 | |
| Inverted fluorescence microscope | Olympus | IX81 | |
| 1.4-NA 100× oil-immersion apochromatic objective | Olympus | UPLSAPO 100× | |
| On-chip multiplication gain charge-coupled-device camera | Roper Scientific | Cascade 128+ | |
| Dichroic filter | Semrock | Di01- R405/488/561/635-25×36 | |
| Emission filter | Semrock | NF01-405/488/561/635-25X5.0 | |
| Slidebook 6.0 | Intelligent Imaging Innovations | digital microscopy software |
References
- Huang, B., Bates, M., Zhuang, X. Super-resolution fluorescence microscopy. Annu Rev Biochem. 78, 993-1016 (2009).
- Leung, B. O., Chou, K. C. Review of super-resolution fluorescence microscopy for biology. Appl Spectrosc. 65, 967-980 (2011).
- Willig, K. I., Rizzoli, S. O., Westphal, V., Jahn, R., Hell, S. W. STED microscopy reveals that synaptotagmin remains clustered after synaptic vesicle exocytosis. Nature. 440, 935-939 (2006).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313, 1642-1645 (2006).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM). Nat Meth. 3, 793-796 (2006).
- Ma, J., Yang, W. Three-dimensional distribution of transient interactions in the nuclear pore complex obtained from single-molecule snapshots. Proc Natl Acad Sci USA. 107, 7305-7310 (2010).
- Ma, J., Goryaynov, A., Sarma, A., Yang, W. Self-regulated viscous channel in the nuclear pore complex. Proc Natl Acad Sci USA. 109, 7326-7331 (2012).
- Ma, J., et al. High-resolution three-dimensional mapping of mRNA export through the nuclear pore. Nat Comm. 4, (2013).
- Akey, C. W., Radermacher, M. Architecture of the Xenopus nuclear pore complex revealed by three-dimensional cryo-electron microscopy. J Cell Biol. 122, 1-19 (1993).
- Akey, C. W. Interactions and structure of the nuclear pore complex revealed by cryo-electron microscopy. J Cell Biol. 109, 955-970 (1989).
- Czarnecki, P. G., Shah, J. V. The ciliary transition zone: from morphology and molecules to medicine. Trends Cell Biol. 22, 201-210 (2012).
- Elf, J., Li, G. -. W., Xie, X. S. Probing transcription factor dynamics at the single-molecule level in a living cell. Science. 316, 1191-1194 (2007).
- Anzalone, A., Annibale, P., Gratton, E. 3D orbital tracking in a modified two-photon microscope: an application to the tracking of intracellular vesicles. J Vis Exp. , (2014).
- Ritter, J. G., Veith, R., Veenendaal, A., Siebrasse, J. P., Kubitscheck, U. Light sheet microscopy for single molecule tracking in living tissue. PloS one. 5, 11639 (2010).
- Marshall, W. F., Nonaka, S. Cilia: tuning in to the cell’s antenna. Curr Biol. 16, 604-614 (2006).
- Scholey, J. M., Anderson, K. V. Intraflagellar transport and cilium-based signaling. Cell. 125, 439-442 (2006).
- Yang, T. T., et al. Superresolution pattern recognition reveals the architectural map of the ciliary transition zone. Sci Rep. 5, 14096 (2015).
- Craige, B., et al. CEP290 tethers flagellar transition zone microtubules to the membrane and regulates flagellar protein content. J Cell Biol. 190, 927-940 (2010).
- Kee, H. L., et al. A size-exclusion permeability barrier and nucleoporins characterize a ciliary pore complex that regulates transport into cilia. Nat Cell Biol. 14, 431-437 (2012).
- Najafi, M., Maza, N. A., Calvert, P. D. Steric volume exclusion sets soluble protein concentrations in photoreceptor sensory cilia. Proc Natl Acad Sci USA. 109, 203-208 (2012).
- Nachury, M. V., Seeley, E. S., Jin, H. Trafficking to the ciliary membrane: how to get across the periciliary diffusion barrier. Annu Rev Cell Dev Biol. 26, 59-87 (2010).
- Ye, F., et al. Single molecule imaging reveals a major role for diffusion in the exploration of ciliary space by signaling receptors. Elife. 2, 00654 (2013).
- Ross, A. J., et al. Disruption of Bardet-Biedl syndrome ciliary proteins perturbs planar cell polarity in vertebrates. Nat Genetics. 37, 1135-1140 (2005).
- Handel, M., et al. Selective targeting of somatostatin receptor 3 to neuronal cilia. Neuroscience. 89, 909-926 (1999).
- Follit, J. A., Tuft, R. A., Fogarty, K. E., Pazour, G. J. The intraflagellar transport protein IFT20 is associated with the Golgi complex and is required for cilia assembly. Mol Biol Cell. 17, 3781-3792 (2006).
- Awata, J., et al. NPHP4 controls ciliary trafficking of membrane proteins and large soluble proteins at the transition zone. J Cell Sci. 127, 4714-4727 (2014).
- Howarth, M., Ting, A. Y. Imaging proteins in live mammalian cells with biotin ligase and monovalent streptavidin. Nat Protoc. 3, 534-545 (2008).
- Huang, B., Wang, W., Bates, M., Zhuang, X. Three-dimensional super-resolution imaging by stochastic optical reconstruction microscopy. Science. 319, 810-813 (2008).

