Chemoprobe tabanlı bağışıklık sistemini kullanarak KDM1A hedef etkileşimi doğrudan ölçümü
Summary
Burada, bir insan veya hayvan hücresi, KDM1A inhibitörleri ile tedavi edilen doku veya kan örneklerinde KDM1A hedef etkileşimi ölçmek için bir protokol sunuyoruz. Protokol, serbest KDM1A enziminin chemoprobe etiketlemesini ve hedef işgali kemoprob bazlı immünozit kullanarak doğrudan ölçülmesini kullanır ve preklinik ve klinik çalışmalarda kullanılabilir.
Abstract
Bir ilacın, tasarlandığı protein ile etkileşimi olarak tanımlanan hedef etkileşiminin değerlendirilmesi, ilaç gelişiminde veya temel araştırma projelerinde herhangi bir bileşiğin biyolojik aktivitesinin yorumlanmasında temel bir gerekliliktir. Epigenetik olarak, hedef nişan en sık hedef bileşik Birliği ölçmek yerine vekil işaretçileri analizi ile değerlendirilir. Analiz edilmiş olan akım biyolojik okuymalar histon işareti modülasyonu veya gen ifadesi değişikliklerini içerir. KDM1A, metil gruplarını Mono-ve dimethylated H3K4, Gen ifadesinin susturulması ile ilişkili bir modifikasyondan kaldıran bir lizin demethylase ‘dir. Vekil işaretçileri modülasyonu hücre türü ve fonksiyon genetik makyaj, incelenen hücreleri bağlıdır, hangi yorumlama ve çapraz durum karşılaştırma oldukça zor yapabilirsiniz. Bu sorunları aşmak için, doğrudan KDM1A hedef etkileşimi doz etkilerini ve dinamiklerini değerlendirmek için çok yönlü bir protokol sunulmaktadır. Tahlil açıklanan bir KDM1A chemoprobe yakalamak ve Unin, enzim ölçmek için yaygın olarak hücreler veya doku örnekleri genetik modifikasyon için gerek kalmadan uygulanabilir, algılama mükemmel bir pencere vardır ve kullanımı yapar temel araştırma için hem de kullanılabilir ve klinik numunelerin analizi.
Introduction
Lizin spesifik demethylase 1 (KDM1A)1 Gen transkripsiyonu kontrolünde yer alan bir demethylase ‘dir. Bu protein, Onkoloji ‘de bir aday farmakolojik hedef2 olarak ortaya çıkmıştır; Akut myeloid lösemi3 (ayl), myelodisplazi Sendromu (MDS)4, myelofibroz (MF)5,6, küçük hücreli akciğer kanseri (sclc)7; orak hücre hastalığı (SCD)8,9ve Alzheimer hastalığı (reklam), multipl skleroz (MS) dahil olmak üzere merkezi sinir sistemi hastalıklarında; ve saldırganlık10.
Klinik gelişiminde KDM1A inhibe bileşiklerin çoğu siklopropilamin türevleri ve flavin adenin dinükleotid (FAD) kofaktör11için kovalent bağlayıcı tarafından protein inhibe. KDM1A inhibisyonu gen ifade değişikliklerini indükler, ancak bu değişiklikler, doku, hücre türleri veya hastalık vakaları arasında muazzam farklılık gösterir. KDM1A inhibisyonu da histon işaretleri değiştirir12, henüz bu değişiklikler genellikle genom belirli bir sitede yerel olarak üretilir, ve yine, yüksek doku ve hücre spesifik.
Protokol, biyolojik örneklerde KDM1A hedef etkileşimi doğrudan ölçmek için geliştirilmiştir ve siklopropilamin türev inhibitörleri ile kullanılmak üzere optimize edilmiştir. Tahlil ELISA teknolojisi dayanmaktadır ve analiz, paralel olarak, Total ve ücretsiz (yani inhibitör tarafından ilişkisiz) KDM1A bir doğal protein özü bir biyolojik örnek bir katı faz tahlil. İlk adım olarak, biyolojik numune biyotinlenmiş KDM1A seçici chemoprobe OG-881, seçici KDM1A inhibitörü ORY-1001 (ıadademstat), KDM1A klinik olarak güçlü bir inhibitör türetilmiştir, varlığı içinde lysed onkolojik hastalığın tedavisi için gelişme. Chemoprobe bir IC50 için KDM1A 120 nm ve bir FAD bağlayıcı kısım bir biyotinlenmiş Polietilen glikol (PEG)-kuyruk bağlı içerir. Chemoprobe özel olarak ücretsiz KDM1A bağlar, ancak numunenin inhibitörü bağlı KDM1A. Chemoprobe bağladıktan sonra, örnekteki kompleksleri içeren KDM1A, ücretsiz KDM1A belirlemek için streptavidin kaplamalı yüzeyli mikrotiter plaklarda veya toplam KDM1A belirlemek için monoklonal Anti-KDM1A yakalama antikor ile kaplanmış plaklarda yakalanır. Yıkandıktan sonra, her iki plaka bir anti-KDM1A algılama antikor ile inkübe, tekrar yıkanır, ve göreli ölçüm tarafından bir Işıksaçan substrat ve Ölçüleme kullanarak algılama için ikincil bir HRP-konjuate eşek Anti-tavşan IgG antikor ile inkübe ışık ünitelerinin (RLU) bir Luminometre (Şekil 1).
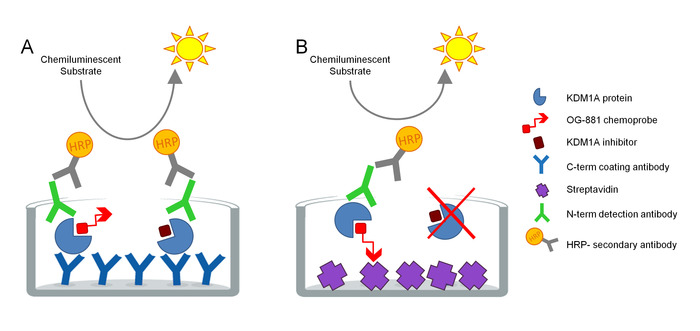
Şekil 1. KDM1A hedef nişan için ELıSA enzim bağlantılı chemoprobe immunemici tahlil şeması: A) Toplam KDM1A sandviç ELISA ve B kullanarak belirlenmesi) ÜCRETSIZ KDM1A chemoprobe ELıSA kullanarak belirlenmesi. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
Her testin doğrusallık doğrulamak için her iki ELıSA plakaları standart bir eğrisi dahil edilir. Her örnekteki KDM1A hedef etkileşimi belirlenmesi daha sonra ön doz veya araç tedavi örnek göreli bir değer olarak hesaplanır.
Protocol
Representative Results
Discussion
Burada sunulan protokol doğrudan KDM1A hedef nişan bir roman KDM1A chemoprobe yakalama tabanlı ELISA kullanarak ölçmek için geliştirilmiştir. Yöntem, insan, sıçan ve fare ve babun (pbmcs, akciğer, beyin, cilt, tümörler dahil), ama kolayca diğer türler için uygulanabilir hangi KDM1A antikor hedef epitopları ve katalitik olarak kültürlü insan hücresi hatları ve ex vivo örnekleri üzerinde doğrulandı Merkezi temin edilmektedir. OG-881 bir aktivite bazlı chemoprobe olduğu için, örnek kalite öne…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Bu çalışmada Oryzon Genomics tarafından finanse edilmiştir. S.A., Hoffman-La Roche ve CIıP-20152001 ve RETOS işbirliği programı RTC-2015-3332-1 tarafından kısmen desteklenmektedir.
Materials
| 0,05% Trypsin-EDTA (1X) | Thermo Scientific | #25300-062 | |
| 10 X Protease Inhibitor Tablets | Roche | #11836153001 | |
| 96 deep well storage block | VWR | #734-1679 | |
| 96 well ELISA plates | Nunc | #436110 | |
| Adhesive black Film | Perkin Elmer | #6050173 | |
| Adhesive transparent Film | VWR | #60941-062 | |
| Biotinylated KDM1A probe OG-881 | Oryzon Genomics S.A. | NA | |
| Bovine Serum Albumin | Sigma | # 3117057001 | |
| Bovine Serum Albumin Standard | Thermo Scientific | #23208) | |
| Bradford Protein Assay | BioRad | #500-0001 | |
| Cell lysis buffer 10X | Cell Signaling | #9803 | |
| Centrifuge for 96- well plates | Hettich | Rotina 420R | |
| Flask | Thermo Scientific | #156499 | |
| Full length, enzymatically active human Recombinant LSD1 / KDM1A | Active Motif | #31426 | |
| Graphpad Prism 5 Project | GraphPad Software | NA | |
| Luminol-Enhacer and Peroxide Solution (Chemiluminescent Substrate) | Thermo Scientific | #37074 | |
| Micro Centrifuge | Eppendorf | 5415 R | |
| Microplate reader Infinite 200-Tecan | Tecan | Infinite 200 | |
| Mouse monoclonal capture antibody Anti-KDM1A (N-terminal epitope) | Abcam | #ab53269 | |
| Needle G18 gauge blunt | BD | #303129 | |
| ORY-1001 (iadademstat) | Oryzon Genomics S.A. | NA | |
| PBMC separation tubes 10 ml | Greiner bio-one | #163288 | |
| PBMC separation tubes 50 ml | Greiner bio-one | #227288 | |
| PBS 1x | Sigma | #D8537 | |
| Plate shaker | Heidolph Instruments | Rotamax 120 | |
| Polysorbate 20 | Sigma | #P7949 | |
| Rabbit monoclonal detection antibody Anti-KDM1A (C-terminal epitope) | Cell Signaling | #672184BF-100 | |
| Secondary antibody Peroxidase-conjugated Donkey Anti-rabbit IgG | Thermo Scientific | #31458 | |
| Spectrophotometer cuvette 1.5 | Deltalab | #302100 | |
| Spectrophotometer for cuvette | GE Healthcare | GeneQuant 1300 | |
| Streptavidin | Promega | #Z704A | |
| Syringe | BD | #303172 | |
| Type 1 ultrapure water | Millipore | Milli-Q Advantage A10 | |
| Ultrasonic cleaner | VWR | USC200T |
References
- Shi, Y. Histone demethylation mediated by the nuclear amine oxidase homolog LSD1. Cell. 119 (7), 941-953 (2004).
- Maiques-Diaz, A., Somervaille, T. C. LSD1: biologic roles and therapeutic targeting. Epigenomics. 8 (8), 1103-1116 (2016).
- Maes, T. ORY-1001, a Potent and Selective Covalent KDM1A Inhibitor, for the Treatment of Acute Leukemia. Cancer Cell. 33 (3), 495-511 (2018).
- Sugino, N. A novel LSD1 inhibitor NCD38 ameliorates MDS-related leukemia with complex karyotype by attenuating leukemia programs via activating super-enhancers. Leukemia. 31 (11), 2303-2314 (2017).
- Kleppe, M., Shank, K., Efthymia, P., Riehnhoff, H., Levine, R. L. Lysine-Specific Histone Demethylase, LSD1, (KDM1A) As a Novel Therapeutic Target in Myeloproliferative Neoplasms. Blood. 126, 601 (2015).
- Jutzi, J. S., et al. LSD1 Inhibition Prolongs Survival in Mouse Models of MPN by Selectively Targeting the Disease Clone. HemaSphere. 2 (3), 54 (2018).
- Mohammad, H. P. DNA Hypomethylation Signature Predicts Antitumor Activity of LSD1 Inhibitors in SCLC. Cancer Cell. 28 (1), 57-69 (2015).
- Rivers, A., et al. RN-1, a potent and selective lysine-specific demethylase 1 inhibitor, increases γ-globin expression, F reticulocytes, and F cells in a sickle cell disease mouse model. Experimental Hematology. 43 (7), 546-553 (2015).
- Rivers, A. Oral administration of the LSD1 inhibitor ORY-3001 increases fetal hemoglobin in sickle cell mice and baboons. Experimental Hematology. 67, 60-64 (2018).
- Buesa, C., et al. The dual LSD1/MAO-B inhibitor ORY-2001 prevents the development of the memory deficit in samp8 mice through induction of neuronal plasticity and reduction of neuroinflammation. Alzheimer’s & Dementia. 11 (7), P905 (2015).
- Schmidt, D. M., McCafferty, D. G. Trans-2-Phenylcyclopropylamine is a mechanism-based inactivator of the histone demethylase LSD1. Biochemistry. 46 (14), 4408-4416 (2007).
- Forneris, F., Binda, C., Vanoni, M. A., Battaglioli, E., Mattevi, A. Human histone demethylase LSD1 reads the histone code. Journal of Biological Chemistry. 280 (50), 41360-41365 (2005).
- Gonz#225;lez, E. C., Maes, T., Crusat, C. M., Mu#241;oz, A. O. Oryzon Genomics, Methods to determine kdm1a target engagement and chemoprobes useful therefor. , (2016).
- Mascaró, C., Ortega, A., Carceller, E., Rruiz Rodriguez, R., Cicero, F., Lunardi, S., Yu, L., Hilbert, M., Maes, T. Chemoprobe-based assays of histone lysine demethylase 1A target occupation enable in vivo pharmacokinetics and -dynamics studies of KDM1A inhibitors. Journal of Biological Chemistry. , (2019).
- Rodriguez-Suarez, R. Development of Homogeneous Nonradioactive Methyltransferase and Demethylase Assays Targeting Histone H3 Lysine 4. Journal of Biomolecular Screening. 17 (1), 49-58 (2011).
- Lynch, J. T., Cockerill, M. J., Hitchin, J. R., Wiseman, D. H., Somervaille, T. C. CD86 expression as a surrogate cellular biomarker for pharmacological inhibition of the histone demethylase lysine-specific demethylase 1. Analytical Biochemistry. 442 (1), 104-106 (2013).
- Schulz-Fincke, J. Structure-activity studies on N-Substituted tranylcypromine derivatives lead to selective inhibitors of lysine specific demethylase 1 (LSD1) and potent inducers of leukemic cell differentiation. European Journal of Medicinal Chemistry. 144, 52-67 (2018).
- Ishii, T., et al. CETSA quantitatively verifies in vivo target engagement of novel RIPK1 inhibitors in various biospecimens. Scientific Report. 7, 13000 (2017).
- Maes, T. ORY-2001: An Epigenetic drug for the treatment of cognition defects in Alzheimer’s disease and other neurodegenerative disorders. Alzheimer’s & Dementia. 12 (7), P1192 (2017).

